Коррозия металлов. Виды коррозии.
Коррозия металлов –разрушение металлов и их сплавов в результате воздействия на них окружающей среды.
По механизму процесса различают химическую и электрохимическую коррозию металлов.
Химическая коррозия — это процесс взаимодействия металла с коррозионной средой, при котором окисление металла и восстановление окислительного компонента среды протекают единовременно в одном акте. Продукты взаимодействия пространственно не разделены.
Электрохимическая коррозия — это процесс взаимодействия металла с коррозионной средой (раствором электролита), при котором ионизация атомов металла и восстановление окислительного компонента коррозионной среды протекают не в одном акте и их скорости зависят от электродного потенциала.
По виду коррозионной среды и условиям протекания различают несколько видов коррозии.
Газовая коррозия - это химическая коррозия металлов в газовой среде при минимальном содержании влаги (как правило не более 0,1%) или при высоких температурах. В химической и нефтехимической промышленности такой вид коррозии встречается часто. Например, при получении серной кислоты на стадии окисления диоксида серы, при синтезе аммиака, получении азотной кислоты и хлористого водорода, в процессах синтеза органических спиртов, крекинга нефти и т.д.
Атмосферная коррозия — это коррозия металлов в атмосфере воздуха или любого влажного газа.
Подземная коррозия — это коррозия металлов в почвах и грунтах.
Биокоррозия— это коррозия, протекающая под влиянием жизнедеятельности микроорганизмов.
Контактная коррозия — это вид коррозии, вызванный контактом металлов, имеющих разные стационарные потенциалы в данном электролите.
Радиационная коррозия - это коррозия, обусловленная действием радиоактивного излучения.
Коррозия внешним током и коррозия блуждающим током. В первом случае — это коррозия металла, возникающая под воздействием тока от внешнего источника. Во втором случае — под воздействием блуждающего тока.
Коррозия под напряжением — коррозия, вызванная одновременным воздействием коррозионной среды и механических напряжений. Если это растягивающие напряжения, то может произойти растрескивание металла. Это очень опасный вид коррозии, особенно для конструкций, испытывающих механические нагрузки (оси, рессоры, автоклавы, паровые котлы, турбины и т.д.). Если металлические изделия подвергаются циклическим растягивающим напряжениям, то можно вызвать коррозионную усталость. Происходит понижение предела усталости металла. Такому виду коррозии подвержены рессоры автомобилей, канаты, валки прокатных станов.
Коррозионная кавитация — разрушение металла, обусловленное одновременным коррозионным и ударным воздействием внешней среды.
Фреттинг-коррозия — это коррозия, вызванная одновременно вибрацией и воздействием коррозионной среды. Устранить коррозию при трении или вибрации возможно правильным выбором конструкционного материала, снижением коэффициента трения, применением покрытий и т.д.
Коррозия называется сплошной, если она охватывает всю поверхность металла. Сплошная коррозия может быть равномерной, если процесс протекает с одинаковой скоростью по всей поверхности металла, и неравномерной когда скорость процесса неодинакова на различных участках поверхности. Равномерная коррозия наблюдается, например, при коррозии железных труб на воздухе.
При избирательной коррозии разрушается одна структурная составляющая или один компонент сплава. В качестве примеров можно привести графитизацию чугуна или обесцинкование латуней.
Местная (локальная) коррозия охватывает отдельные участки поверхности металла. Местная коррозия может быть выражена в виде отдельных пятен, не сильно углубленных в толщу металла; язв - разрушений, имеющих вид раковины, сильно углубленной в толщу металла, или точек (питтингов), глубоко проникающих в металл.
Первый вид наблюдается, например, при коррозии латуни в морской воде. Язвенная коррозия отмечена у сталей в грунте, а питтинговая — у аустенитной хромоникелевой стали в морской воде.
Подповерхностная коррозия начинается на поверхности, но затем распространяется в глубине металла. Продукты коррозии оказываются сосредоточенными в полостях металла. Этот вид коррозии вызывает вспучивание и расслоение металлических изделий.
Межкристаллитная коррозия характеризуется разрушением металла по границам зерен. Она особенно опасна тем, что внешний вид металла не меняется, но он быстро теряет прочность и пластичность и легко разрушается. Связано это с образованием между зернами рыхлых малопрочных продуктов коррозии. Этому виду разрушений особенно подвержены хромистые и хромоникелевые стали, никелевые и алюминиевые сплавы.
2. Направленность химической связи. Гибридизация атомных орбиталей. Строение простейших молекул.
Химическая связь направлена туда, где обеспечивается наибольшее перекрывание электронных облаков.
Гибридизация орбиталей — гипотетический процесс смешения разных (s, p, d) орбиталей центрального атома многоатомной молекулы с возникновением того же числа орбиталей, эквивалентных по своим характеристикам.
+ то что в тетради!!!
3. Вычислите массовую долю, моляльную концентрацию и мольную долю хлорида бария в растворе, содержащем 50 г BaCl2×2H2O в 1000 г воды.
----------------------------------------------------------------------------------------------------------------------------------
ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ № 40
1. Контактная коррозия металлов.
Контактная коррозия — это вид коррозии, вызванный контактом металлов, имеющих разные стационарные потенциалы в данном электролите.
При контакте двух разнородных металлов на их поверхности реализуется компромиссный потенциал, который по своему значению отличается от потенциалов каждого металла по отдельности. Компромиссный потенциал определяется пересечением суммарных поляризационных кривых: анодной и катодной.
При контактной коррозии анодом будет тот металл, который обладает более электроотрицательным потенциалом, катод при этом имеет более электроположительный. Скорость растворения катода может быть выше, ниже либо равна его собственной скорости растворения в том же электролите.
2. Квантовые числа. Электронные спектроскопические формулы атомов.
Квантовые числа — энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится.
Главное квaнтовое число n определяет общую энергию электрона и степень его удаления от ядра (номер энергетического уровня); оно принимает любые целочисленные значения, начиная с 1 (n = 1, 2, 3, . . .)
Орбитальное (побочное или азимутальное) квантовое число l определяет форму атомной орбитали. Оно может принимать целочисленные значения от 0 до n-1 (l = 0, 1, 2, 3,..., n-1). Каждому значению l соответствует орбиталь особой формы. Орбитали с l = 0 называются s-орбиталями,
l = 1 – р-орбиталями (3 типа, отличающихся магнитным квантовым числом m),
l = 2 – d-орбиталями (5 типов),
l = 3 – f-орбиталями (7 типов).
Магнитное квантовое число m определяет ориентацию орбитали в пространстве относительно внешнего магнитного или электрического поля. Его значения изменяются от +l до -l, включая 0. Например, при l = 1 число m принимает 3 значения: +1, 0, -1, поэтому существуют 3 типа р-АО: рx, рy, рz.
Спиновое квантовое число s может принимать лишь два возможных значения +1/2 и -1/2. Они соответствуют двум возможным и противоположным друг другу направлениям собственного магнитного момента электрона, называемого спином (от англ. веретено). Для обозначения электронов с различными спинами используются символы: 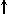 и
и 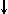 ..
..
СПЕКТРОСКОПИЯ,раздел физики, посвященный изучению спектров электромагнитного излучения. Здесь мы рассмотрим оптическую спектроскопию часто называют просто спектроскопией. Каждый атом и молекула имеют уникальное строение, которому соответствует свой уникальный спектр. Структура спектра атома или молекулы определяется их энергетическими уровнями. Согласно законам квантовой механики, каждый энергетический уровень соответствует определенному квантовому состоянию. Электроны и ядра в таком состоянии совершают характерные периодические движения, для которых энергия, орбитальный момент количества движения и другие физические величины строго определены, т.е. принимают лишь разрешенные дискретные значения. Если известны силы, связывающие электроны и ядра в единую систему, то по законам квантовой механики можно рассчитать ее уровни энергии и квантовые числа, а также предсказать интенсивности и частоты спектральных линий. С другой стороны, анализируя спектр конкретной системы, можно определить энергии и квантовые числа состояний, а также сделать выводы относительно действующих в ней сил. Таким образом, спектроскопия является основным источником сведений о квантово-механических величинах и о строении атомов и молекул.
3. Вычислите молярность и нормальность 20 %-ного раствора хлорида кальция с плотностью 1,178 г/см3.
Мольная масса хлорида кальция равна 111. Следовательно,
m(CaCl2) = 111 и э(CaCl2) = 111 : 2 = 55,5.
а) Молярная концентрация 20% раствора хлорида кальция равна
M = (c · p · 10) / m = (20 · 1,178 · 10) / 111 = 2,1 M
б) Нормальная (эквивалентная) концентрация 20% раствора хлорида кальция равна
N = (c · p · 10) / э = (20 ·1,178 ·10) / 55,5 = 4,2 H.
------------------------------------------------------------------------------------------------------------------------------
ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ № 41
