Лабораторная работа № 5. Получение и свойства хлорэтана
Цель: получить хлорэтан и его идентификация.
Формируемые умения:
· собирать прибор для получения газа, монтировать его в штатив
· нагревать стеклянную посуду с жидкими веществами
· получать хлорэтан из этанола
· поджигать выделяющийся газ
· работать с концентрированной серной кислотой
· идентифицировать хлорэтан по цвету пламени
Реактивы и оборудование: смесь этилового спирта и концентрированной серной кислоты в отношении 2:1 (по объему), хлорид натрия; прямые газоотводные трубки с оттянутым концом, пробирки.
Методика
В пробирку поместите 2 лопаточки хлорида натрия, прилейте 8—10 капель этанола и 4—5 капель концентрированной серной кислоты. Пробирку закройте пробкой с газоотводной трубкой и осторожно нагрейте на слабом пламени горелки. Подожгите выделяющийся хлороэтан у отверстия газоотводной трубки. Он загорается, образуя колечко зеленого цвета (образование хлороэтана начинается не сразу). Напишите уравнения реакции, механизм (SN2).
Литература для самостоятельной работы
Органическая химия: Учебник для вузов: В 2 кн./В.Л. Белобородов, С.Э. Зурабян, А.П. Тюкавкина; Под ред. Н.А. Тюкавкиной. - М.: Дрофа, 2002. – Кн. 1: Основной курс. – 620с. (С. 300 – 301)
Лабораторно-практическое занятие № 23. «Спирты и тиолы: строение и свойства» (2ч)
Цель:сформировать знания о строении и реакционной способности спиртов, их тиоаналогов.
Вопросы для обсуждения:
1. Спирты и тиолы, их реакционные центры и свойства.
2. Кислотно-основные свойства спиртов и тиолов.
3. Реакции нуклеофильного замещения у спиртов и тиолов.
4. Окисление спиртов и тиолов. Реакции элиминирования .
Материалы и примеры для самостоятельного изучения
Пример 1. Объясните различное отношение спиртов и тиолов к окислению.
Под окислением в органической химии понимают реакции, в которых происходит удаление из молекулы атомов водорода или образование связей с более электроотрицательными атомами, чем водород. Окисление происходит вследствие переноса электронов от способной окисляться молекулы к реагенту—окислителю.
Этанол и этантиол относятся соответственно к классам спиртов и тиолов.
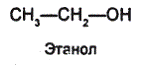
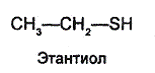
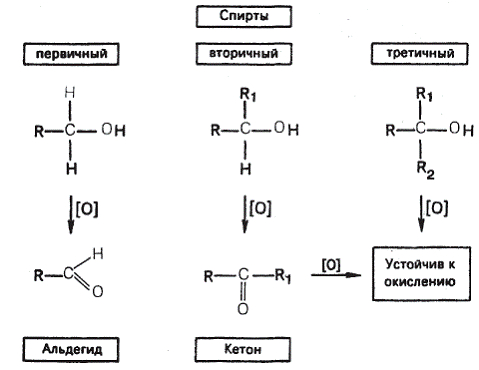
Отношение спиртов к окислению определяется наличием или отсутствием атома водорода у 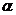 -углеродного атома. Первичные спирты окисляются в альдегиды, вторичные — в кетоны; третичные спирты, у которых
-углеродного атома. Первичные спирты окисляются в альдегиды, вторичные — в кетоны; третичные спирты, у которых 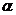 -углеродный атом не связан с атомом водорода, устойчивы к окислению.
-углеродный атом не связан с атомом водорода, устойчивы к окислению.
В лабораторных условиях для окисления спиртов используют хромовую кислоту Н2СrО4 из хромовой смеси (К2Сг2О7 + H2SO4). При этом хром(VI) восстанавливается а хром(III).
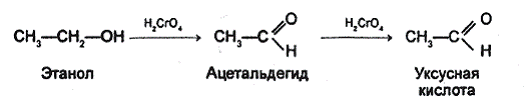
Образующиеся при окислении первичных спиртов альдегиды очень легко окисляются в кислоты. Для окисления альдегидов используют мягкие окислители — аммиачный раствор оксида серебра, раствор гидроксида меди(II). С помощью этих окислителей проводят качественные реакции на альдегидную группу.
Тиолы легко окисляются в дисульфиды, а дисульфиды легко восстанавливаются вновь в тиолы. Например, в мягких условиях этантиол окисляется с образованием диэтилдисульфида.
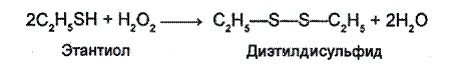
Различие в способности к окислению спиртов и тиолов объясняется меньшей энергией связи S—Н (330 кДж/моль) по сравнению со связью О—Н (464 кДж/моль). При окислении спиртов вместо прочной О—Н связи расщеплению подвергается более слабая связь С—Н (414 кДж/моль), что приводит к образованию иных продуктов окисления.
Задачи для самостоятельного решения
Задача 23.1.Назовите следующие соединения:
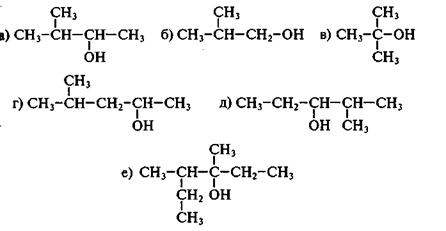
Задача 23.2 .Напишите формулы следующих соединений:
а) спирт листьев (запах листьев и свежей травы) — цис-гексен-3-ол-1;
б) бомбикол (аттрактант самки тутового шелкопряда) — пентадекадиен- 10,12-ол-1;
в) фитол (составная часть хлорофилла) — 3,7,11,15-тетраметилгексадецен-2-ол-1;
г) цитронеллол — 3,7-диметилоктен-6-ол-1;
д) гераниол — транс-3,7-диметилоктадиен-2,6-ол-1;
е) нерол (жидкость с запахом розы, содержащаяся в гераниевом и розовом маслах) — цис-изомер гераниола.
Задача 23.3.Приведите структурные формулы ненасыщенных спиртов и тиолов состава С4Н7SН, С5Н10(ОН)2. Назовите их согласно систематической номенклатуре; напишите, если возможно, геометрические изомеры.
Задача 23.4.Изобразите схему строения молекул метанола и этантиола с помощью атомных орбиталей. Укажите особенности распределения электронной плотности и основные реакционные центры.
Задача 23.5. Нарисуйте схему образования водородной связи между молекулами этанола и воды. Как водородная связь влияет на температуру кипения веществ и их растворимость? Сравните эти свойства для метанола , этанола, этантиола и диэтилового эфира.
Задача 23.6.Как объяснить уменьшение растворимости спиртов нормального строения в воде при увеличении их молекулярной массы? Какие фрагменты молекулы спирта обладают гидрофобными свойствами, какие — гидрофильными?
Задача 23.7.Расположите спирты в порядке усиления кислотных свойств:
а) этанол, бутанол-1, пропанол-1;
б) метанол, пропанол-2, пропанол-1, 2-метилпропанол-2. Ответ обоснуйте.
Задача 23.8.Расположите спирты: этанол, пропандиол-1,3, этандиол-1,2, пропантриол-1,2,3 — в порядке усиления кислотных свойств. Объясните взаимное влияние гидроксильных групп.
Задача 23.9.Назовите вещества, образующиеся при взаимодействии:
а) пропанола-1 с натрием;
б) этантиола с магнием (опилки);
в) бутанола-1 с кальцием;
г) глицерина с гидроксидом натрия (2 моль);
д) этиленгликоля с гидроксидом калия (1 моль);
е) глицерина с оксидом кальция (2 моль). Напишите уравнения реакций.
Задача 23.10. Напишите уравнения реакций бромоводорода со следующими спиртами:
а) пропанол-1;
б) пропанол-2;
в) 2-метилпропанол-2.
Для реакций с участием пропанол-1 и 2-метилпропанол-2 объясните механизм процесса
Задача 23.11. Из каких спиртов, действуя на них соответствующим галогеноводородом, можно получить:
а) 2-метил-3-хлоробутан;
б) 2-иодо-2-метилпропан;
в) 1-бромо-2-метилпропан?
Напишите уравнения реакций; укажите механизм, по которому они протекают, их молекулярность.
Задача 23.12. Напишите уравнения реакций дегидратации и этерификации с молекулой уксусной кислоты следующих спиртов:
а) пропанол-2;
б) бутанол-2;
в) 2-метилбутанол-2;
г) 2,3-диметилпентанол-2.
Какие из спиртов легче подвергаются дегидратации?
Задача 23.13. Какие вещества образуются при окислении:
а) бутанол-1;
б) пропанол-2;
в) 2-метилбутанола-1;
г) 2,4-диметилпентанола-3?
Задача 23.14. Напишите уравнения возможных реакций бутанол-2 и этиленгликоля со следующими реагентами:
а) Nа(мет.);
б) РС15;
в) гидроксид меди (II);
г) KMnO4 + H2SO4.
Задача 23.15. Напишите схемы следующих превращений:
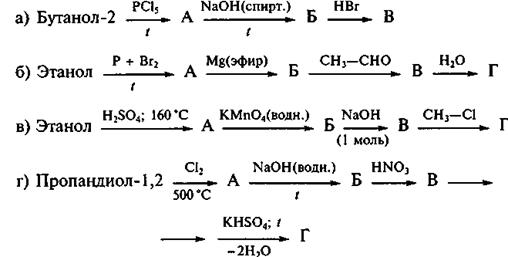
Литература для самостоятельной работы
Органическая химия: Учебник для вузов: В 2 кн./В.Л. Белобородов, С.Э. Зурабян, А.П. Тюкавкина; Под ред. Н.А. Тюкавкиной. - М.: Дрофа, 2002. – Кн. 1: Основной курс. – 620с. (С. 340 – 363; 408- 418)
