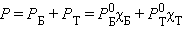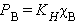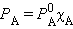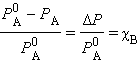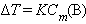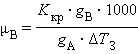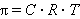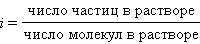Выполнить вопрос из теста № 22.
Лабораторная работа №2.
Растворимость солей.
Цели:
1. Изучить способность солей к растворимости.
2. Экспериментально оценить растворимость сульфатов и карбонатов (по величине осадков в пробирке) Na, Mg, Ca, Sr, Ba, Pb.
3. Составить ряд по уменьшению растворимости по сульфатам и карбонатам.
4. Найдите в справочнике величину ПР соответствующих сульфатов и карбонатов.
5.Составить ряд по уменьшению ПР ( уменьшению растворимости) сульфатов и карбонатов.
6. Сравнить оба ряда и сделать выводы.
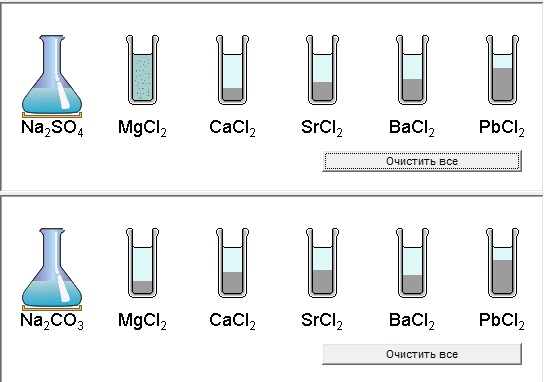 |
| Модель 6.2. Растворимость солей. Эта модель демонстрирует растворимость солей ряда металлов: магния, кальция, стронция, бария, свинца. В модели можно исследовать растворимость сульфатов и карбонатов этих металлов. Количество осадка, изображаемого в пробирке, символизирует растворимость соответствующего сульфата или карбоната (чем больше осадка, тем меньше растворимость). В процессе экспериментов вы можете убедиться, что растворимость соли зависит не только от катиона, но и от аниона. Из сульфатов исследуемых металлов полностью растворим только MgSO4. Растворимость сульфатов уменьшается в следующем ряду: CaSO4 > SrSO4 > PbSO4 > BaSO4. Полностью растворимых солей среди карбонатов изучаемых металлов нет. Растворимость уменьшается в следующем порядке: MgCO3 > CaCO3 > BaCO3 > SrCO3 > PbCO3. Выполнить вопросы №22, №26 из теста. |
Растворимостью вещества при данных условиях называют его концентрацию в насыщенном растворе. В таком растворе достигается равновесие между растворяемым веществом и раствором. В отсутствие равновесия раствор остается стабильным, если концентрация растворенного вещества меньше его растворимости (ненасыщенный раствор), или нестабильным, если в растворе содержится вещества больше его растворимости (пересыщенный раствор).
Растворы неэлектролитов.
По термодинамическому признаку растворы делятся на идеальные и реальные. Для идеальных растворов предполагается, что между компонентами раствора любыми взаимодействиями можно пренебречь. Следовательно, любое свойство растворяемых веществ при их смешении не должно меняться. Например, при смешении близких по свойствам бензола и толуола давление пара P над раствором в соответствии с законом Рауля будет аддитивной величиной
|
Здесь 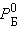 и
и 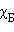 ,
, 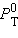 и
и 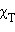 – соответственно давление и мольные доли бензола и толуола.
– соответственно давление и мольные доли бензола и толуола.
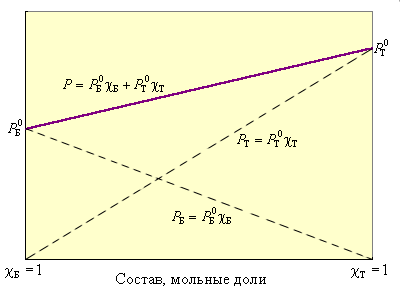 |
| Рисунок 6.1. Зависимость давления пара над смесью бензол–толуол от мольной доли. |
Если раствор сохраняет свойства идеальности при любых концентрациях, его называют идеальным (растворы изотопов). Часто раствор приобретает эти качества только при достаточно большом разведении, это – «бесконечно разбавленный» раствор при χ→0. Во всех прочих случаях раствор считается реальным.
Взаимодействие между компонентами раствора, выражаемое через энтальпию сольвации ΔHсольв, служит в определенных пределах мерой идеальности раствора. Д. И. Менделеев показал, что взаимодействие между компонентами раствора может рассматриваться как химический процесс образования соединений переменного состава – сольватов. Этот подход лежит в основе химической или сольватной теории растворов. Если при кристаллизации твердая фаза содержит молекулы растворителя, то ее называют кристаллосольватом.
Закон Генри.
Если растворенное вещество характеризуется большой упругостью пара по сравнению с упругостью пара растворителя (PB >> PA) и при этом оба компонента раствора химически инертны, то растворение такого газообразного вещества в жидкости подчиняется закону Генри: при постоянной температуре давление летучего (газообразного) компонента PB прямо пропорционально его мольной доле χB:
| (6.1) |
KH – константа Генри.
В табл. 6.1 приведены константы Генри некоторых газов для воды.
| ||||||||||||||
| Таблица 6.1. Константы Генри для воды при 298 K. |
Из уравнения (6.1) следует, что KH определяется выбором единиц давления и концентрации.
Законы Рауля.
Если упругость пара растворенного вещества очень мала PB << PA, то его парциальным давлением можно пренебречь (нелетучий компонент), и тогда упругость пара над раствором будет зависеть только от парциального давления растворителя:
|
Это первый закон Рауля – парциальное давление над раствором прямо пропорционально мольной доле растворенного вещества. После подстановки χA = 1 – χB и несложных преобразований
 |
получаем
|
Относительное понижение упругости пара над раствором равно мольной доле растворенного вещества. Это закон Рауля для нелетучего растворенного компонента. Из этого закона можно вывести два следствия, которые в объединенном виде формируются как второй закон Рауля.
 |
| Рисунок 6.2. Зависимость повышения температуры кипения ΔTкип и понижения температуры замерзания ΔTзам раствора от концентрации растворенного вещества. |
На рис. 6.2 приведены зависимости P(T) чистого растворителя и двух его растворов P'(T) и P''(T).
Выразим мольную долю 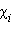 через моляльную концентрацию
через моляльную концентрацию 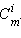 Для двухкомпонентного раствора
Для двухкомпонентного раствора 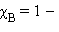
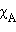 . При
. При 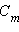 << 1 получим
<< 1 получим
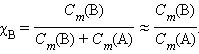 |
Из подобия треугольников следует
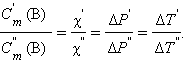 |
По определению, при  (B) = 1 моль∙
(B) = 1 моль∙ 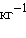 повышение температуры
повышение температуры 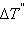 равно
равно 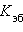 – эбулиоскопической константе для данного растворителя. Тогда повышение температуры кипения для данного раствора будет пропорционально его моляльной концентрации:
– эбулиоскопической константе для данного растворителя. Тогда повышение температуры кипения для данного раствора будет пропорционально его моляльной концентрации:
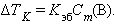 |
Проведя аналогичное исследование, касающееся понижения температуры замерзания раствора, получим
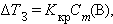 |
где Kкр – криоскопическая константа.
Второй закон Рауля – понижение температуры кипения и повышение температуры замерзания раствора прямо пропорционально моляльной концентрации раствора:
|
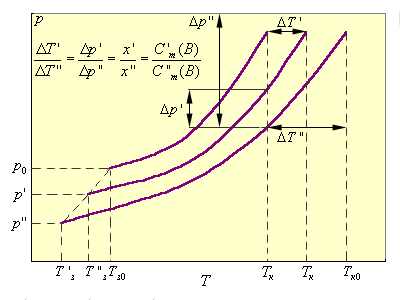
Kэб и Kкр являются экстраполяционными величинами от малых концентраций растворенного вещества, где выполняется этот закон, на Cm(B) = 1, где этот закон уже не действует (рис. 6.3). В табл. 6.2 приведены Kкр и Kэф для воды и бензола.
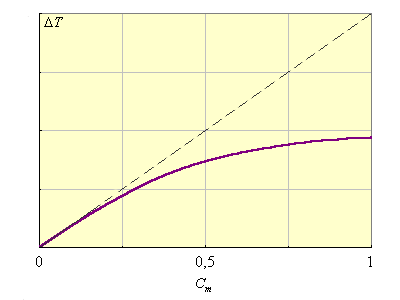 |
| Рисунок 6.3. Иллюстрация справедливости второго закона Рауля для разбавленных растворов и экстраполяционной природы Kкр и Kэб. |
| |||||||||
| Таблица 6.2. Криоскопические и эбулиоскопические константы для воды и бензола (град∙моль–1∙кг). |
Второй закон Рауля дает легко осуществимую экспериментально возможность определения молекулярных масс некоторых молекулярных соединений, неспособных к диссоциации в данном растворителе. Действительно, моляльная концентрация растворенного вещества может быть представлена в виде соотношения Cm = gB ∙ 1000 / μB ∙gA, где gA – вес растворителя, gB – вес растворенного вещества, μB – его молярная масса. Тогда из ΔT = Kкр · m получим молярную массу растворенного вещества:
|
Осмос.
Если система, разделенная мембраной, представляет собой растворы, в которых через мембрану способны проходить только молекулы растворителя, то свойства ее будут определяться разностью мольных долей (концентраций) растворителя по обе стороны мембраны.
Явление, связанное со способностью проходить через мембрану, в частности, только молекул растворителя, называется осмосом, а вызываемое им изменение давления по обе стороны мембраны – осмотическим давлением. Явление осмоса чрезвычайно разнообразно и во многом определяется природой мембраны и компонентов раствора.
Лабораторная работа №3.
Осмос.
Цели:
1. Изучить понятие «осмос».
2. Наблюдать явление в ходе лабораторной работы.
3. Вычислить осмотическое давление (Р).
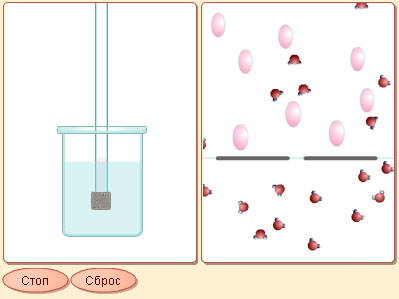 |
| Модель 6.3. Осмос. Эта модель демонстрирует явление осмоса как в мелком, так и в крупном масштабе. Вы видите неподвижные стакан и трубку с водой за пористой перегородкой в левом окне, а в правом окне, в крупном масштабе – движение молекул воды в стакане. Затем трубка начинает опускаться в стакан, в результате чего молекулы воды из стакана могут переходить в трубку сквозь пористую перегородку. Однако их обратное проникновение затруднено наличием растворенного вещества (схематически показанного в модели розовыми образованиями оваль ной формы), не проникающего через пористую перегородку. В результате молекулы воды реже проходят в обратном, нежели в прямом направлении. Это и создает суммарный поток молекул воды, направленный в трубку, и уровень воды в ней начинает повышаться. Он повышается до тех пор, пока избыточное давление воды в трубке не уравняет потоки молекул в ту и в другую сторону. Это избыточное давление и называется осмотическим давлением. |
Выполнить вопросы №25 из теста.
Представим, что сосуд с двумя горлами для залива раствора разделен мембраной M (рис. 6.4). В каждую часть сосуда зальем растворы, отличающиеся только концентрацией. Поскольку мольные доли растворителя по обе стороны мембраны не совпадают, то стремление их к выравниванию приведет к переходу части растворителя в ту часть сосуда, где концентрация растворенного вещества больше. Увеличение количества растворителя эквивалентно возрастанию давления, и если мембрана способна к деформации, она изогнется в сторону с меньшей концентрацией растворенного вещества (рис. 6.4а).
Если мембрана жесткая, то в отсеке с большей концентрацией количество растворителя будет возрастать до тех пор, пока гидростатическое давление h (рис. 6.4б) не станет равным осмотическому давлению и не прекратит осмос.
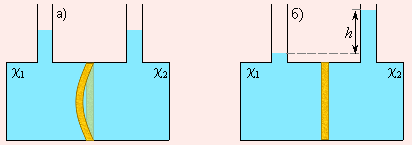 |
| Рисунок 6.4. Схема разности осмотических давлений при χ1 < χ2 при эластичной (а) и жесткой (б) мембранах. |
Осмотическое давление π – внутреннее давление растворенного вещества, численно равное тому внешнему давлению, которое нужно приложить, чтобы прекратить осмос; оно зависит от температуры и концентрации.
Эту зависимость Вант-Гофф уподобил поведению идеального газа:
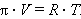 |
По Вант-Гоффу осмотическое давление раствора численно равно тому газовому давлению, которое имело бы растворенное вещество, будучи переведенным в газообразное состояние в том же объеме и при той же температуре. Поскольку объем (разбавление) обратно пропорционален концентрации, то закон Вант-Гоффа можно записать в виде
|
Так как объем одного моля газообразного вещества при нормальных условиях равен 22,4 литра, то осмотическое давление раствора, содержащего 1 моль вещества, равно 22,4 атм.
Измерение осмотического давления раствора используется для определения молекулярных масс даже разбавленных растворов, что позволяет оценивать молекулярные массы растворимых высокомолекулярных соединений, в частности, биополимеров. Заменив C(B) в формуле Вант-Гоффа соотношением (m(B) ∙ 1000 / μ(B) ∙ V), получим уравнение, позволяющее вычислять молекулярные массы растворенных веществ:
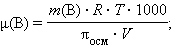 |
m(B) – масса растворенного вещества, V – объем раствора.
Если растворы характеризуются одинаковыми осмотическими давлениями, то по Вант-Гоффу такие растворы называются изотоническими. Независимо от природы растворенного вещества, изотоничность является следствием одинакового числа частиц в растворе.
Поскольку при растворении реальное число частиц может отличаться от числа растворенных молекул, Вант-Гофф ввел понятие изотонического коэффициента i. По определению это отношение числа всех частиц к числу растворенных молекул:
| (6.1) |
В бензольном растворе уксусной кислоты i < 1, ибо в этом растворе число частиц меньше числа молекул, в результате реакции ассоциации в соответствие с уравнением
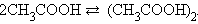 |
Если же в растворе преобладает не ассоциативный, а диссоциативный или ионизационный механизмы взаимодействия, то i > 1. Так, в водном растворе уксусная кислота диссоциирует CH3COOH = CH3COO– + H+, и число частиц становится больше числа молекул.
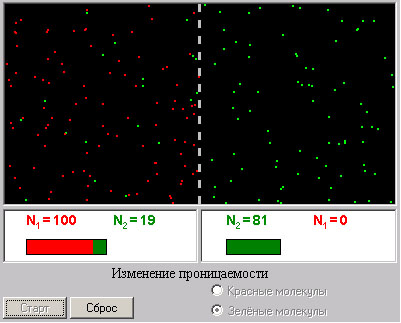 |
| Модель 6.4. Полунепроницаемая мембрана. |
Моделируется процесс возникновения осмотического давления в системе с полупроницаемой перегородкой. Перегородка, разделяющая сосуд на две половины, проницаема для одного из газов и непроницаема для другого. Модель позволяет продемонстрировать закон Дальтона для смеси газов.
Если в сосуде находится смесь газов, то каждый из них вносит свой вклад в общее давление. Парциальным давлением называют давление одного из газов при условии, что все остальные удалены из сосуда. Экспериментально установленный закон Дальтона утверждает: давление в смеси химически невзаимодействующих газов равно сумме их парциальных давлений:
| P = P1 + P2 + ... |
При этом парциальное давление каждого из газов подчиняется в случае достаточно разреженных газов уравнению состояния идеального газа:
| P1V = (m1/μ1)RT; P2V = (m2/μ2)RT; ..., |
где V – объем смеси, T – абсолютная температура, m1, m2, ... – массы различных газов в смеси, μ1, μ2, ...– их молярные массы.
Примером газовой смеси является воздух, состоящий из азота, кислорода, углекислого газа и других газов.
Иллюстрацией закона Дальтона может служить процесс диффузии газа через полупроницаемую перегородку (мембрану). Пусть в начальный момент два разных газа занимают две половины сосуда, разделенные полупроницаемой мембраной. Температуры обоих газов и их начальные давления одинаковы. Мембрана полностью непроницаема для одного из газов и частично прозрачна для другого. В процессе диффузии газа через полупроницаемую перегородку давление в одной половине сосуда возрастает в соответствии с законом Дальтона, а в другой – падает. Это явление носит название осмоса.