Типы изомерии в органической химии. Структурная, пространственная и оптическая изомерии. Хиральность. Комформация и конфигурация.R,S, Z,E – номенкулатуры.
Различают два вида изомерии: структурную и пространственную (стереоизомерию). Структурные изомеры отличаются друг от друга порядком связи атомов в молекуле, стерео-изомеры — расположением атомов в пространстве при одинаковом порядке связей между ними.
Структурная изомерия: изомерию углеродного скелета, изомерию положения, изомерию различных классов органических соединений (межклассовую изомерию).
Структурная изомерия
 +
+
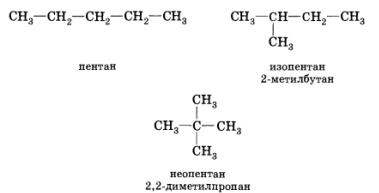
Изомерия углеродного скелета
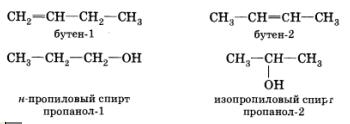 Изомерия положения обусловлена различным положением кратной связи, заместителя, функциональной группы при одинаковом углеродном скелете молекулы:
Изомерия положения обусловлена различным положением кратной связи, заместителя, функциональной группы при одинаковом углеродном скелете молекулы:
Пространственная изомерия
Пространственная изомерия подразделяется на два вида: геометрическую и оптическую.
 Геометрическая изомерия характерна для соединений, содержащих двойные связи, и циклических соединений. Так как свободное вращение атомов вокруг двойной связи или в цикле невозможно, заместители могут располагаться либо по одну сторону плоскости двойной связи или цикла (цис-положение), либо по разные стороны (транс-положение).
Геометрическая изомерия характерна для соединений, содержащих двойные связи, и циклических соединений. Так как свободное вращение атомов вокруг двойной связи или в цикле невозможно, заместители могут располагаться либо по одну сторону плоскости двойной связи или цикла (цис-положение), либо по разные стороны (транс-положение).

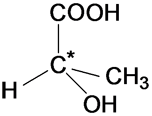 Оптическая изомерия возникает, если молекула несовместима со своим изображением в зеркале. Это возможно, когда у атома углерода в молекуле четыре различных заместителя. Этот атом называют асимметрическим.
Оптическая изомерия возникает, если молекула несовместима со своим изображением в зеркале. Это возможно, когда у атома углерода в молекуле четыре различных заместителя. Этот атом называют асимметрическим.
ХИРАЛЬНОСТЬ, св-во объекта быть несовместимым со своим отображением в идеальном плоском зеркале.
Различные пространственные структуры, возникающие за счет вращения вокруг простых связей без нарушения целостности молекулы (без разрыва химических связей), называют КОНФОРМАЦИЯМИ.
Строение алканов. Sp3- состояние углерода. Характеристика связей С-С и С-Н. Принцип свободного вращения. Конформация. Способы изображения и номенклатуры. Физические свойства алканов.
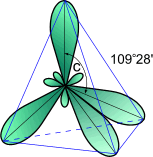 Все атомы углерода в молекулах алканов находятся в состоянии sр3-гибридизации, угол между связями С-C составляет 109°28', поэтому молекулы нормальных алканов с большим числом атомов углерода имеют зигзагообразное строение (зигзаг). Длина связи С-С в предельных углеводородах равна 0,154 нм
Все атомы углерода в молекулах алканов находятся в состоянии sр3-гибридизации, угол между связями С-C составляет 109°28', поэтому молекулы нормальных алканов с большим числом атомов углерода имеют зигзагообразное строение (зигзаг). Длина связи С-С в предельных углеводородах равна 0,154 нм
Связь С-С ковалентная неполярная. Связь С-Н ковалентная слабополярная, тк С и Н близки по электроотрицательности.
Физические свойства
В обычных условиях первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, а начиная с C18 – твердые вещества. Температуры плавления и кипения алканов их плотности увеличиваются с ростом молекулярной массы. Все алканы легче воды, в ней не растворимы, однако растворимы в неполярных растворителях (например, в бензоле) и сами являются хорошими растворителями..
· Температуры плавления и кипения понижаются от менее разветвленных к более разветвленным.
· Газообразные алканы горят бесцветным или бледно-голубым пламенем с выделением большого количества тепла.
Вращение атомов вокруг s-связи не будет приводить к ее разрыву. В результате внутримолекулярного вращения по s-связям С–С молекулы алканов, начиная с этана С2Н6, могут принимать разные геометрические формы.
Различные пространственные формы молекулы, переходящие друг в друга путем вращения вокруг s-связей С–С, называют конформациями илиповоротными изомерами (конформерами).
Поворотные изомеры молекулы представляют собой энергетически неравноценные ее состояния. Их взаимопревращение происходит быстро и постоянно в результате теплового движения. Поэтому поворотные изомеры не удается выделить в индивидуальном виде, но их существование доказано физическими методами.
Общее (родовое) название предельных углеводородов — алканы.
Названия первых четырех членов гомологического ряда метана тривиальные: метан, этан, пропан, бутан. Начиная с пятого названия образованы от греческих числительных с добавлением суффикса –ан
9. Углеводороды. Классификация. Предельные углеводороды ряда метана. Гомологический ряд. Номенклатура. Изомерия. Радикалы. Природные источники. Синтез Фишера-Тропша. Методы получения ( из алкенов, карбоновых кислот, галогенпроизводных, по реакции Вюрца)
| УГЛЕВОДОРОДЫ | |||
| Ациклические Нет замкнутых цепей в углеродном скелете | Циклические В углеродном скелете есть хотя бы один цикл | ||
| Насыщенные Все связи в молекуле одинарные | Ненасыщенные Есть хотя бы одна кратная связь | Алициклические Нет ароматической системы связей | Ароматические Ароматическая система связей присутствует |
Общее (родовое) название предельных углеводородов — алканы.
Названия первых четырех членов гомологического ряда метана тривиальные: метан, этан, пропан, бутан. Начиная с пятого названия образованы от греческих числительных с добавлением суффикса –ан
Свою номенклатуру имеют и радикалы (углеводородные радикалы). Одновалентные радикалы называют алкилами и обозначают буквой R или Alk.
Их общая формула CnH2n+ 1 .
Названия радикалов составляют из названий соответствующих углеводородов заменой суффикса -ан на суффикс -ил (метан — метил, этан — этил, пропан — пропил и т.д.).
Двухвалентные радикалы называют, заменяя суффикс -ан на -илиден (исключение - радикал метилен ==СН2).
Трехвалентные радикалы имеют суффикс -илидин
Изомерия. Для алкановхарактерена структурная изомерия. Если в молекуле алкана содержится более трех углеродных атомов, то порядок их соединения может быть различным. Один из изомеров бутана (н-бутан) содержит неразветвленную углеродную цепь, а другой — изобутан — разветвленную (изостроение).
Важнейшим источником алканов в природе является природный газ, минеральное углеводородное сырье- нефть и сопутствующие ей нефтяные газы.
Получение алканов можно осуществить реакцией Вюрца, заключающейся в действии металлического натрия на моногалогенопроизводные углеводородов.
2CH3–CH2Br(бромистый этил) + 2Na ––> CH3–CH2–CH2–CH3(бутан) + 2NaBr
· Из алкенов
CnH2n + H2 → CnH2n+2
Синтез Фишера — Тропша
nCO + (2n+1)H2 → CnH2n+2 + nH2O
Из таблицы видно, что эти углеводороды отличаются друг от друга количеством групп - СН2-.Такой ряд сходных по строению, обладающих близкими химическими свойствами и отличающихся друг от друга числом данных групп называется гомологическим рядом. А вещества, составляющие его называются гомологами.
| Формула | Название |
| CH4 | метан |
| C2H6 | этан |
| C3H8 | пропан |
| C4H10 | бутан |
| C4H10 | изобутан |
| C5H12 | пентан |
| C5H12 | изопентан |
| C5H12 | неопентан |
| C6H14 | гексан |
| C7H16 | гептан |
| C10H22 | декан |
