Расчёт концентраций ионов в растворах слабых электролитов
Расчёт концентраций ионов в растворах слабых электролитов сводится к решению задачи на химическое равновесие для того случая, когда известна константа равновесия и необходимо найти равновесные концентрации веществ, участвующих в реакции.
Пример 7.3 Рассчитать концентрацию ионов водорода в растворе слабой одноосновной кислоты HA, молярная концентрация которой равна C0 моль/л, и константа диссоциации равна K .
Пусть кислоты продиссоциировало x моль/л, тогда из уравнения процесса диссоциации HA ⇆ H+ + A– следует, что в результате диссоциации образовалось x моль/л ионов H+, x моль/л ионов A–, и к моменту наступления равновесия осталось в непродиссоциированом состоянии (C0-x) моль/л кислоты HA. Таким образом, равновесные концентрации всех частиц будут следующими:
С(H+) = x моль/л; С(A–) = x моль/л; С(HA) = C0-x моль/л.
Далее необходимо подставить выраженные через x «икс» значения равновесных концентраций в выражение константы диссоциации.
(7.4)
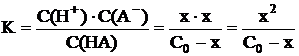
Концентрацию ионов водорода, равную x, можно найти, решая полученное квадратное уравнение относительно x. Расчёт можно значительно упростить, пренебрегая «иксом» в знаменателе полученного выражения. Это можно сделать в том случае, если электролит очень слабый, и вследствие его очень малой диссоциации x стремится к нулю. При решении задач общей и неорганической химии «иксом» можно пренебречь, если выполняется условие K/C0 < 10–2; допускаемая при этом погрешность расчёта не превышает 1-2 % . При решении задач аналитической химии, где требуется большая точность, «иксом» пренебрегают при выполнении условия K/C0 < 10–4 . В случае пренебрежения «иксом» в знаменателе полученного выражения, оно принимает следующий вид:
, (7.5)
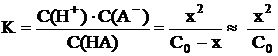
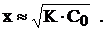 откуда
откуда
Таким образом, концентрацию ионов водорода в растворе слабой одноосновной кислоты можно рассчитать по следующей приближённой формуле:
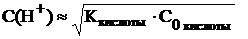
. (7.6)
Концентрацию ионов OH– в растворе слабого основания можно рассчитать по аналогичной формуле
 . (7.7)
. (7.7)
Следует ещё раз подчеркнуть, что формулы 7.6 и 7.7 являются приближёнными, вследствие чего пользоваться ими можно только при выполнении условия K/C < 10–2 . Если это условие не выполняется, нужно решать квадратное уравнение 7.4.
Пример 7.4 Рассчитать концентрации ионов водорода, дигидрофосфат-, гидрофосфат- и фосфат-ионов в 0,1 М растворе фосфорной кислоты. Константы диссоциации фосфорной кислоты: K1 = 7,5·10–3, K2 = 6,3·10–8, K3 = 1,3·10–12.
Строго говоря, общая концентрация ионов водорода в растворе слабой многоосновной кислоты равна сумме концентраций ионов H+, образовавшихся на каждой стадии диссоциации. Например, для фосфорной кислоты
C(H+)общая = C(H+)по 1 стадии + C(H+)по 2 стадии + C(H+)по 3 стадии .
Однако, в связи с тем, что диссоциация слабых электролитов протекает преимущественно по первой стадии, а по второй и последующим стадиям – лишь в незначительной степени, то C(H+)по 2 стадии » 0, C(H+)по 3 стадии » 0. Поэтому, допустимо считать, что что общая концентрация ионов водорода в растворе слабой многоосновной кислоты приблизительно равна концентрации ионов водорода, образовавшихся в результате диссоциации кислоты по первой стадии.
C(H+)общая » C(H+)по 1 стадии
Пусть фосфорной кислоты продиссоциировало по первой стадии x моль/л, тогда из уравнения диссоциации H3PO4 ⇆ H+ + H2PO4– следует, что в результате диссоциации образовалось x моль/л ионов H+ и x моль/л ионов H2PO4– ; к моменту наступления равновесия в недиссоциированном состоянии осталось (0,1-x) моль/л H3PO4. Таким образом, равновесные концентрации всех частиц будут следующими: С(H+) = x моль/л; С(H2PO4–) = x моль/л ; С(H3PO4) = (0,1-x) моль/л.

В данном случае пренебрегать «иксом» в знаменателе полученного уравнения нельзя, поскольку условие K/C < 10–2 не выполняется:
K1/C = 7,5·10–3 / 0,1 = 7,5·10–2 > 10–2 .
Поэтому x находится решением квадратного уравнения.
x2 + 7,5·10–3·x - 7,5·10–4 = 0
Из двух корней этого уравнения (x1 = -3,139·10–3; x2 = 2,389·10–2) физический смысл имеет второй корень. Таким образом, С(H+) = С(H2PO4–) ≈ 0,024 моль/л.
Поскольку гидрофосфат-ионы HPO42– образуются в результате диссоциации кислоты по второй стадии, для расчёта их концентрации необходимо воспользоваться выражением константы для второй стадии диссоциации фосфорной кислоты H2PO4– ⇆ H+ + HPO42–. Здесь важно понимать, что в выражение константы диссоциации любой стадии входят общие концентрации ионов, находящихся в растворе. Общая концентрация ионов водорода была найдена в результате расчёта по первой стадии, причём C(H+) = С(H2PO4–). Поэтому концентрация гидрофосфат-ионов оказывается численно равной второй константе диссоциации.

(моль/л)
Концентрацию фосфат-ионов легко найти, подставляя в выражение третьей константы диссоциации найденные значения С(H+) и С(HPO42–).
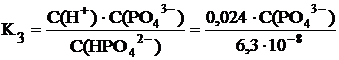
С(PO43–) = 3,43·10–18 моль/л
Закон разбавления Оствальда
Закон разбавления Оствальда показывает связь степени диссоциации слабого электролита с его концентрацией в растворе.
Пусть имеется раствор слабой кислоты HA или слабого основания MeOH с молярной концентрацией C0 . Пусть продиссоциировало х моль/л электролита. Тогда равновесные концентрации ионов каждого типа будут равны x моль/л, а равновесная концентрация непродиссоциировавшей части электролита – (C-x) моль/л.
|
|
| |||||||||
|
| ||||||||||
| |||||||||||
HA ⇆ H+ + A– MeOH ⇆ Me+ + OH–
Так как x – это концентрация продиссоциировавшего электролита, то степень диссоциации α равна: α = x /C0 . Таким образом, x = α·C0.
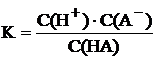 При подстановке х в выражение константы диссоциации для слабой кислоты
При подстановке х в выражение константы диссоциации для слабой кислоты
или слабого основания
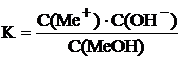 уравнение константы диссоциации принимает следующий вид.
уравнение константы диссоциации принимает следующий вид.
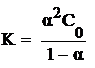
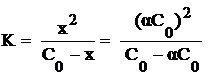
или (7.8)
Выражение 7.8 представляет собой закон разбавления Оствальда.
Для растворов, в которых степень диссоциации очень мала, уравнение закона разбавления Оствальда упрощается. Поскольку в таких растворах α << 1, то величиной α в знаменателе правой части уравнения 7.8 можно пренебречь. В этом случае закон разбавления Оствальда может быть выражен приближёнными формулами.
 (7.9) (7.10)
(7.9) (7.10)
 Полученные уравнения показывают зависимость степени диссоциации слабого электролита от концентрации раствора: степень диссоциации увеличивается с разбавлением раствора (т.е. по мере уменьшения концентрации слабого электролита).
Полученные уравнения показывают зависимость степени диссоциации слабого электролита от концентрации раствора: степень диссоциации увеличивается с разбавлением раствора (т.е. по мере уменьшения концентрации слабого электролита).
Очень важно понимать, что закон разбавления Оствальда применим только для растворов слабых электролитов, не содержащих посторонних веществ, усиливающих или подавляющих диссоциацию слабого электролита. Если к раствору слабой кислоты, например, уксусной CH3COOH добавить её соль, например, ацетат натрия CH3COONa, то в растворе резко увеличится концентрация ацетат-ионов, вследствие полной и необратимой диссоциации ацетата натрия, являющегося сильным электролитом. В соответствии с принципом Ле-Шателье это должно привести к смещению равновесия диссоциации уксусной кислоты CH3COOH ⇆ CH3COO– + H+ влево, вследствие чего концентрация недиссоциированных молекул уксусной кислоты увеличится, а степень диссоциации электролита уменьшится. Сказанное справедливо и для слабых оснований. Если к раствору слабого основания, например, гидроксида аммония NH4OH, добавить соль этого основания, например, хлорид аммония NH4Cl, то в растворе появится большое количество ионов аммония, вследствие полной и необратимой диссоциации соли. Это приведёт к смещению равновесия диссоциации основания NH4OH ⇆ NH4+ + OH– влево и подавлению диссоциации NH4OH. В данном случае было бы грубой ошибкой рассчитывать степень диссоциации слабых электролитов по закону разбавления Оствальда, т.к. при его выводе не предполагалось присутствие в растворе веществ, смещающих равновесие диссоциации слабого электролита. Степень диссоциации слабых кислот и оснований в подобных системах следует рассчитывать по формуле α = x /C0 ,
где x – концентрация продиссоциировавшего электролита;
C0 – молярная концентрация электролита в растворе.
Эта формула является универсальной и может применяться для расчёта степени диссоциации слабого электролита в любом растворе. Поскольку в растворе слабой одноосновной кислоты x = C(H+), а в растворе слабого однокислотного основания x = C(OH–), то степень диссоциации слабых кислот и оснований можно рассчитать по представленным ниже формулам.
αкислоты = C(H+) /C0 кислоты (7.11) αоснования = C(OH–) / C0 основания (7.12)
