Методы познания веществ и химических явлений
АХМЕТОВ М. А.
Пособие предназначено для учителей химии, методистов органов управления образования. Оно содержит тематические и итоговые тесты по химии для 8-9 классов, соответствующие государственному стандарту общего образования по химии за курс основной школы. Каждый тест составлен на основе спецификации, описывающей содержание и уровень трудности каждого задания, приведены ответы. При составлении тестов были учтены современные требования как к тесту в целом, так и тестовому заданию. Тесты позволят оценить качество образовательной подготовки школьников, их готовность к итоговой аттестации. Результаты теста помогут внести необходимые коррективы в учебный процесс.
ОГЛАВЛЕНИЕ
ВВЕДЕНИЕ. 4
СТАНДАРТ ОСНОВНОГО ОБЩЕГО ОБРАЗОВАНИЯ ПО ХИМИИ. 6
I. ПЕРВОНАЧАЛЬНЫЕ ХИМИЧЕСКИЕ ПОНЯТИЯ. 10
II. ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ. 15
III. ПЕРИОДИЧЕСКИЙ ЗАКОН. ХИМИЧЕСКАЯ СВЯЗЬ. 20
IV. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ. 25
V. ХИМИЯ НЕМЕТАЛЛОВ. 30
VI. ХИМИЯ МЕТАЛЛОВ. 35
VII. ПЕРВОНАЧАЛЬНЫЕ ПРЕДСТАВЛЕНИЯ ОБ ОРГАНИЧЕСКИХ ВЕЩЕСТВАХ. 40
VIII. ИТОГОВЫЙ ТЕСТ за курс ХИМИИ ОСНОВНОЙ ШКОЛЫ.. 43
ОТВЕТЫ.. 61
ЛИТЕРАТУРА. 63
ВВЕДЕНИЕ
В течение последнего десятилетия произошло изменение структуры школьного химического образования. Вместо линейной системы преподавания предмета была введена так называемая концентрическая система. Согласно данной системе в курс основной школы были введены начальные сведения об органических веществах. Некоторые наиболее сложные вопросы курса химии, которые ранее включались в требования к уровню подготовки выпускников основной школы, теперь перенесены в старшую школу. Они либо совсем не изучаются в 8-9 классах, либо изучаются только в ознакомительном плане[1]:
| Изучаются в ознакомительном плане | Совсем не изучаются |
| 1.Атомная единица массы 2. Природные смеси: воздух, природные воды 3. Аморфные вещества 4. Типы кристаллических решеток (атомная, молекулярная, ионная, металлическая) 5. Понятие о скорости химической реакции. Катализаторы 6. Сернистая и сероводородные кислоты 7. Амфотерные свойства оксида и гидроксида алюминия 8. Строительные и поделочные материалы (мел, мрамор, известняк, стекло, цемент) 9. Токсичные, горючие и взрывоопасные вещества. 10. Нагревательные устройства, проведение химических реакций при нагревании. | 1. число Авогадро[2] 2. Сила электролита 3. Зависимость скорости химической реакции от различных факторов. 4. Обратимые и необратимые реакции 5. Химическое равновесие и условия его смещения 6.. Химическое производство 7. Минеральные удобрения 8. Понятие о коррозии металлов 9. Сплавы железа: чугун и сталь |
Учителям химии следует учитывать тот факт, что все ранее рекомендованные Министерством образования программы были написаны до появления нового стандарта школьного химического образования и потому не в полной мере ему соответствуют. Такая же ситуация сложилась и с учебниками химии. Учителю химии необходимо установить соответствие между ныне действующим стандартом и программой по химии, на предмет выделения надстандартных элементов содержания. Включение этих элементов в учебный процесс целесообразно в двух случаях:
1. Если на изучение химии за счет школьного компонента выделяется большее количество часов, чем предусмотрено в базисном учебном плане[3].
2. В рамках разноуровневого обучения, в том случае если учащийся полностью освоил содержание стандарта по данной теме.
Учитывая высокую степень технологичности теста, именно данная форма была взята за основу при составлении контрольно-измерительных материалов. В пособии представлены тесты по семи основным темам курса химии (в 2-х вариантах) и итоговый тест (в 4-х вариантах). Темы выделены таким образом, что они соответствуют большей части современных программ по химии:
| 8 класс | 9 класс |
| I. ПЕРВОНАЧАЛЬНЫЕ ХИМИЧЕСКИЕ ПОНЯТИЯ | V. ХИМИЯ НЕМЕТАЛЛОВ |
| II. ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ | VI. ХИМИЯ МЕТАЛЛОВ |
| III. ПЕРИОДИЧЕСКИЙ ЗАКОН. ХИМИЧЕСКАЯ СВЯЗЬ | VII. ПЕРВОНАЧАЛЬНЫЕ ПРЕДСТАВЛЕНИЯ ОБ ОРГАНИЧЕСКИХ ВЕЩЕСТВАХ |
| IV. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ | VIII. ИТОГОВЫЙ ТЕСТ за курс ХИМИИ ОСНОВНОЙ ШКОЛЫ |
Если Ваш тематический план отличается от предложенного, то последовательность контрольных срезов может быть изменена. Тематические тесты рассчитаны на 1 урок (45 минут). Для перевода результатов теста в школьные оценки рекомендуется следующая шкала:
| количество верных ответов | оценка |
| 15-16 | |
| 12-14 | |
| 9-11 | |
| менее 9 |
Итоговый тест рассчитан на 120 минут. Для перевода результатов теста в школьные оценки может быть рекомендована следующая шкала:
| количество верных ответов | оценка |
| 32-36 | |
| 26-31 | |
| 19-26 | |
| менее 19 |
Учащиеся при выполнении теста могут пользоваться периодической таблицей Д. И. Менделеева, таблицей растворимости, рядом напряжения металлов, калькулятором. Для получения надежных результатов следует полностью исключить контакт учащихся друг с другом.
СТАНДАРТ ОСНОВНОГО ОБЩЕГО ОБРАЗОВАНИЯ
ПО ХИМИИ
Изучение химии в основной школе направлено на достижение следующих целей:
· освоение важнейших знаний об основных понятиях и законах химии, химической символике;
· овладение уменияминаблюдать химические явления, проводить химический эксперимент, производить расчеты на основе химических формул веществ и уравнений химических реакций;
· развитиепознавательных интересов и интеллектуальных способностей в процессе проведения химического эксперимента, самостоятельного приобретения знаний в соответствии с возникающими жизненными потребностями;
· воспитание отношения к химии как к одному из фундаментальных компонентов естествознания и элементу общечеловеческой культуры;
· применение полученных знаний и уменийдля безопасного использования веществ и материалов в быту, сельском хозяйстве и на производстве, решения практических задач в повседневной жизни, предупреждения явлений, наносящих вред здоровью человека и окружающей среде.
ОБЯЗАТЕЛЬНЫЙ МИНИМУМ СОДЕРЖАНИЯ
ОСНОВНЫХ ОБРАЗОВАТЕЛЬНЫХ ПРОГРАММ
ВЕЩЕСТВО
Атомы и молекулы. Химический элемент. Язык химии. Знаки химических элементов, химические формулы. Закон постоянства состава.
Относительные атомная и молекулярная массы. Атомная единица массы. Количество вещества, моль. Молярная масса. Молярный объем.
Чистые вещества и смеси веществ. Природные смеси: воздух, природный газ, нефть, природные воды.
Качественный и количественный состав вещества. Простые и сложные вещества. Основные классы неорганических веществ.
Периодический закон и периодическая система химических элементов Д.И. Менделеева. Группы и периоды периодической системы.
Строение атома. Ядро (протоны, нейтроны) и электроны. Изотопы. Строение электронных оболочек атомов первых 20 элементов периодической системы Д.И. Менделеева.
Строение молекул. Химическая связь. Типы химических связей: ковалентная (полярная и неполярная), ионная, металлическая. Понятие о валентности и степени окисления.
Вещества в твердом, жидком и газообразном состоянии. Кристаллические и аморфные вещества. Типы кристаллических решеток (атомная, молекулярная, ионная и металлическая).
ХИМИЧЕСКАЯ РЕАКЦИЯ
Химическая реакция. Условия и признаки химических реакций. Сохранение массы веществ при химических реакциях.
Классификация химических реакций по различным признакам: числу и составу исходных и полученных веществ; изменению степеней окисления химических элементов; поглощению или выделению энергии. Понятие о скорости химических реакций. Катализаторы.
Электролитическая диссоциация веществ в водных растворах. Электролиты и неэлектролиты. Ионы. Катионы и анионы. Электролитическая диссоциация кислот, щелочей и солей. Реакции ионного обмена.
Окислительно-восстановительные реакции. Окислитель и восстановитель.
ЭЛЕМЕНТАРНЫЕ ОСНОВЫ
НЕОРГАНИЧЕСКОЙ ХИМИИ
Свойства простых веществ (металлов и неметаллов), оксидов, оснований, кислот, солей.
Водород. Водородные соединения неметаллов. Кислород. Озон. Вода.
Галогены. Галогеноводородные кислоты и их соли.
Сера. Оксиды серы. Серная, сернистая и сероводородная кислоты и их соли.
Азот. Аммиак. Соли аммония. Оксиды азота. Азотная кислота и ее соли.
Фосфор. Оксид фосфора. Ортофосфорная кислота и ее соли.
Углерод. Алмаз, графит. Угарный и углекислый газы. Угольная кислота и ее соли.
Кремний. Оксид кремния. Кремниевая кислота. Силикаты.
Щелочные и щелочноземельные металлы и их соединения.
Алюминий. Амфотерность оксида и гидроксида.
Железо. Оксиды, гидроксиды и соли железа.
ПЕРВОНАЧАЛЬНЫЕ ПРЕДСТАВЛЕНИЯ ОБ
ОРГАНИЧЕСКИХ ВЕЩЕСТВАХ
Первоначальные сведения о строении органических веществ.
Углеводороды: метан, этан, этилен.
Спирты (метанол, этанол, глицерин) и карбоновые кислоты (уксусная, стеариновая) как представители кислородсодержащих органических соединений.
Биологически важные вещества: жиры, углеводы, белки.
Представления о полимерах на примере полиэтилена.
ХИМИЯ И ЖИЗНЬ
Знать / понимать
· химическую символику: знаки химических элементов, формулы химических веществ и уравнения химических реакций;
· важнейшие химические понятия: химический элемент, атом, молекула, относительные атомная и молекулярная массы, ион, химическая связь, вещество, классификация веществ, моль, молярная масса, молярный объем, химическая реакция, классификация реакций, электролит и неэлектролит, электролитическая диссоциация, окислитель и восстановитель, окисление и восстановление;
· основные законы химии: сохранения массы веществ, постоянства состава, периодический закон;
Уметь
· называть: химические элементы, соединения изученных классов;
· объяснять: физический смысл атомного (порядкового) номера химического элемента, номеров группы и периода, к которым элемент принадлежит в периодической системе Д.И. Менделеева; закономерности изменения свойств элементов в пределах малых периодов и главных подгрупп; сущность реакций ионного обмена;
· характеризовать: химические элементы (от водорода до кальция) на основе их положения в периодической системе Д.И.Менделеева и особенностей строения их атомов; связь между составом, строением и свойствами веществ; химические свойства основных классов неорганических веществ;
· определять: состав веществ по их формулам, принадлежность веществ к определенному классу соединений, типы химических реакций, валентность и степень окисления элемента в соединениях, тип химической связи в соединениях, возможность протекания реакций ионного обмена;
· составлять: формулы неорганических соединений изученных классов; схемы строения атомов первых 20 элементов периодической системы Д.И.Менделеева; уравнения химических реакций;
· обращатьсяс химической посудой и лабораторным оборудованием;
· распознавать опытным путем: кислород, водород, углекислый газ, аммиак; растворы кислот и щелочей, хлорид-, сульфат-, карбонат-ионы;
· вычислять: массовую долю химического элемента по формуле соединения; массовую долю вещества в растворе; количество вещества, объем или массу по количеству вещества, объему или массе реагентов или продуктов реакции;
использовать приобретенные знания и умения в практической деятельности и повседневной жизнидля:
· безопасного обращения с веществами и материалами;
· экологически грамотного поведения в окружающей среде;
· оценки влияния химического загрязнения окружающей среды на организм человека;
· критической оценки информации о веществах, используемых в быту;
· приготовления растворов заданной концентрации.
V. ХИМИЯ НЕМЕТАЛЛОВ
СПЕЦИФИКАЦИЯ ТЕСТА
| № задания | Требование к уровню подготовки выпускников | Виды деятельности | ||
| Воспроизведение знаний | Применение знаний и умений | |||
| В знакомой ситуации | В измененной ситуации | |||
| Водород | + | |||
| 2. | Водородные соединения неметаллов | + | ||
| 3. | Кислород. Озон | + | ||
| 4. | Вода | + | ||
| 5. | Галогены. Галогеноводородные кислоты и их соли | + | ||
| 6. | Сера. Оксиды серы | + | ||
| 7. | Серная кислота и их соли | + | ||
| 8. | Азот. Аммиак | + | ||
| 9. | Соли аммония. Оксиды азота | + | ||
| 10. | Азотная кислота и ее соли. | + | ||
| 11. | Фосфор. Оксид фосфора. | + | ||
| 12. | Ортофосфорная кислота и ее соли. | + | ||
| 13. | Углерод. Алмаз, графит. Угарный газ | + | ||
| Углекислый газ и угольная кислота. | + | |||
| Угольная кислота и ее соли. | + | |||
| 16. | Кремний. Оксид кремния. Кремниевая кислота. | + |
ВАРИАНТ 1
1. Реакция водорода с оксидом меди (II) относится к реакциям
1) соединения 2) замещения 3) обмена 4) разложения
2. Аммиаку соответствует химическая формула
1) NO 2) NH3 3) CH4 4) CO
3. Объем кислорода (при н. у.), необходимый для окисления 6,4 г серы:
1) 11,2 л 2) 5,6 л 3) 2,24 л 4) 4,48 л
4. Фенолфталеин приобретает малиновую окраску в растворе, полученном при взаимодействии
1) хлорида натрия и нитрата серебра 2) гидроксида натрия с соляной кислотой
3) оксида серы (IV) с водой 4) натрия с водой
5. Отбеливает ткани и убивает болезнетворные бактерии
1) жидкий хлор 2) сухой газообразный хлор 3) хлороводород 4) хлор в присутствии воды
6. В 40 г оксида серы (IV) содержится моль кислорода
| 1) 0,5 | 3)1,5 |
| 2) 1 | 4) 2 |
7. При нагревании кристаллического хлорида натрия с концентрированной фосфорной кислотой выделяется газ
1) SO2 2) SO3 3) HCl 4) Cl2
8. 7 г азота при нормальных условиях занимают объем (л)
| 1) 5,6 | 3) 16,8 |
| 2) 11,2 | 4) 22,4 |
9. Взаимодействуют друг с другом при комнатной температуре и обычном давлении
1) аммиак и хлороводород
2) аммиак и кислород
3) азот и водород
4) кислород и азот
10. Белый осадок, не растворимый в соляной кислоте, образуется при взаимодействии
1) Ва(ОН)2 и НNО3
2) CuCl2 и NaOH
3) FеС13 и NaOH
4) СаСl2 и AgNО3
11. От капли лакмуса приобретает красный цвет раствор, который получается при взаимодействии
1) оксида фосфора (V) с водой
2) натрия с водой
3) оксида кальция с водой
4) аммиака с водой
12. Фосфат кальция можно получить реакцией ионного обмена
| 1) кальция с фосфорной кислотой | 3) сульфата кальция с фосфорной кислотой |
| 2) оксида кальция с оксидом фосфора (V) | 4) фосфата натрия с хлоридом кальция |
13. Простые вещества: сажа, озон, графит, кислород, алмаз, красный фосфор. Число химических элементов, входящих в состав этих веществ, равно
| 1) 6 | 2) 3 | 3) 4 | 4) 5 |
14. Превращение СаСО3—> CО2 при 20 °С можно осуществить с помощью
1) гидроксида натрия
2) азотной кислоты
3) кремниевой кислоты
4) нитрата калия
15. Карбонат кальция нельзя получить, если смешать водный раствор
1) хлорида кальция и углекислый газ
2) оксида кальция и карбонат натрия
3) гидроксида кальция и карбонат калия
4) хлорида кальция и карбонат натрия
16. Сокращенное ионное уравнение 2H+ + SiО32- = Н2SiO3 соответствует реакции между
1) SiО2 и NaOH
2) Na2SiO3 и Ca(NO3)2
3) Na2SiО3 и НС1
4) KOH и SiO2
ВАРИАНТ 2
1. В химической реакции водорода с оксидом меди окислителем является
1) водород 2) кислород в оксиде меди 3) медь в оксиде меди 4) вода
2. Электронной формуле m:n:m отвечает строение
1) хлороводорода 2) сероводорода 3) метана 4) оксида серы (IV)
3. Объем кислорода (при н. у.), необходимый для окисления 6,2 г фосфора
1) 11,2 л 2) 5,6 л 3) 2,24 л 4) 4,48 л
4. При полном разложении 72 г воды количество вещества и объем (при н. у.) выделившегося водорода:
1) 4 моль; 89,6л 2) 2 моль; 44,8 л 3) 0,5 моль; 11,2 л 4) 4 моль; 44,8 л
5. Наличие хлороводорода в растворе нельзя определить с помощью
1) метилоранжа 2) лакмуса 3) нитрата бария 4) нитрата серебра
6. Формула соединения серы, в котором массовая доля серы 50%
| 1) SO3 | 3) SO2 |
| 2) Н2SO3 | 4) H2SO4 |
7. Серная кислота может реагировать с каждым веществом ряда
1) СО2, BaCl2, КОН, ZnO
2) ZnO, CaO, NaOH, Р2О5
3) Ва(NО3)2, NaOH, Zn(OH)2, CuO
4) Ва(ОН)2, CuO, HC1, Аl2О3
8. Аммиак можно получить при взаимодействии
1) (NH4)2S04 и Са(ОН)2
2) N2 и О2
3) NH4C1 и AgNО3
4) (NH4)2SО4 и ВаCl2
9. Катионы аммония и нитрат - анионы при диссоциации образует вещество
1) NH4NО3 2) NH4NО2 3) NH4Cl 4) NaNO3
10. Уравнение реакции меди с разбавленной азотной кислотой
1) 3Сu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
2) Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O
3) Cu + 2HNO3 = Cu(NO3)2 + H2
4) реакция невозможна, поскольку в ряду активности металлов медь находится правее водорода.
11. Формула белого фосфора
| 1) Р | 2) Р2 | 3) Р4 | 4) Р8 |
12. Соль, растворимая в растворе соляной кислоты
| 1) фосфат кальция | 2) сульфат бария | 3) хлорид серебра | 4) йодид серебра |
13. Угарным газом называют
1) оксид углерода (IV) 2) оксид серы (II) 3) оксид углерода (II) 4) оксид азота (II)
14. Оксид углерода (IV) взаимодействует с парой веществ:
1) хлороводород и гидроксид калия
2) гидроксид кальция и оксид калия
3) гидроксид натрия и серная кислота
4) азотная кислота и гидроксид бария
15. При прокаливании карбоната магния образуются
1) Mg(HCO3)2 и СO2
2) Mg(OH)2 и СО
3) MgO и СO2
4) MgO, CO2 и Н2O
16. Реакция между растворами Na2SiO3 и НNО3
1) нейтрализации
2) каталитическая
3) окислительно-восстановительная
4) необратимая
VI. ХИМИЯ МЕТАЛЛОВ
СПЕЦИФИКАЦИЯ ТЕСТА
| № задания | Требование к уровню подготовки выпускников | Виды деятельности | ||
| Воспроизведение знаний | Применение знаний и умений | |||
| В знакомой ситуации | В измененной ситуации | |||
| Основные оксиды | + | |||
| 2. | Основания, щелочи | + | ||
| 3. | Основания, щелочи | + | ||
| 4. | Щелочные металлы | + | ||
| 5. | Щелочно-земельные металлы | + | ||
| 6. | Щелочно-земельные металлы | + | ||
| 7. | Соли щелочных металлов | + | ||
| 8. | Соли щелочных металлов | + | ||
| 9. | Соли щелочноземельных металлов | + | ||
| 10. | Соли и гидроксиды щелочноземельных металлов | + | ||
| 11. | Алюминий | + | ||
| 12. | Алюминий | + | ||
| 13. | Железо | + | ||
| Железо | + | |||
| Оксиды железа | + | |||
| 16. | Оксиды железа | + |
ВАРИАНТ 1
1. В ряду веществ, формулы которых К2О, Na2О, CuO, MgO
1) кислотные оксиды
2) амфотерные оксиды
3) основные оксиды
4) кислотные и основные оксиды
2. Основаниями являются:
1) Сu(OH)2, Cu(NO3)2, Fe(OH)2
2) HNO3, NaOH, Fe(OH)3
3) NaOH, NaNO3, LiOH
4) Fe(OH)3 , KOH, Cu(OH)2
3. Используя гидроксид кальция и нитрат аммония, можно получить
1) аммиак, воду и нитрат кальция
2) нитрат кальция, оксид азота (IV), воду
3) воду, хлорид аммония, нитрат кальция
4) нитрат кальция, аммиак, оксид азота (II)
4. Щелочной металл, катионы которого имеют по 18 электронов
1) литий 2) натрий 3) калий 4) рубидий
5. Атомы магния и алюминия имеют
1) одинаковое число протонов в ядрах
2) одинаковое число валентных электронов
3) одинаковую степень окисления в оксидах
4) одинаковое число электронных слоев
6. Сокращенное ионное уравнение H+ + ОН- = Н2O соответствует реакции между
1) NaOH и NH4C1
2) Са(ОН)2 и HC1
3) AgNO3 и HC1
4) Ва(ОН)2 и H2SO4
7. Наиболее ярко выраженная ионная химическая связь образуется в соединении натрия с элементом, заряд атомного ядра которого
1) +14 2) +9 3) +15 4) +1
8. Одновременно в растворе могут быть ионы
1) H+ и ОН- 2) Ag+ и Вг- 3) Na+ и Cl- 4)Ba2+ и S042-
9. В растворе не могут одновременно находиться вещества:
1) К2СО3 и Na2SiO3
2) NaOH и K2SO4
3) СаСl2 и KNO3
4) Na2CO3 и СаСl2
10. Образуется белый осадок при взаимодействии
1) гидроксида натрия и нитрата железа (III)
2) хлорида кальция и карбоната калия
3) карбоната калия и азотной кислоты
4) хлорида меди (II) и гидроксида натрия
11. Высший оксид состава ЭO3 образует химический элемент, имеющий
1) заряд атомного ядра +13
2) пять электронов на внешнем электронном слое
3) заряд атомного ядра+16
4) два электрона на внешнем электронном слое
12. Самым распространенным металлом, входящим в состав земной коры, является
1) железо 2) лантан 3) алюминий 4) натрий
13. Результат взаимодействия хлорида железа (III) и гидроксида калия можно выразить сокращенным ионным уравнением:
1) Fe2О3 + 6H+ = 2Fe3+ + 3Н2О
2) Н+ + ОН- = Н2О
3) Fe3+ + 3ОН- = Fе(ОН)3
4) Ag+ + Сl- = AgCl
14. Железо наиболее интенсивно реагирует с концентрированной кислотой
1) серной 2) соляной 3) азотной 4) угольной
15. В уравнении реакции разложения гидроксида железа (III) коэффициент перед формулой воды равен
1)1 2) 2 3) 3 4) 6
16. Гидроксиду железа (III) соответствует оксид, формула которого
1) Fe2O3 2) FeO 3) Fe3O4 4) смесь Fe2O3 и FeO
ВАРИАНТ 2
1. Оксид, реагирующий с водой при комнатной температуре
1) Na2O 2) MgO 3) Al2O3 4) Fe2O3
2. Необратимая химическая реакция происходит между растворами веществ:
1) КОН и Na2SО4 2) КОН и CuCl2 3) NaCI и Ca(NО3)2 4) CuSО4 и KNО3
3. Превращение Cu(NO3)2 -> Cu(OH)2 можно осуществить с помощью:
1) воды
2) хлорида меди (II)
3) гидроксида железа (III)
4) гидроксида лития
4. Щелочной металл, катионы которого имеют по 10 электронов
1) литий 2) натрий 3) калий 4) рубидий
5. Если заменить цинк на магний в реакции с соляной кислотой, то
1) скорость увеличится
2) скорость уменьшится
3) скорость не изменится
4) реакция прекратится
6. Химическая реакция, которая возможна между гидроксидом кальция и азотной кислотой, выражена сокращенным ионным уравнением:
1) Са2+ + СО32- = СаСО3
2) H+ + ОН- = Н2О
3) H+ + NO3- = HNO3
4) СаСО3 + 2Н+ = Са2+ + Н2О + СО2
7. Смоченный раствором сульфата натрия графитовый стержень внесли в пламя. Цвет пламени стал
1) фиолетовым 2) желтым 3) зеленым 4) красным
8. Ионную кристаллическую решетку имеет
1) оксид фосфора(V)
2) «сухой лед»
3) хлорид натрия
4) сера кристаллическая
9. При взаимодействии нитрата кальция и карбоната натрия получаются
1) СаСО3 и NaNO3
2) NaNO3, СО2 и СаО
3) СаСО3 и HNO3
4) NaNO3 и Са(ОН)2
10. Основания состава Э(ОН)2 образуют химические элементы с атомными номерами в периодической системе
1) 4, 12, 20 2) 11, 12, 13 3) 12, 16, 19 4) 3, 4, 12
11. В алюминиевой посуде нельзя хранить кислую капусту (или другие кислые продукты), потому что
1) алюминий катализирует гниение капусты
2) металл взаимодействует с кислотой
3) происходит взаимодействие алюминия с водой
4) поверхность посуды вследствие действия на нее кислорода воздуха покрывается пленкой оксида алюминия
12. Ошибочная характеристика алюминия
1) алюминий – серебристо-белый металл, обладающий высокой электропроводностью
2) плотность алюминия примерно втрое меньше плотности железа
3) алюминий - достаточно прочный металл
4) алюминий – очень хрупкий металл
13. Химическую реакцию, сущность которой выражена уравнением
Fe2++2OH-=Fe(OH)2, можно осуществить с помощью…
1) гидроксида калия и фосфата железа (II)
2) нитрата железа (II) и гидроксида меди (II)
3) нитрата железа (III) и гидроксида натрия
4) хлорида железа (II) и гидроксида бария
14. Хлорид железа (II) можно получить при взаимодействии
1) соляной кислоты и железа
2) хлора и железа
3) растворов хлорида меди (II) и сульфата железа (II)
4) железа и хлорида магния (раствор)
15. Железная окалина – это
1) FeO 2) Fe2O3 3) Fe3O4 4) смесь Fe2O3 и FeO
16. Продуктом реакции оксида железа (II) с соляной кислотой является
1) только FeCl3 2) только FeCl2 3) реакция не идет 4) смесь FeCl2 и FeCl3
СПЕЦИФИКАЦИЯ ТЕСТА
| № задания | Требование к уровню подготовки выпускников | Виды деятельности | ||
| Воспроизведение знаний | Применение знаний и умений | |||
| В знакомой ситуации | В измененной ситуации | |||
| Первоначальные сведения о строении органических веществ | + | |||
| 2. | Первоначальные сведения о строении органических веществ | + | ||
| 3. | Метан | + | ||
| 4. | Этан | + | ||
| 5. | Этилен | + | ||
| 6. | Метанол | + | ||
| 7. | Этанол | + | ||
| 8. | Глицерин | + | ||
| 9. | Уксусная кислота | + | ||
| 10. | Стеариновая кислота | + | ||
| 11. | Жиры | + | ||
| 12. | Углеводы | + | ||
| 13. | Белки | + | ||
| Массовая доля элемента в веществе | + | |||
| Массовая доля вещества в растворе | + | |||
| 16. | Простейшие расчеты по химической реакции | + |
ВАРИАНТ 1
1. Формула органического вещества:
1) СО2 2) СН4 3) Н2СО3 4) СS2
2. Формула углеводорода
1) Н2СО3 2) СН3ОН 3) С2Н4 4) (С6Н10О5)n
3. Структурная формула метана
1) СН4 2) СН3-Н 3) Н-СН2-Н 4) 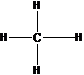
4. Степень окисления атомов углерода в молекуле этана равна
1) -4 2) -3 3) +4 4) +3
5. Молекула, содержащая двойную углерод-углеродную связь
1) СН4 2)С2Н4 3) С2Н6 4) СН3СООН
6. Формула вещества, попадание которого в организм даже в незначительных количествах очень опасно
1) СН3ОН 2) СН3СООН 3) Н2СО3 3) С17Н35ООН
7. Формула вещества, которое используют для хранения биологических препаратов
1) С2Н4 2) СН3СООН 3) СН3ОН 4)С2Н5ОН
8. Вещество, которое представляет собой вязкую сладковатую жидкость
1) СН3СООН 2) СН3ОН 3) С17Н35СООН 4) СН2ОН-СНОН-СН2ОН
9. Вещество, которое широко применяют как пищевую добавку
1) СН3ОН 2) С2Н4 3) СН3СООН 4) С17Н35СООН
10. Для получения мыла может быть использовано вещество, формула которого
1) С17Н35СООН 2) СН3ОН 3) С2Н4 4) С2Н5ОН
11. Наиболее калорийный компонент пищи
1) жиры 2) белки 3) углеводы 4) витамины
12. Вещество, которое не содержит азот
1) аммиак 2) целлюлоза 3) белок 4) нитрат натрия
13. Вещество, нагревание которого может привести к необратимой денатурации
1) белки 2) жиры 3) углеводы 4) углеводороды
14. Вещество, массовая доля водорода в котором наибольшая
1) СН4 2) С2Н4 3) С2Н6 3) СН3ОН
15. 15 г крахмала при нагревании растворили в 285 г воды. Массовая доля крахмала в полученном растворе составит (%)…
16. Объем кислорода, затраченный на сжигание 5,6 л этана, составит (л) …. (ответ округлите до целых)
ВАРИАНТ 2
1. Формула неорганического вещества
1) СН3ОН 2) СН4 3) Н2СО3 4) СН3СООН
2. Формула кислоты
1) СН3ОН 2) С2Н5ОН 3) СН4 4) СН3СООН
3. Метан - главный составной компонент
1) нефти 2) природного газа 3) минеральной воды 4) бензина
4. Валентность атомов углерода в молекуле этана равна
1) I 2) II 3) III 4) IV
5. Какая из приведенных ниже молекул содержит 6 ковалентных связей?
1) СН4 2) С2Н4 3) С2Н6 4) СН3ОН
6. Вещество, которое при комнатной температуре и обычном давлении является жидкостью
1) СН4 2) С2Н4 3) СН3ОН 4) С17Н35СООН
7. Вещество, которое НЕ диссоциирует в водных растворах
1) СН3СООН 2) Н2СО3 3) NaCl 4) C2H5OH
8. Вещество, которое может быть получено при гидролизе жира
1) уксусная кислота 2) метанол 3) этилен 4) глицерин
9. Вещество, которое реагирует с гидроксидом натрия
1) С2Н4 2) С2Н5ОН 3) СН3СООН 4) СН3ОН
10. Вещество, натриевые соли которого – твердые вещества, а калиевые – жидкие
1) СН3СООН 2) Н2СО3 3) С17Н35СООН 4) Н2SO4
11. Вещества, в результате реакции которых с гидроксидом натрия образуется мыло
1) белки 2) жиры 3) углеводы 4) углеводороды
12. Вещество, которое не усваивается в организме человека
1) крахмал 2) целлюлоза 3) жиры 4) белки
13. Вещество, структурными фрагментами которого являются аминокислоты
1) белки 2) жиры 3) углеводы 4) углеводороды
14. Вещество, массовая доля углерода в котором наибольшая
1) СН4 2) С2Н4 3) С2Н6 3) СН3ОН
15. 2 г белка альбумина растворили в 198 г воды. Массовая доля альбумина в полученном растворе (%) составит …
16. В результате сжигания этилена образовалось 11,2 л углекислого газа. Объем затраченного кислорода составит (л) …(ответ округлите до целых)
ОТВЕТЫ
ОТВЕТЫ НА ТЕМАТИЧЕСКИЕ ТЕСТЫ
| № темы | I | II | III | IV | V | VI | VII | |||||||
| № вар. № зад | ||||||||||||||
| 1. | ||||||||||||||
| 2. | ||||||||||||||
| 3. | ||||||||||||||
| 4. | ||||||||||||||
| 5. | ||||||||||||||
| 6. | ||||||||||||||
| 7. | ||||||||||||||
| 8. | ||||||||||||||
| 9. | ||||||||||||||
| 10. | ||||||||||||||
| 11. | ||||||||||||||
| 12. | ||||||||||||||
| 13. | ||||||||||||||
| 14. | ||||||||||||||
| 15. | ||||||||||||||
| 16. |
ОТВЕТЫ НА ИТОГОВЫЕ ТЕСТЫ
| ВАРИАНТ | I | II | III | IV |
| № вопроса | ||||
| < |
