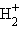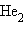Энергия, длина и порядок связи в молекулах элементов I периода
|
Чем выше порядок связи, тем, при прочих равных условиях, прочнее данная молекула, что подтверждается экспериментальными данными. Наличие на МО хотя бы одного неспаренного электрона придает частице парамагнитные свойства и заставляет ее втягиваться в магнитное поле. Если все электроны спарены, то частица обладает диамагнитными свойствами и магнитным полем выталкивается.
МЕТАЛЛИЧЕСКАЯ СВЯЗЬ
Атомы металлов отличаются от атомов других элементов тем, что имеют малые энергии ионизации и сравнительно слабо удерживают свои внешние электроны. Поэтому в кристаллической решетке металла большое количество электронов покидает свои атомы, превращая их в положительно заряженные ионы. «Обобществленные» электроны передвигаются в междоузлиях кристаллической решетки и за счет электростатических сил «цементируют» ионы металла. Такая связь называется металлической и существует не только в твердых кристаллах металлов, но и в расплавах и в аморфном состоянии.
Единая система электронов в металлических веществах называется «электронным газом». Металл можно представить в виде остова из положительных ионов, погруженного в электронный газ, который компенсирует силы взаимного отталкивания положительных ионов. В свою очередь, “электронный газ” может свободно двигаться через решетку, состоящую из ионов металла обеспечивая его высокую электропроводность, теплопроводность и ковкость . В кристаллах металлов атомы ионизированы не полностью, и часть валентных электронов остается связанной. В результате возможно появление частично ковалентных связей между соседними атомами. Вклады ионной и ковалентной составляющей обнаружены во многих металлах. Металлическая связь имеет признаки, характерные как для ковалентной, так и для ионной связи.

Рис. 4.9. Схематическое строение элементарной решетки металла
Электропроводность металлов уменьшается с ростом температуры. Это объясняется тем, что электроны в металле беспорядочно движутся, переходя от одного атома к другому. А положительно заряженные ионы лишь слегка колеблются около своего положения в кристаллической решетке. При нагревании металла колебания катионов усиливаются и электронам становится труднее продвигаться между ними, поэтому электрическое сопротивление металла увеличивается.
Наличие свободных электронов обусловливает высокую теплопроводность металлов и характерный металлический блеск. Их высокая пластичность и ковкость связаны с возможностью взаимного смещения катионов в металлической кристаллической решетке без разрыва химической связи.
Описываемая картина электростатического связывания ионов металла в решетке с помощью «электронного газа» слишком упрощена. В пользу этого свидетельствует следующее. Если бы ионы металлов были связаны только
делокализованными электронами, то все металлические системы были бы похожи: чем больше свободных электронов и меньше атомный радиус металла, тем в большей степени за счет электростатического притяжения фиксировались бы ионы металла в узлах решетки и тем прочнее должен бы быть металл. Но таких простых корреляций не наблюдается. Например, щелочные металлы легко теряют электроны, имеют высокую электропроводность, но они очень мягкие. Медь, серебро и золото также хорошо проводят электрический ток, но они на порядок тверже. Так, в гранецентрированной кубической решетке кристалла меди каждый атом окружен 12 другими атомами. Медь достаточно твердый металл, имеет высокую температуру плавления Тпл = 1100 оС и плотность 8,9 г/см3.
В решетку типа «меди» кристаллизуются такие прочные и твердые металлы, как: γ-Fe, Ni, Rh, Pd, Ir, Pt, Аи. Однако такие металлы, как Мg, А1 и Рb, тоже имеют гранецентрированную кубическую решетку, но их, в отличие от меди, можно резать ножом, и они сильно отличаются по плотности и температурам плавления, например: Мg (ρ =1,74 г/см3, Тпл = 700 оС); Рb (ρ =11,34 г/см3 , Тпл = 327 оС).
Таким образом, количество свободных электронов и тип кристаллической решетки не являются определяющими при формировании механических и физических свойств металлов.
Для объяснения причин образования связей в металлах было предложено несколько теорий (теория резонансной связи Полинга, зонная теория, метод молекулярных орбиталей), каждая из которых внесла свой вклад в понимание вопроса и которые в той или иной мере дополняют друг друга.