Атомные и массовые кларки элементов
| Легкие элементы | Тяжелые элементы | ||||
| Элемент | Массовый кларк | Атомный кларк | Элемент | Массовый кларк | Атомный кларк |
| O | U | 2,5·10–4 | 2·10–5 | ||
| Li | 3,2·10–3 | 1,9·10–2 | Au | 4,3·10–7 | 5·10–8 |
| Be | 3,8·10–4 | 1,2·10–3 | Ra | 2·10–10 | 9·10–12 |
У легких элементов количество атомов большее при малой массе, у тяжелых – большие массы при малом количестве атомов. Близкие по химическим свойствам элементы резко различаются по кларкам: Na –2,50 %; Rb – 1,5 ·10–2; Li – 3,2 ·10–3; Cs – 3,7 ·10–4 %. Разные по свойствам химические элементы имеют близкие кларки: Mn – 0,1 и Р – 0,093; Rb – 1,5 ·10–2 и Cl – 1,7 ·10–2. В земной коре преобладают легкие элементы до железа включительно. Доминируют элементы с четными номерами по атомной массе (86,43 %) как наиболее устойчивые, и очень мало их с нечетными номерами (13,53 %). Особенно большие кларки имеют те элементы, атомная масса которых делится на четыре, например, O, Mg, S, Ca и т. д. (рис. 6).
Среди атомов одного и того же элемента преобладают изотопы с массовым числом, кратным четырем, например: 16О – 99,76 %; 17О – 0,04; 18О – 0,2; 32S – 95,01; 33S – 0,75; 34S – 4,22; 36S – 0,02 %. Элементы с четными порядковыми номерами имеют большее число изотопов, чем с нечетными: № 50 Sn – 10 изотопов; № 9 F – 1 изотоп. В зависимости от генезиса элемента соотношение между изотопами в природе будет разным, а атомная масса отличаться, как индиеатор происхождения пород. Это используется в геологии, например: атомная масса Pb 207,21, в урановых рудах – 206,1, в ториевых – 207,97. При этом химические свойства всех видов свинца одинаковые. Химический элемент устанавливают не по массе изотопа, а по совокупности атомов с одинаковым положительным зарядом ядра. Среди четных элементов, начиная с № 2 – Не, наибольшим кларком обладает каждый шестой: № 8 – О; № 14 – Si; № 20 – Ca; № 26 – Fe; № 32 – Ge; № 38 – Sr и т.д. Аналогичное правило среди нечетных элементов, начиная с № 1 – Н: № 7 – N; № 13 – Al; № 19 – K; № 25 – Mg; № 31 – Ga; № 37 – Rb и т. д.
Редкие элементы мигрируют интенсивнее, чем близкие им по химическим свойствам более распространенные. Поэтому редкие анионы (CrO42–, SeO42–) соединяются с распространенными катионами (Ca, Mg, Fe) и наоборот. «Химическое» поведние элемента отличается от «геохимического». Например, S и Se сходны по химическим свойствам, а в геохимии отличаются: S – ведущий элемент многих процессов, образует руды, сульфиды, другие минеральные формы, для Se это нехарактерно.
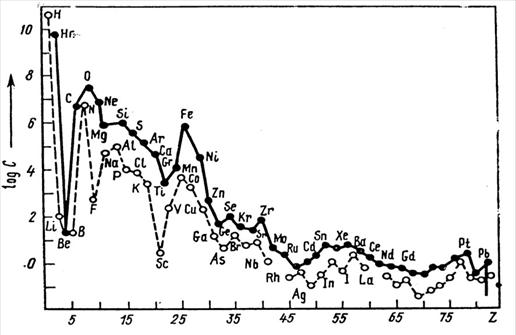
Рис. 6. Относительная атомная распространенность химических элементов в Солнечной системе в зависимости от порядкового номера Z (по А. Аллеру и Д. Россу). Черными кружками обозначены четные номера, светлыми – нечетные
Ведущие элементы определяют геохимические особенности системы и выступают в роли типоморфных элементов или геохимических диктаторов. Примером может служить водород. При высоком его содержании в растворе среда имеет кислую реакцию, которая разрушает минеральные соединения и переводит их в миграционную форму. Кларк влияет на способность элементов образовывать минералы. Число минеральных видов элемента уменьшается с уменьшением его кларка. Например, при величине кларка от 1 до 10 % элемент может образовывать до 239 соединений, при кларке 10–5–10–6 % – всего до 23 минеральных видов. С уменьшением кларков отсутствуют условия для концентрации элементов, труднее достигаются произведение растворимости и выпадение самостоятельной фазы из расплава.
Способность элементов к минералообразованию (М) определяются отношением числа минералов (n) данного элемента к его кларку (К) в земной коре (табл. 6):
М = n / К.
По Е. М. Квятковскому, элементы с большой способностью к минералообразованию называются минералофильными (Si, C, Fe, Bi, Te, Se, U, S), с малой – минералофобными (Mg, Ba, Ga, Rb, Sr, In, Tl, TR).
Таблица 6
Минералообразование элементов (по А.С. Поваренных, 1977)
| Элемент | Кларк (К) | Число минералов (n) | Способность к минералообразованию (М) | ||
| в земной коре | в гипергенных условиях | в земной коре | в гипергенных условиях | ||
| Cr | 8,3 ·10–3 | 2 ·103 | 7 ·102 | ||
| Zn | 8,3 ·10–3 | 8 ·103 | 3,5 ·102 | ||
| V | 9 ·10–3 | 6,8 ·103 | 1,1 ·103 | ||
| Ni | 5,8 ·10–3 | 9,1 ·103 | 7 ·103 |
На образование минералов влияет изоморфизм. Ионные радиусы Na и Cu почти одинаковые, но у них большое различие по величине ЭО: Na+ (ro = 95 пм, ЭО = 0,9), Cu+ (ro = 96 пм, ЭО = 1,9), т. е. разница между элементами по ЭО составляет 1,0. Однако пределы взаимной смесимости резко возрастают, если повышается температура и давление, что соответствует гипогенным условиям. Часть элементов входит в кристаллы распространенных «идеальных изоморфных партнеров»: Rb→K; Hf→Zn, Re→Mo. Почти 1/3 всех стабильных элементов либо не образуют собственных минералов, либо образуют очень редкие минералы в специфических условиях (высокое давление, температура и др.): Ge, Ga, Sc, Ta, Nb, Cd, In, Tl, Y, платиноиды, редкие земли, т. е. чем тяжелее элемент, тем меньше его минеральных видов. Некоторые космические системы имеют близкие спектры по атомным кларкам (рис. 7). У каменных метеоритов и Солнца кларки по большинству элементов сходны, за исключением резких различий по N, In, Re, B, C. Атомные кларки кислых пород Земли представлены в виде плавной ниспадающей кривой от водорода до палладия. Во всех трех геохимических системах атомные кларки совпадают по Si, Ti, отчасти V.

Рис. 7. Атомные кларки кислых пород (1) каменных метеоритов (2) и Солнца (3).
Содержание Si в каждой системе принято равным 106
6. ВНЕШНИЕ ФАКТОРЫ МИГРАЦИИ И РОЛЬ
ГЕОХИМИЧЕСКИХ ПРОЦЕССОВ В МИГРАЦИИ ЭЛЕМЕНТОВ
В каждой геосфере Земли создаются специфические внешние факторы миграции в зависимости от изменения соотношений температуры, давления и концентрации раствора. Эти параметры обусловливают специфику термодинамики системы, которая, в свою очередь, создает условия для формирования тех или иных геохимических процессов. Рассмотрим особенности формирования среды, в которой постоянно протекают миграция, концентрация и рассеивание элементов.
Внешние факторы миграции
Ведущими факторами природной среды являются температура, давление, концентрация раствора, в гипергенной зоне дополнительно влияет тип климата. В зависимости от соотношения факторов изменяются условия от активной миграции элементов в жарком гумидном климате до их концентрации в аридном климате. В гипогенных условиях активная миграция возможна при высоком давлении и температуре, а кристаллизация – при понижении этих параметров. Таким образом, воздействие внешних факторов следует рассматривать самостоятельно в двух сферах: гипергенной и гипогенной.
Гипергенная зона является главным местом действия солнечной радиации. Под ее влиянием прямо или косвенно протекают все гипергенные процессы и связанная с ними миграция элементов. Потребление энергии и ее расход изменяются в зависимости от природной зоны. На ежегодную продукцию растительной массы затраты энергии колеблются от 2,5 кал/см2 в год в тундре до 2000 кал/см2 в год во влажнотропических лесах (для лесов умеренных широт 100–400 кал/см2 в год). На разрушение минералов и освобождение элементов (минеральное преобразование) затрачивается 0,2–0,5 кал/см2 в год в тундре и пустыне и 10–15 кал/см2 в год во влажных тропиках.
Скорость геохимических процессов определяется динамикой температуры. В теплый сезон контрасты температур колеблются от 5–6 °С до 40–50 °С. Повышение температуры активизирует процессы и миграцию. В тундре из-за низких температур геохимические процессы и миграция замедлены, во влажных тропических лесах высокая температура и влажность повышают скорость процессов и миграцию в 9,5 раза. Использование энергии на процессы во влажных тропических лесах в 30–35 раз выше по сравнению с тундрой.
Давление как фактор миграции элементов в зоне гипергенеза имеет меньшее значение, чем температура. В пределах вертикального профиля атмосферное давление составляет 1 атм и изменяется не более чем ± 3 %. Такое колебание давления активизирует лишь растворение газов в воде и косвенно влияет на гидролиз минералов.
Различное соотношение температур и увлажнения приводит к формированию различных типов климата. Среди них наиболее контрастные аридный и гумидный типы. В аридном климате при выпотном водном режиме создаются условия для активизации галогенеза, повышенной концентрации растворов, прежде всего, галогенов, щелочных и щелочноземельных металлов (Na, K, Rb, Cs, Ca, Mg, Ba, Cl, Br, I и др.). Гумидный климат создает промывной тип водного режима, который способствует выносу всех легкорастворимых и концентрации труднорастворимых соединений Fe, Al, Ti, Zr и др. Концентрация растворов минимальная. Моря и океаны отличаются повышенной концентрацией растворов, из которых осаждаются тяжелые элементы.
Гипогенная зона характеризуется высокими и сверхвысокими температурами, давлением и концентрацией химических элементов, что приводит к метаморфизации и магматизации пород, насыщению водных гидротермальных растворов. Во внутренних сферах Земли миграция элементов ограничена. В магме они распределяются более или менее равномерно и дифференцируются под действием гравитации: более легкие оказываются в верхней зоне, а тяжелые – в нижней. Снижение ведущих параметров гипогенной зоны приводит к трансформации фазы в ходе кристаллизации и последовательности образования минеральных видов с включением изоморфных форм более редких элементов. В ходе кристаллизации и других гипогенных процессов вблизи поверхности Земли, при излиянии магмы или извержении вулканов, происходит равномерное или концентрированное распределение элементов на разных глубинах в виде месторождений.
Большинство освоенных месторождений железных руд по генезису обязано формированию под влиянием гипергенных процессов настоящего или геологического времени.
