Вычислить рН 0,05 М водного раствора хлорноватистой кислоты (HOCl).
Дано: c  = 0,05 М = 0,05 М | Решение HOCl <=> H+ + OCl- HOCl – слабый электролит. рН = –lg[H+]; [H+] = cНOСl·α·n  , , |
| pH – ? |
n  – число Н+ образовавшихся при диссоциации одной молекулы HOCl, n
– число Н+ образовавшихся при диссоциации одной молекулы HOCl, n  = 1.
= 1.
 ;
;
КHOCl – константа диссоциации HOCl:
К  = 5,0·10-8 (таблица),
= 5,0·10-8 (таблица),
тогда

c  = 5·10-2 · 10-3 · 1 = 5,0 · 10-5 моль/л,
= 5·10-2 · 10-3 · 1 = 5,0 · 10-5 моль/л,
тогда рН = – lg5,0·10-5 = (-lg 5) + (-lg10-5) = – 0,7 + 5 = 4,3.
Ответ: рН 0,05 М HOCl равно 4,3.
3. Определить произведение растворимости MgF2, если его растворимость в воде при 25 ºС равна 1,17·10-3 моль/л.
Дано: c  = 1,17·10-3 моль/л = 1,17·10-3 моль/л | Решение Равновесие между осадком малорастворимого электролита и насыщенным раствором над ним выражается уравнением |
ПР  – ? – ? |
MgF2(к) <=> Mg2+ (р) + 2F-(р),
ПР  = [Mg2+ ]·[F-]2,
= [Mg2+ ]·[F-]2,
[Mg2+ ] = c  ·α·n
·α·n  , [F-] = c
, [F-] = c  ·α·n
·α·n  .
.
MgF2 – сильный электролит, α = 1;
n  = 1, n
= 1, n  = 2 (из приведенного уравнения)
= 2 (из приведенного уравнения)
[Mg2+ ] = 1,17·10-3·1·1 = 1,17·10-3 моль/л;
[F-] = 1,17·10-3·1·2 = 2,34·10-3 моль/л.
Тогда ПР  = 1,17·10-3·(2,34 · 10-3)2 = 6,41·10-9.
= 1,17·10-3·(2,34 · 10-3)2 = 6,41·10-9.
Ответ: ПР  = 6,41·10-9.
= 6,41·10-9.
УРОВЕНЬ C
1. Вычислить активность ионов в растворе, содержащем
0,01 моль/л нитрата кальция и 0,1 моль/л хлорида кальция.
Дано: c  = 0,01 моль/л c = 0,01 моль/л c  = 0,2 моль/л = 0,2 моль/л | Решение Активность ионов в растворе сильных электролитов определяется по формуле аион = ƒСиона. Процессы диссоциации Сa(NO3)2 и CaCl2 протекают по следующим уравнениям: |
а  – ? а – ? а  – ? а – ? а  – ? – ? |
Сa(NO3)2 = Са2+ + 2NO 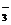 ; (7.1)
; (7.1)
CaCl2 = Ca2+ + 2Cl- . (7.2)
Концентрация ионов определяется по формуле
cион = cв·α·nион ,
тогда
n  = 1 (7.1); n
= 1 (7.1); n  = 1 (7.2);
= 1 (7.2);
n  = 2 (7.1) nCl- = 2 (7.2); α = 1;
= 2 (7.1) nCl- = 2 (7.2); α = 1;
c  = c
= c  ·α·n
·α·n  + c
+ c  α·n
α·n  =
=
= 0,01·1·1 + 0,1·1·1 = 0,11 моль/л.
с  = с
= с  ·α·n
·α·n  = 0,01·1·2 = 0,02 моль/л, см. (7.1)
= 0,01·1·2 = 0,02 моль/л, см. (7.1)
с  = с
= с  ·α·n
·α·n  = 0,1·1·2 = 0,2 моль/л, см. (7.2)
= 0,1·1·2 = 0,2 моль/л, см. (7.2)
Ионная сила раствора
I = 0,5(с  · Z
· Z  + с
+ с  · Z
· Z  + с
+ с  · Z
· Z  ).
).
I = 0,5(0,11·22 + 0,02·(–1)2 + 0,2·(–1)2) = 0,33 ≈ 0,3.
Коэффициент активности ионов определяем из таблицы:
ƒ 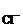 = ƒ
= ƒ  = 0,81. ƒ
= 0,81. ƒ  = 0,42.
= 0,42.
Тогда активность ионов
а  = 0,81 · 0,2 = 0,162 моль/л;
= 0,81 · 0,2 = 0,162 моль/л;
а  = 0,81 · 0,02 = 0,0162 моль/л;
= 0,81 · 0,02 = 0,0162 моль/л;
а  - = 0,42 · 0,11 = 0,0462 моль/л.
- = 0,42 · 0,11 = 0,0462 моль/л.
Ответ: а  = 0,162 моль/л, а
= 0,162 моль/л, а  = 0,0162 моль/л,
= 0,0162 моль/л,
а  = 0,0462 моль/л.
= 0,0462 моль/л.
2. Определить, образуется ли осадок, если смешали 100 см  0,01 М водного раствора хлорида кальция и 200 см
0,01 М водного раствора хлорида кальция и 200 см  0,02 М водного раствора карбоната натрия.
0,02 М водного раствора карбоната натрия.
Дано: с  = 0,01 M с = 0,01 M с  = 0,02 M V = 0,02 M V  = 100 cм = 100 cм  V V  =200 cм =200 cм  | Решение При смешении растворов протекает следующая реакция: CaCl  + Na + Na  CO CO  = = CaCO = = CaCO  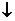 + NaCl. Осадок CaCO + NaCl. Осадок CaCO  образуется только в случае, если образуется только в случае, если |
| Образуется ли осадок? |
с  ·с
·с  > ПР
> ПР  = 5·10
= 5·10  (таблица).
(таблица).
Поскольку смешали 100 cм  раствора CaCl
раствора CaCl 
 и 200 cм
и 200 cм  Na
Na  CO
CO  , то объем раствора после смешения составляет 300 cм
, то объем раствора после смешения составляет 300 cм  . Тогда после смешения объем раствора CaCl
. Тогда после смешения объем раствора CaCl 
 от общего объема смеси составит 1/3, а объем
от общего объема смеси составит 1/3, а объем  раствора Na2CO
раствора Na2CO  после смешения составит 2/3 от общего объема смеси. После смешения концентрации ионов Ca2+ и CO
после смешения составит 2/3 от общего объема смеси. После смешения концентрации ионов Ca2+ и CO  2- будут:
2- будут:
с  =
=  с
с  ·
·  ·n
·n  ; с
; с  =
=  с
с  ·
·  ·n
·n  .
.
CaCl  и Na2CO
и Na2CO  – сильные электролиты,
– сильные электролиты,  = 1.
= 1.
Процессы диссоциации CaCl  и Na
и Na  CO
CO  протекают по следующим уравнениям :
протекают по следующим уравнениям :
CaCl  = Ca
= Ca  + 2Cl
+ 2Cl 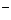
Na  CO
CO  = 2Na
= 2Na  + CO
+ CO  , тогда n
, тогда n  = 1 и n
= 1 и n  = 1.
= 1.
с  =
=  0,01·1·1 = 3,3·10
0,01·1·1 = 3,3·10  моль/л;
моль/л;
с  =
=  0,02·1·1 = 1,3·10
0,02·1·1 = 1,3·10 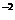 моль/л;
моль/л;
с  ·с
·с  = 3,3·10
= 3,3·10  ·1,3·10
·1,3·10 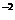 = 4,29·10
= 4,29·10 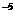 .
.
Так как 4,29·10-5 > 5·10-9 (ПР  ), то осадок CaCO
), то осадок CaCO  образуется.
образуется.
Ответ: осадок CaCO  образуется.
образуется.
3. Вычислить рН 0,01 M водного раствора HNO2, содержащего, кроме того, 0,02 моль/л KNO2.
Дано: с  = 0,01 M с = 0,01 M с  = 0,02 M = 0,02 M | Решение рН = –lg с  , HNO2 <=> H+ + NO , HNO2 <=> H+ + NO  , KNO2 = K+ + NO , KNO2 = K+ + NO  , , |
| рН – ? |
 .
.
Прибавление KNO2 к раствору HNO2 смещает равновесие диссоциации HNO2 влево за счет возрастания концентрации NO2-. В результате в системе устанавливается равновесие при новых концентрациях Н+ и NO  , но значение константы диссоциации HNO2 остается прежним.
, но значение константы диссоциации HNO2 остается прежним.
Тогда обозначим равновесную концентрацию ионов водорода [Н+] в новых условиях через х:
[H+] = х моль/л.
Общая равновесная концентрация [NO  ] равна сумме концентраций NO
] равна сумме концентраций NO  , образовавшихся при диссоциации HNO2 и диссоциации KNO2:
, образовавшихся при диссоциации HNO2 и диссоциации KNO2:
[NO  ] = с
] = с  + с
+ с 
из HNO2 из KNO2
Концентрация NO  , образовавшихся при диссоциации HNO2, равна х моль/л, так как при диссоциации 1 моль HNO2 образуется 1 ион Н+ и 1 ион NO
, образовавшихся при диссоциации HNO2, равна х моль/л, так как при диссоциации 1 моль HNO2 образуется 1 ион Н+ и 1 ион NO  .
.
Концентрация NO  , образовавшихся при диссоциации КNO2:
, образовавшихся при диссоциации КNO2:
с  = с
= с  ·α·n
·α·n  = 0,2·1·1 = 0,2 моль/л.
= 0,2·1·1 = 0,2 моль/л.
из КNO2
КNO2 – сильный электролит, α = 1, n  = 1,
= 1,
тогда [NO  ] = х + с
] = х + с  = (х + 0,02), моль/л;
= (х + 0,02), моль/л;
[HNO2] = (с  – х) = (0,01 – х), моль/л.
– х) = (0,01 – х), моль/л.
 .
.
К  = 4·10-4, (таблица)
= 4·10-4, (таблица)
тогда
 ,
,
так как, х << 0,01 моль/л, то значением х, ввиду его малого значения, в выражениях (х + 0,02) и (0,01 – х) можно пренебречь и данное выражение записать в виде:
 ;
;
откуда х = 2·10-4 моль/л.
[H+] = 2·10-4 моль/л
рН = – lg(2·10-4)= (–lg2) + (–lg10-4) = –0,3 + 4 = 3,7.
Ответ: рН = 3,7.
8. ГИДРОЛИЗ СОЛЕЙ
УРОВЕНЬ A
1. Какие из перечисленных солей подвергаются гидролизу: NH4NO2, Na2CO3, Al2(SO4)3, NaNO3?
Ответ: любую соль можно представить как продукт взаимодействия кислоты и основания:
NH4NO2 Na2CO3
NH4OH + HNO2 NaOH + H2CO3
слаб. слаб. сильн. слаб.
Al2(SO4)3 NaNO3
Al(OH)3 + H2SO4 NaOH + HNO3
слаб. сильн. сильн. сильн.
Гидролизу подвергаются соли, которые образованы при взаимодействии слабой кислоты и слабого основания; слабой кислоты и сильного основания; сильной кислоты и слабого основания; это соли NH4NO2, Na2CO3, Al2(SO4)3. Соли, образованные сильной кислотой и сильным основанием, гидролизу не подвергаются (NaNO3).
2. Указать реакцию среды водных растворов солей K2SO3, ZnCl2, Cr(NO3)3, KNO3.
Ответ:
K2SO3
KOH + H2SO3
сильн. слаб.
Реакция среды определяется сильным электролитом, участвующим в образовании соли. Сульфит калия образован слабой кислотой и сильным основанием, поэтому реакция среды щелочная, рН > 7.
ZnCl2 Cr(NO3)3
Zn(OH)2 + HCl Cr(OH)3 + HNO3
слаб. сильн. слаб. сильн.
Хлорид цинка и нитрат хрома (III) образованы сильной кислотой и слабым основанием, поэтому реакция среды кислая, pH < 7.
КNO3
КOH + HNO3
сильн. сильн
Нитрат калия образован сильным основанием и сильной кислотой, гидролизу не подвергается, поэтому реакция среды – нейтральная, рН = 7.
3. Написать полное молекулярное уравнение по данному сокращенному ионно-молекулярному уравнению:
Ca2+ + CО  → CaCО3↓.
→ CaCО3↓.
Ответ: для написания молекулярного уравнения ионы Ca2+ и CО  берем из растворимых солей (см. таблицу растворимости). Вторая образующаяся в результате реакции соль в молекулярном уравнении должна быть растворима.
берем из растворимых солей (см. таблицу растворимости). Вторая образующаяся в результате реакции соль в молекулярном уравнении должна быть растворима.
СaCl2 + Na2CO3 → CaCO3↓ + 2NaCl
растворимая растворимая осадок растворимая
соль соль соль
УРОВЕНЬ B
1. Написать ионно-молекулярные и молекулярные уравнения гидролиза солей:
а) сульфата хрома (III),
б) сульфида натрия
