Механизм электрохимической коррозии
Разрушение металлов в растворах электролитов это результат окислительно-восстановительного взаимодействия, которое слагается из анодного и катодного электродных процессов. Анодный процесс (окисление)— это переход металла в раствор в виде гидратированных ионов; при этом на поверхности металла остается эквивалентное число электронов:
Ме – ne → Men+
Катодный процесс — связывание появившихся в металле избыточных электронов атомами, ионами или молекулами электролита, которые называются деполяризаторами (D):
D + me → Dm+
Без деполяризации анодный процесс, т.е. растворение металла, прекратился бы, как только сформировался двойной электрический слой и установилось динамическое равновесие на поверхности раздела фаз.
Наличие электронной проводимости у металла и ионной проводимости у электролитов позволяет анодным и катодным процессам протекать раздельно на разных участках металла. При этом потенциал анодного участка всегда должен иметь более отрицательное значение по сравнению с потенциалом катодного участка.
Важнейшими деполяризаторами служат ионы водорода (в кислой среде) и растворенный кислород (в нейтральной и щелочной средах):
а) 2H+ + 2 e = H 2 (водородная деполяризация), φа0= 0 В
б) О2 +2Н2О + 4е= 4 OH- (кислородная деполяризация), φб0= -0,41 В (нейтральная среда)
В случае электрохимической коррозии на поверхности металла возникают гальванические микроэлементы, каждый из которых состоит из участков с различными электродными потенциалами. Электрохимическая неоднородность поверхности обусловлена рядом факторов: неравномерным распределением остаточных деформаций в металле после термической и механической обработки, структурной неоднородностью защитных пленок, но чаще всего химической и структурной неоднородностью за счет включений разного рода. Применительно к железу и стали такими включениями могут быть примеси (вкрапления) другого металла, например, медь, шлаки, зерна графита, оксиды железа и, наконец, углеродсодержащая фаза в виде цементита. В конечном итоге в металле возникает множество гальванических микроэлементов с электродами очень малых размеров.
Масштабы потерь от коррозии металлов очень велики. Поэтому борьба с коррозией является одной из важнейших технических проблем в народном хозяйстве. В настоящее время применяют различные способы защиты металлов от коррозии с учетом характера агрессивных сред и условий эксплуатации металлоконструкций. К наиболее важным из них относятся защита поверхности металлов покрытиями, протекторная защита и электрозащита, использование ингибиторов коррозии.
Защита поверхности металла покрытиями. Такие покрытия изолируют от агресссивной среды и могут быть металлическими и неметаллическими. В качестве металлических покрытий чаще всего применяют медь, олово, цинк, никель, хром, тантал, реже — серебро и золото. В зависимости от соотношения электродных потенциалов защищаемого и покрывающего металлов различают анодные и катодные покрытия. В соответствии со своим местом в (гальванической паре более электроотрицательные покрытия являются анодными. Они действуют даже в случае нарушения сплошности.
Например, оцинкованное железо, при нарушении покрытия и попадания на поврежденные участки влаги, образует гальванический элемент, с электродами из железа и цинка. Рассмотрим возможные реакции на его электродах:
1. Fe2+ + 2e → Fe0 φ10= -0,44 В
2. Zn2+ + 2e → Zn0 φ20= -0,76 В
Восстановительная реакция будет протекать на электроде с большим электродным потенциалом, а окислительная на электроде с меньшим электродным потенциалом. Следовательно, окисляться на аноде будет цинк. На катоде же пойдет процесс восстановления, но не ионов железа, которых в электролите нет, а, в зависимости от среды, ионов водорода или кислорода.
А: Zn0 - 2e → Zn2+
К: О2 +2Н2О + 4е = 4 OH- (кислородная деполяризация), φб0= - 0,41 В
Возникший гальванический элемент можно записать следующим образом:
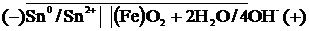
Покрытия, электродный потенциал которых более положителен, чем потенциал защищаемого металла, называются катодными. Они предохраняют изделие до тех пор, пока покрытие остается целостным. Например, в луженом железе анодом служит железо ( -0,44В), а катодом —слой олова
Sn2+/Sn= -0,14 В). Даже незначительное разрушение слоя приводит к быстрому развитию коррозии железа. В этих условиях олово не только не предохраняет от коррозии, а напротив, интенсифицирует ее. Однако достоинством луженых изделий является возможность применения их в пищевой, промышленности. Соединения олова не ядовиты в отличие от весьма токсичных соединений цинка и свинца. Поэтому металлические консервные банки изготавливают исключительно из луженой жести.
Для защиты сельскохозяйственной техники, ирригационного оборудования, насосных станций и гидротехнических сооружений от атмосферной коррозии применяют лаки и краски. Широко используют и другие неметаллические покрытия: эмали, смазки, масла, воск, битум, различного рода полимеры (полиэтилен, полистирол, полиамиды, фторопласты, эпоксидные смолы). Последние весьма эффективны для защиты деталей машин, работающих в контакте с особо агрессивными средами, например, машин для химической обработки растений гербицидами, туковысевающих аппаратов, машин для внесения жидких комплексных удобрений или мелиорантов.
Многослойные битумные покрытия надежно предохраняют подводные и подземные сооружения, включая водоводы и водопроводные сети, от воздействия речной воды, почвенных или грунтовых вод.
Протекторная защита и электрозащита. Это — электрохимические приемы защиты, основанные на том, что защищаемая конструкция становится катодным участком гальванической системы.
В случае протекторной защиты анодом (протектором) служит более активный металл или сплав (например, цинк, магний или их сплавы) с более отрицательным электродным потенциалом, чем потенциал металла защищаемой конструкции. Соединенные электрическим проводником с конструкцией протекторы в процессе эксплуатации разрушаются, предохраняя последнюю от коррозии. Эффективность протекторной защиты зависит от способов размещения протекторов и их размеров.
Катодная защитаотличается от протекторной тем, что защищаемую конструкцию искусственно делают катодом, присоединяя ее к внешнему источнику тока. В каждом отдельном случае подбирают и постоянно поддерживают оптимальное напряжение.
Описанные способы применяют для защиты от коррозии подземных водопроводных сетей, а также гидротехнических металлоконструкций (затворов, шлюзовых ворот, водоводов, сороудерживающих решеток и др.).
Для замедления коррозии металла в среду вводят вещества, называемые ингибиторами коррозии. Защитное действие этих веществ связано либо с окислением поверхности металлов (хроматы, нитриты), либо с образованием пленки труднорастворимого продукта (фосфаты), либо с адсорбционными явлениями). При этом ингибиторы чаще всего изменяют потенциал металла (пассивируют его) в растворе электролита, приближая его к потенциалу малоактивных металлов. Ингибиторы коррозии используются при хранении и перевозке минеральных кислот, при консервации сезонно эксплуатируемых дождевальных агрегатов, комплектов ирригационного оборудования, сельскохозяйственной техники.
Электролиз
Электролиз и его закономерности. Методы обработки поверхности метериалов, основанные на электрохимическом воздействии.
Электролиз — это совокупность окислительно-восстановительных процессов под действием внешнего источника постоянного тока в специальных устройствах — электролизерах. При электролизе происходит направленное перемещение ионов электролита, окисление на аноде одних из них и восстановление на катоде — других. Однако в этом случае катодом служит отрицательно заряженный электрод, а анодом — положительно заряженный, (при электролизе вещества восстанавливаются на катоде и окисляются на аноде).
В качестве примера рассмотрим электролиз расплава хлорида натрия, диссоциирующего по схеме:
NaCl ↔ Na + +CI-
При пропускании электрического тока через расплав катионы натрия движутся к катоду. Здесь, взаимодействуя с электронами из внешней цепи, они восстанавливаются:
Na+ + е = Na
Анионы хлора перемещаются к аноду, где отдают избыточные электроны и окисляются:
Cl - - е = Cl c последующим образованием молекул газа Cl2
Каждая из этих полуреакций протекает не самопроизвольно, а за счет энергии внешнего источника. Суммарная окислительно-восстановительная реакция описывается уравнением:
Na+ + 2CI- = Na + Cl2
Количественно электролиз описывается двумя законами М. Фарадея (1827):
1. Масса выделившегося на электроде вещества пропорциональна количеству электричества, прошедшего через электролит.
2. Одинаковые количества электричества выделяют на электродах массы веществ, пропорциональные их химическим эквивалентам.
Из второго закона следует, что для выделения одного моля химических эквивалентов вещества следует затратить одно и то же количество электричества, не зависящее ни от каких условий. Измерениями установлено, что это количество составляет 96485 (округленно 96500) кулонов и называется постоянной Фарадея (F). Следовательно:
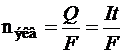
Умножив обе части уравнения на молярную массу эквивалентов, получим:

где: m — масса вещества, г; I — сила тока, А; t — продолжительность электролиза, с; Э — молярная масса эквивалентов вещества, г/моль экв.
