Классификация и номенклатура неорганических веществ.
Классификация простых веществ:
1 Металлы.
2 Неметаллы.
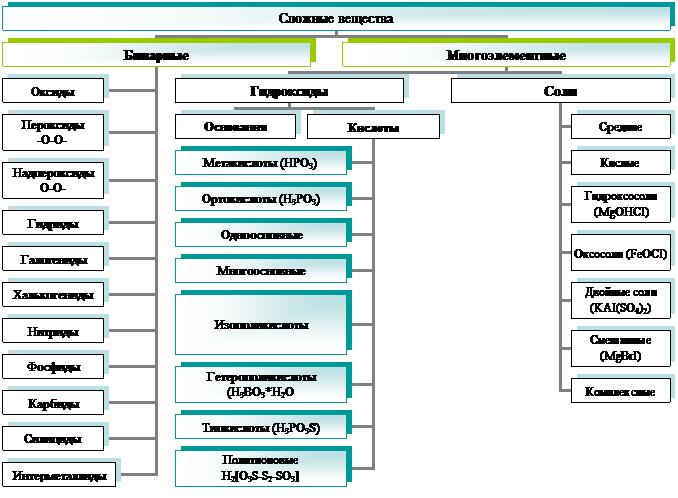
Классификация сложных веществ по составу: 
Классификация сложных веществ по функциональному признаку:
Номенклатура
Традиционные названия
Традиционные названия кислот складываются из двух слов. Собственно название кислоты, выраженное прилагательным, и группового слова – кислота. Собственно название кислоты образуется от русского названия элемента, а степень его окисления указывается с помощью суффикса:
1 +6, +7 – высшая степень окисления. Суффиксы – н, ов, ев (серная, марганцовая, германиевая).
2 +5 – промежуточная степень окисления. Суффикс – новат (хлорноватая).
3 +3, +4 – промежуточная степень окисления. Суффиксы – истов, ист (азотистая, марганцовистая).
4 +1 – низшая степень окисления. Суффикс – новатист (хлорноватистая).
Традиционные названия солей образуются из двух слов. Из названия аниона и катиона. Название аниона указывается в именительном падеже, а катиона в родительном. Название аниона кислоты образуется от латинского названия элемента. Если анион кислородсодержащей кислоты, то употребляются суффиксы и приставками по с/о:
1 Высшая – а; пер (сульфат, перманганат).
2 Низшая – ит; гипо (нитрит, гипосульфит).
Названия по международной номенклатуре даются тремя способами:
1 Метод Штока. Степень окисления электроположительного элемента указывается римской цифрой в скобках. (FeCI3 (III) – хлорид железа три).
2 Метод Эвенса-Бассета. Применяется для ионных соединений. После названия катиона, в скобках, указывается его заряд арабской цифрой. (FeCI3 (+3) – хлорид железа плюс три).
3 Номенклатура ИЮПАК. В 1947г. на совещании Международного союза чистой и прикладной химии (International Union of Pure and Applied Chemistry – сокращенно IUPAC), состоявшимся в Лондоне, было принято решение о пересмотре существующих правил номенклатуры, и выработке новых международных правил. В 1979г. правила были обобщены и тогда же был опубликован их русский перевод – «Номенклатурные правила ИЮПАК по химии. Эти правила опираются на практику англоязычной литературы. При переходе на другие языки учитывается языковые особенности, поэтому в ряде случаев могут быть допущены незначительные отклонения от классического звучания названий. Эту номенклатуру по-другому называют систематическая. В ней для обозначения стехиометрического состава используются числовые приставки или множительные приставки, если числовые уже присутствуют:
- – моно;
- – ди; бис
- – три; трис
- – тетра; тетракис
- - пента;
- – гекса;
- – гепта;
- – окто;
- – нана;
- – дека;
- – ундека;
- – додека.
Если в соединении имеется две электроположительных части, то их названия указываются через дефис.
Названия бинарных соединений состоят из двух слов. Название электроположительной части образуется от корня латинского названия и суффикса – ид. Название электроположительной части образуется от русского названия элемента и указывается в родительном падеже.
Fe2O3 – триоксид дижелеза
W3O10 – декаоксид тривольфрама
MgCI2 – дихлорид магния.
Название гидридов образуются путем добавления к названию элемента суффикса – ан, или – ин.
H2S – моносульфан
AsH3 – арсин
SiH6 – диселан
B2H4 – диборан.
Названия основанийсостоит из слова гидроксид, с указанием числа гидроксогрупп, ирусского названия металла.
AI(OH)3 – тригидроксид алюминия.
Названия кислот и солей состоят из двух слов. Название аниона и катиона в родительном падеже. Все присутствующие в соединении анионы перечисляются с права на лева, в одно слово, и имеют окончание – ат. Оно присоединяется к корню латинского названия кислотообразующего элемента, после которого, в скобках римской цифрой, указывается с/о этого элемента.
Na3PO4 – тетраоксофосфат (V) тринатрия
Fe(NbO2)2 – бис(диоксониобат (III)) железа
NaTl(NO3)2 – бис(триоксонитрат (V)) талия-натрия
Na6(SO4)2CIF – фторид-хлорид-бис(тетраоксосульфат (VI)) гексанатрия
H2Cr2O7 – гептаоксодихромат (VI) гексаводорода.
NaHSO4 – тетраоксогидросульфат (VI) натрия
NaLa(UO2)3(CH3COO)9*6H2O – гексагидрат нанаацетаттриуранила-лантана-натрия
