Специальность: 060301 «Фармация»
Учебный год
Содержание учебно-методического пособия №1
1. Мотивация темы и цель самоподготовки
- Рекомендации для самоподготовки
- Вопросы для самоподготовки
- Задачи для самоподготовки
Мотивация темы и цель самоподготовки.
Современная теория строения атома основана на законах, описывающих движение и взаимодействие микрочастиц (квантовая или волновая механика).
В первые годы ХХ века стало очевидно, что классическая физика терпит неудачу, когда рассматривает явления в атомных масштабах. Чтобы разрешить эту трудность Планк предложил теорию квантов, а де Броиль ввел понятие о «корпускулярных волнах».
В 1861г. Д.И. Менделеев на основании данных других ученых формулирует периодический закон и составил графическое изображение закона – периодическую систему.
Цель самоподготовки
Изучить строение электронных оболочек атомов и периодический закон с точки зрения строения атома.
Представлять: Значение периодического закона и периодической системы. Историю развития представлений о строении атома
Знать: 1)Периодический закон и структуру П.С.
2)Электронное строение атомов элементов .
3)Принцип Паули, правило Гунда, правило Клечковского.
4)Принцип наименьшей энергии.
5)Виды химической связи.
6)Строение веществ неорганической природы.
Уметь:
- Составлять электронные и электронно-графические формулы элементов 1-4 периодов.
- Определять тип химической связи по формуле вещества.
Рекомендации для самоподготовки
- Внимательно прочитайте материал учебника «Неорганическая химия» Л.М. Пустовалова, И.Е. Никанорова, стр.4-65; учебник "Неорганическая химия" Э.Т.Оганесян стр.69-95; и теоретический материал, изложенный в этом пособии.
- Лекции №2 и№3
- Ответьте на вопросы для самоподготовки данного пособия
- Решите задачи для самоподготовки знаний данного пособия.
Вопросы для самоподготовки
1. Основные положения ядерной модели строения атома, ее недостатки.
2. Элементарные частицы строения атома. Изотопы.
3. Современное представление о строении элемента в атоме. Электронное облако. Электронная плотность.
4. Понятие об энергетическом уровне. Главное квантовое число, его значение. Какую информацию можно извлечь из значения главного квантового числа.
5. Квантовые числа, их обозначения. Какую информацию определяет каждое квантовое число.
6. Взаимосвязь между квантовыми числами.
7. Какую информацию дает электронная формула.
8. Принципы минимума энергии. Правило Гунда. Правило Паули.
9. Деление элементов в таблице Менделеева на периоды и группы.
10. Группы элементов. Главные и побочные подгруппы. Какие элементы там располагаются.
11. Типические элементы. Объясните изменения их свойств.
12. Периодические и не периодические свойства атомов.
13. В одном из учебников приведено следующее определение:
«Молекула – наименьшая частица вещества, обладающая
его химическими свойствами».
1. Обсудите недостатки этого определения.
2. Обладает ли молекула физическими свойствами вещества?
3. Попытайтесь дать свое определение термина «молекула».
14. Два моля атомов элемента А образуют соединение с 16 г
кислорода. Определите валентность элемента А.
15. Напишите графические формулы оксида железа(III)
Fe2O3, сульфата бария BaSO4, тритиновой кислоты
Н2S3O6, гидроксида алюминия Al(OH)3.
16. Используя значения, полученные при изучении
органической химии, объясните тост силы кислот в ряду:
СН3СООН>CH2ClCOOH>CHCl2COOH>CCl3COOH
17. Сколько валентных электронов имеют атомы Н, К, Мо, Тl
и Со?.
18. Приведите пример многоатомной молекулы с неполярной
связью.
19. Приведите пример полярной связи, образованной
одинаковыми атомами.
20. Укажите механизм образования всех связей в соединениях
Н3О+, SO3, N2O HNO3, K2SO4.
21. Приведите примеры соединений с б- и П-связями.
22. Какой тип гибридизации имеет место у атоиа азота в
молекуле аммиака?
23. Какой тип гибридизации у атома углерода в молекулах
этана, бутадиена-1,3 и пропина?
24. Какими аномальными физическими свойствами обладает
вода?
25. На основе использования представлений о водородной
связи и о полярности связи объясните наблюдаемые
различия в температурах кипения у следующей группы
соединений:
| Соединение | Т кипения, С |
| Бутан | |
| Метилэтиловый эфир | |
| Пропаналь | |
| Пропанол |
Задачи для самоподготовки
1. Какова сила отталкивании между двумя протонами в ядре атома гелия? Масса протона mp=1,00728 а.е.м. (а.е.м. — «атомная единица массы, 1 а.е.м. = 1,661-10-27 кг), расстояние между протонами принять равным 10-15м, заряд протона q = 1,602-19Кл).
2. Рассчитайте массу атома кислорода 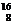 О в а.е.м. (в этих единицах измерения масса протона mp = 1,00728, нейтрона mn = 1,675, электрона me = 5,486*10-4). Сравните полученное значение с числом, приведенным в таблице Менделеева Как Вы думаете, чем объясняется различие? ("подсказка":
О в а.е.м. (в этих единицах измерения масса протона mp = 1,00728, нейтрона mn = 1,675, электрона me = 5,486*10-4). Сравните полученное значение с числом, приведенным в таблице Менделеева Как Вы думаете, чем объясняется различие? ("подсказка":
1. Кислород, находящийся в природе, состоит из смеси изотопов 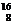 О,
О,  O и
O и  O;
O;
2. Вспомните взрыв ядерной бомбы).
3. Сколько протонов и нейтронов в ядрах  N,
N, 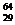 Cu,
Cu, 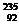 U?
U?
4. Впишите недостающие элементы в реакции:
 N + X =
N + X = 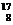 O +
O + 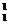 H
H
Х + 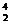 Не =
Не = 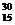 Р +
Р + 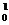 n
n
5. Напишите электронное строение атомов Re, Nb и Вг.
6. Предскажите возможные степени окисления серы, сурьмы, олова. Обоснуйте свою точку зрения.
7. Сравните азотную (HNO3) и метафосфорную (НРО3) кислоты.
8. Укажите три пары элементов, расположение которых в Периодической системе не соответствует Периодическому закону в его первоначальной формулировке.
9. С позиции принципа неопределенности обоснуйте устойчивость атома (невозможность столкновения электрона и ядра).
10. Почему при диссоциации в воде поваренная соль образует ионы Na+ и СI-, а не Na- и СI+?
11. Напишите электронную и электронно-графическую формулу атома серы в основном и в возбужденном состоянии.
12. Плотность паров хлорида элемента по воздуху ровна 5,31. Какой это элемент.
13. Какова масса меди, если в ней содержится 1г электронов (масса электрона 9*10-28г).
ОБЛАСТНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ СРЕДНЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«СМОЛЕНСКИЙ БАЗОВЫЙ МЕДИЦИНСКИЙ КОЛЛЕДЖ»
Учебно-методическое пособие для студентов по
подготовке к практическому занятию
