Периодический закон Менделеева в геохимии.
Периодический закон Менделеева в геохимии.
В 1868 установил закон, связывающий cв-ва хим. эл-ов с их атомными весами. В 1914 году было показано, что в качестве основной константы для периодического закона надо принимать не атомные веса элементов, а заряды ядер их атомов. Согласно закону, свойства элементов изменяются периодически в зависимости от атомного порядкого числа элементов. Это касается: валентности, способности вступать в хим. соединения с другими элементами, состава и свойства этих соединений. Периодичность обнаруживает и многие другие свойства элементов, в том числе их оптические спектры, потенциалы ионизации радиусов атомов и ионов, атомные объемы, окраска ионов, температура плавления, удельные веса и другие. Эти свойства связаны со строением электронных оболочек атомов. Элементы четных порядковых номеров преобладают над нечетными. С увеличение порядковых номеров распространеность уменьшается. Избыточные элементы O, Si, Ca, Fe, Sr, Ba и другие имеют разницу порядковых номеров, равную или кратную 6.
Определение геохимии, ее объект, место среди других наук. История геохимии.
Геохимия изучает историю элементов в ходе геологических процессов, формы их переноса и нахождения в горных породах и минералах, поведение ионов в кристаллических решетках минералов и энергетику геохимических процессов. Геохимия-наука о законах распределения и взаимном сочетании элементов в земной коре, наука, изучающая химические процессы земной коры-миграцию элементов, их концентрацию и рассеяние, химический состав земли и ее оболочки. Геохимия наука комплексная, занимающая промежуточное положение между геологическими и химическими науками. Термин Геохимия был веден Шейнбейтном 1838 год. Фундамент для геохимии: 1859 Бунзеном и Киргором был открыт спектральный анализ, 1869 – закон Менделеева. Создание современной геохимии на основе атомной теории принадлежит Гольдшмиду, Вернадскому и Ферсману. Ферсман-основатель геохимических поисков методов п/и.
Методологическая основа геохимии-второй закон термодинамики (закон энтропии).
Любая природная система стремится перейти в состояние максимальной устойчивости с минимальным запасом свободной энергии. Z=U-TS-PV, Z-изобарно-изотермический потенциал, U-внутренняя энергия, Т-абсолютная температура, S-энтропия, Р-давление, V-объем. Энтропия в термодинамике – это термодинамическая функция состояния системы, элементарное изменение которой в равновесном процессе равно отношению, а в неравновеном больше отношения бесконечно малого количества сообщенной системы теплоты к абсолютной температуре, dS>=Q/T.
Иерархическая лестница природных объектов геохимии.
Электрон; атом; молекула; кристалл (минерал); горная порода; фация (слой); формация; регион; континент; земная кора; планета; галактика; скопление галактик; космос.
Химическая классификация элементов.
1. инертные газы-их внешние оболочки полностью заполнены.
2. сильно электроположительные металлы-имеют 1-3 электрона сверх конфигурации инертных газов. Это щелочи и щелочно-земельные металлы 1 и 2 группы и большая часть 3 группы. Li, Na, K, Rb, Cs, Fr, be, Mg, Ca, Sr, Ba, Ra, Al, Y, La, Ac.
3. неметаллы-те, у которых 1-4 электрона до конфигурации благородных газов F, Cl, Br, I, At, O, S, Se, N, P, As, C, Si.
4. переходные металлы-элементы с незаполненным d слоем Ni, V, Mn, Fe, Cr, Co, Zr, Nb, Mo, Te, Re, Os, Pt.
5. лантаноиды и актиноиды – элементы с незаполненным f слоем.
6. металлы побочных подгрупп на внешних оболочках содержат от 1 до 3 электронов на внешних оболочках сверх электронной предшествующей оболочки Cu, Ag, Au, Zn, Cd, Ga, In, Ti
Геохимическая классификация химических элементов по Гольдшмидту.
В основу положено строение электронных оболочек и величины атомных объемов.
1. атмофильные (инертные газы, азот). Преобладают атомы с 8 электронными оболочками.
2. литофильные (камнелюбивые), в земной коре и мантии, соединения с О.
3. халькофильные, месторождения п/и, руды, соединения с S, Cu, Zn, Pb, As.
4. сидерофильные, находятся в ядре и мантии, Fe, Ni.
Кларки.
Кларки элементов - числа выражающие среднее содержание элементов в земной коре, гидросфере земли в целом, космических тел и др. геохимических и космических систем. Различают весовые и атомные кларки. Элементы с четным порядковым слагают 87% массы земной коры, а с нечетными только 13%, средний химический состав земли в целом рассчитывался на основании данных о содержании элементов в метеоритах. Кларк служит эталоном сравнения пониженных или повышенных концетраций элементов в месторождениях п/и горных пород или целых регионов. Знание их важно при поиске и промышленной оценки месторождений п/и. Главные элементы: О, S, Al, Fe, Ca, Na, K, Mg, Ti, Mn. Количество кларка уменьшается по мере увеличения номера элемента, количество легких элементов до железа снижается быстрее, чем тяжелых.
В земной коре: O2 – 47 Si – 29 Al – 8 Fe – 5 Ca – 3 Na – 3 K – 3 Mg – 2 Ti 0,5 Mn – 0.1
Метеориты.
Метеориты представляют собой обломки космической материи, 2 типа: каменные и железные, или силикатные и металлические. В их веществе выделяются 3 фазы:
1. железоникелевая или металлическая
2. сульфидная или троилитовая
3. каменная или силикатная.
Каменные делятся на хондриты и ахондриты.
Хондриты-примитивный тип метеоритов, представляют собой продукты значительно более сложных процессов химической дифференциации вещества. Они состоят из оливина, пироксена, никелистого железа и плагиоклаза.
Ахондриты-группа каменных метеоритов характеризуется большим разнообразием. Они обладают кристаллической структурой, многие из них имеют большое сходство с изверженными породами на земле. Делятся на 2 группы: бедные и богатые кальцием.
16-1 Отличия элементного состава литосферы земли от состава поверхности луны, марса, венеры и планет-гигантов.
Венера близка по размерам и средней плотности к земле. Обладает наиболее плотной и мощной атмосферой из всех внутренних планет. Атмосфера планеты состоит почти целиком из СО2 (93-97%), обнаружено присутствие кислорода, азота, воды, содержание азота вместе с инертными газами достигает 2-5%, а количество О-0,4%, Т=747 К, а Р=90*10^5 Па. Марс обладает самой низкой плотностью, имеется разреженная атмосфера, атмосферное давление у поверхности не превышает 800 Па на 2 порядка меньше, чем на земле. Основной компонент атмосферы СО2, обнаружено содержание примеси NO2, содержание О2 и О3 пренебрежительно мало. Луна – лишенная атмосферы. Повышенные гравитационные аномалии в районах лунных морей. По косвенным данным можно допустить, что в составе внешних планет много гелия. В центральных частях внешних планет гелия (уран, нептун, юпитер, сатурн).
Атомный и ионный радиусы.
Атомные радиусы-числа, получаемые при измерении растояния между центрами атомов в кристаллической структуре. Атомные радиусы элементов, у которых заполняются s и p уровни, закономерно возрастают в каждой группе в направлении сверху вниз, при увеличении числа слоев в атоме. В пределах каждого периода слева на право, при увеличении числа элементов в слое, атомные радиусы уменьшаются. Наращивающие d уровни в начале ряда уменьшаются, затем возрастают.
Ионные радиусы-радиусы ионов, а точнее атомов в состоянии, когда у них проявляется ионная связь. Размер иона изменяется в зависимости от внешних условий и влияния окружающих соседей в структуре минерала. Радиус иона зависит от его валентности. При возрастании положительной валентности радиус уменьшается по сравнению с атомами, а при отрицательной валентности возрастает. У s, p, d уровнях в первых периодах радиус чуть сокращается, далее возрастает, для f уменьшается во всем ряду. В вертикальных группах радиусы возрастают сверху вниз.
Изотопная геохронология.
Метод определения возраста. Путем радиоактивного распада 40К превращается в Ar, зная константы, можно измерить концентрацию материнского и дочернего изотопов и вычислить возраст. Распад 40К стабильного 40Ar происходит путем электроного захвата, 11% атомов 40К распадаются путем электронного распада до ядер 40Ar в возбужденном состоянии, которые переходят в основное состояние, испуская гамма излучение. Преимущественно же атомы 40К путем бетта распада переходят в состояние 40Ca. 40Ar-39Ar метод датирования. С помощью 40Ar/39Ar можно преодолеть некоторые затруднения, возникающие при датировании K-Ar методом.
Rb-Sr метод. Точный изотопный состав строения в породе или минерале, которые содержат рубидий, зависит от возраста и отношения Rb/Sr в этой породе или минерале. Из всех этот метод наиболее тесно связан с петрологией и геохимией. Преимущество перед Cl-Pb заключается в том, что в нем используются главные породообразующие минералы, такие как слюда и полевые шпаты, которые определяют историю породы. Перед K-Ar Rb-Sr имеет преимущество в том, что он связан с геохимией пород. Если аргон выносится из слюд, то его сохранность в породе контролируют случайные факторы, такие как наличие близлежащих трещин и зон разломов. Применение метода рубидия-стронция ограничивается двумя факторами:
1. большим периодом полураспада 87Rb
2. тем, что обычный стронций содержит около 7 % 87Sr. Для датирования пригодны только образцы с высокими отношениями Rb/Sr причем чем больше возраст, тем отношение выше.
Координационные числа.
К каждой частице, находящейся в кристалле, примыкает вплотную только определенное число соседних частиц. Это число ближайших соседних частиц называется координационным числом. В структурах алмаза, кремния к.ч.=4, NaCl=6, наибольшее число 12, что характерно для металлов с плотнейшей кубической или гексагональной упаковкой, для полупроводников кристаллов, не имеющие плотнейшей упаковки атомов характерно к.ч.=4 или 6.
ЭКи по Ферсману.
Энергентические коэффициенты, введенные Ферсманом, базируются на величинах радиусов ионов и относятся к важнейшим понятиям в геохимии.
ЭКаниона=W2/aRиона
ЭКкатиона=W2/aRиона
(0,75R+0,15)
ЭК-величины безразмерные, однако, умножив их на 1071, 74 получаем кДж. Это определенный пай энергии, который вносится каждым ионом при формировании кристаллической решетки. Применение ЭК ограничивается ионной формой, а во многих случаях есть возможность решения обратной задачи: если с помощью Эк и радиуса иона невозможно объяснить некоторые процесы, то элементы в них участвуют не в виде ионов. Для решения некоторых задач Ферсман считал необходимым определить пай энергии иона, приходящийся на единицу заряда. Этот коэффициент обозначают ВЭК, равняется ЭК, деленный на валентность. ЭК и ВЭК получили широкое применение в геохимии. Они используются для определения энергии кристаллических решеток, твердости и растворимости минералов, дальности миграции и зональности концентрации ионов.
Эвтектическая дифференциация. Примеры и представители пород.
Гранитная эвтектика-тройная, определяется соотношением приблизительно в равных количествах по 30% альбита, ортоклаза, кварца.
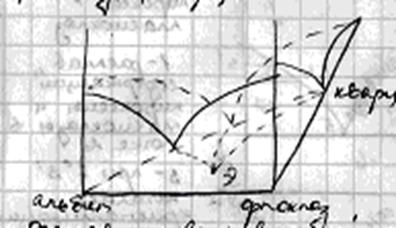 Рисунок 4
Рисунок 4
Расплав, соответствующий граниту, выплавляется из вещества, богатого кремнеземом и водой, получается кисло-мокрая магма. Такой состав имеют осадочные породы, поэтому вещество всех гранитов когда-то было осадочным.
Все граниты сходного эвтектоидного состава, т.е. приблизительно соответствует 1/3 альбита, 1/3 ортоклаза, 1/3 кварца. Однако это соотношение немного меняется в зависимости от Р и Т, кроме того, до 10% в граните-слюды и роговые обманки. Поэтому гранитная эвтектика более многомерна.
Два крыла эвтектики образованы двумя группами минералов, кристаллизующиеся по закону изоморфной смеси. У пироксенов: энстатит-бронзит-гиперстен. У плагиоклазов: альбит-анортит.
Ударный метаморфизм.
Это изменение в горных породах и минералах, обусловленные происхождением мощной ударной (метеоритной) волны. Единственным известным природным процессом, при котором может происходить ударный метаморфизм является падение крупных метеоритов. Характеризуется мгновенностью проявления, высоким Р (10-100 кбар-Мбар) и остаточной температурой свыше 1500. Возникают высокобарические фазы ряда соединений, происходит дробление минералов, разрушение их кристаллических решеток, плаление минералов и горных пород.
Лунные, солнечные циклы.
Приливные воздействия луны в несколько раз больше, чем у солнца, потому что луна ближе. Если солнце, земля, луна выстроились в одну линию (новолуние, полнолуние), то приливы максимальны. Если луна в полуфазе, то приливы минимальны. Приливы происходят не только в океане, но и ов всей земной коре. Приливная волна бежит по земле, немного ее вытягивает и сплющивает. В результате изменений приливных сил в течение суток предопределяют не только приливы и отливы, но и провоцируют землетрясения, более вероятные в полнолуние и новолуние. Лунно-солнечный календарь. Солнчная система движется и по отношению к солнцестоянию. Солнц в тепловом режиме поставляет на землю ккал. А в радиодиапазоне, в гамма лучах, в рентгеновских лучах солнце крайне непостоянно. От этих излучений нас ограждает атмосфера.
Мезо-кайнозойский цикл.
Длится триас-четвертичка. Т наступил после пермского соленакопления, происходит крупная регрессия-осадки почти не отлагаются. Но там, где есть осадконакопление, отлагается С и образуются месторождения гиганты (нефть). T3-J1-J2 – трансгрессия, планетарный холод. Формируются теригенные толщи с нефтью в одних случаях и углем в других. К концу J3 потепление углерод отлагается в виде карбонатов (СО3): унификация теплового климата по всей планете, нет п/и. В J3-K1 продолжается потепление, но на континентах усиливается регрессия, в южных районах образуются соляные отложения; в северных (там похолодало вследствие дифференциации климата)-углеродистые (нефтяные) толщи. Следующий углеродистый цикл К1 начинается с терригнных (нефтяных) отложений, завершается отложением карбонатов (К1-К2) великое планетарное потепление, трансгрессия, отсутствие п/и. В К-палеогене новое похолодание, также завершается отложением карбонатов. Всего 6 циклов. Мы живем в регрессивной части цикла и у нас галактическая зима. П/и образуются в течение углеродистого цикла (весной и осенью). Зимой фосфор и углерод не выводятся в осадки из биосферного оборота. Летом углерод связывается в карбонаты, следовательно нет п/и.
Состав живого вещества.
В организмах создаются многочисленные органические соединения (улеводы, жиры, белки, элементарные органические соединения и др) В состав организмов входит целый ряд элементов. Один-в больших количествах и постоянно, другте-в малых и не всегда. Все элементы в организмах с учетом количества можно разделить на 3 группы: макрохимические, микрохимические, ультраэлементы.
Первые биогенные элементы абсолютно необходимые для жизни. C, O, H, N, S, P, K, Fe, I, Mn, Zn, Cu. В организмах обнаружены: Li, Be, Se, Ga, Ge, W, Ar, Mo, Rh, Pd, Pt, Cd, Sr, Cs, Te, Sb, Bi, U, La, Cl
Элементы обнаруженные в организмах относятся большей частью к циклическим. К макроэлементам относятся: O, H, C, N, Ca, S, P, K, Si
Микроэлементы: Zn, Br, Mn, Cu, Об As, B, F, Pb, Ti, V, Cr, Ni, Sr
Ультраэлементы: Ag, Co, Ba, Th, Au, Rb, Hg/
Углеродный цикл.
Элементы. Входящие в состав органическог овещества образуют сложные в основно массе эндотермичские соединения и таким образом находятся на высшем энергетическом уровне. Покинув живое вещество в форме таких соединений они проходят некоторый путь прежде чем перейдут в наимение активные и наиболее устойчивые формы вне организмов. Такой путь проходит углерод в земных растениях, захваченный растениями из СО2 атмосферы в результате фотосинтеза и находящийся в них самых разнообразных соединениях (клетчатка, белок) углерод попадает в тела животных и других гетеротрофных организмов. В результате дыхания этих организмов углерод довольно быстро через ряд промежуточных соединений принимает наимнее активную форму СО2. Другая часть углерода после смерти организмов в соответствующих условиях аккумуляции, скапливается в углях-сопропелитах, переходит в нефть и через длительный промежуток времени попадает в исходную малоактивную форму СО2 атмосферы. Этот круговорот углерода осуществляется за счет энергии солнечных лучей, трансформируемых хлорофиолом зеленых растений.
Периодический закон Менделеева в геохимии.
В 1868 установил закон, связывающий cв-ва хим. эл-ов с их атомными весами. В 1914 году было показано, что в качестве основной константы для периодического закона надо принимать не атомные веса элементов, а заряды ядер их атомов. Согласно закону, свойства элементов изменяются периодически в зависимости от атомного порядкого числа элементов. Это касается: валентности, способности вступать в хим. соединения с другими элементами, состава и свойства этих соединений. Периодичность обнаруживает и многие другие свойства элементов, в том числе их оптические спектры, потенциалы ионизации радиусов атомов и ионов, атомные объемы, окраска ионов, температура плавления, удельные веса и другие. Эти свойства связаны со строением электронных оболочек атомов. Элементы четных порядковых номеров преобладают над нечетными. С увеличение порядковых номеров распространеность уменьшается. Избыточные элементы O, Si, Ca, Fe, Sr, Ba и другие имеют разницу порядковых номеров, равную или кратную 6.
