Исследования связи структура-активность
Одним из ключевых параметров лигандов TSPO, определяющих их биологическую активность, является их аффинность по отношению к этому рецептору. В связи с этим нами был проведен анализ теоретической аффинности новых лигандов TSPO в ряду 1-арилпирроло[1,2-a]пиразин-3-карбоксиамидов с использованием QSAR и метода молекулярного докинга.
QSAR/QSPR – метод измерения количественной связи между структурой молекулы и её свойством, в нашем случае -активностью. Методы QSAR появились в начале 1960-х и их основателем был Корвин Ганч. Основное применение QSAR моделей- прогноз биологической активности для химических соединений[50]. Для числового обозначения молекулы используют независимые друг от друга числовые параметры молекулы - дескрипторы. [51]
Существующие QSAR методы можно разбить на две группы: на основе трехмерной структуры молекулы и на основе топологии молекулы, которые используют информацию о атомах и типах связи между ними, а также другие локальные дескрипторы (липофильность, константы заместителей, дипольный момент и др.). Структурная формула молекул записывается в виде молекулярного графа, где атомы — это вершины, а ребра – это связи между атомами. Однако топологический подход не позволяет учитывать информацию о взаимном расположении структурных особенностей в пространстве и такие методы не могут быть универсальным инструментом прогнозирования физиологической активности.
Для построения QSAR моделей формируется обучающая и тестовая выборка из молекул для которых заранее известна биологическая активность. Обучающая выборка загружается в компьютерную программу, которая проводит подбор дескрипторов и строит зависимость как А = f(D), где A- активность, D – дескриптор. На основе обучающей выборки строится корреляционное уравнение активности из набора дескрипторов. Модель проверяется с помощью тестовой выборки, в которой активность молекул уже известна. Таким образом модель связывает активность с определенными фрагментами в молекуле и их окружением. Точность модели зависит от размера обучающей выборки и оптимального набора дексрипторов. [52]
Анализ связи структура-активность [24] (Таблица 4) показал, что наибольшую активность проявляют соединения, у которых отсутствует заместитель в бензольном кольце (R3 = H), а амидная группа замещена на метильную (R1= CH3) и бензильную или н-бутильную группу (R2= Bz, n-Bu). Различные вариации орто заместителя R3 в бензольном кольце (ГМЛ-2, ГМЛ-4, ГМЛ-5) при R1=CH3, R2=n-Bu, приводят к снижению активности. При введении фтора в R3 положение активность снижается, а при введении брома и хлора полностью исчезает. Удаление одного из заместителей у амидной группы (ГМЛ-7 и ГМЛ-8) R1 или R2 = H существенно снижает активность.
Таблица 4.
| Шифр | R1 | R2 | R3 |
| ГМЛ – 1 | CH3 | Bz | H |
| ГМЛ – 2 | CH3 | n-Bu | Cl |
| ГМЛ – 3 | CH3 | n-Bu | H |
| ГМЛ – 4 | CH3 | n-Bu | F |
| ГМЛ – 5 | CH3 | n-Bu | Br |
| ГМЛ – 6 | CH3 | втор-Bu | H |
| ГМЛ – 7 | H | Bz | H |
| ГМЛ – 8 | H | CH3 | H |
| ГМЛ – 9 | CH3 | Bz | F |
| ГМЛ – 10 | CH3 | Bz | Cl |
| ГМЛ – 11 | CH3 | изо-Bu | H |
Для анализа количественной связи структура-активность построена QSAR модель на основе обучающей выборки из 1297 соединений с известной константой ингибирования. Первоначально осуществили поиск лигандов TSPO с известными константами ингибирования в базе данных химических структур ZINC [53]. Полученную базу в формате sdf загрузили в веб-сервис для QSAR моделирования - OCHEM [54]. Были созданы 9 моделей из комбинации трех методов машинного обучения (ASNN, FSMLR, PLS) с различным набором 2D фрагментарных дескрипторов (OEState, ISIDA, GSFrag). Для валидации модели использовался 5 – кратный перекрёстный контроль. В результате была выбрана модель на основе искусственных нейронных сетей с коэффициентом корреляции r2= 0,68 (Таблица 5) и параметром перекрёстного контроля q2= 0,65 (Таблица 6). Графическое отображение модели изображено на рисунке 5. В качестве дескрипторов были использованы фрагментарные дескрипторы ISIDA длинной 2-4 атома.
Таблица 5. Значения коэффициента корреляции для комбинаций дескрипторов и методов машинного обучения.
| R2 | ASNN | FSMLR | PLS |
| ALogPS, OEstate | 0.62 | 0.32 | 0.41 |
| Fragmentor (Length 2 - 4) | 0.68 | 0.41 | 0.5 |
| GSFrag | 0.67 | 0.22 | 0.33 |
Таблица 6. Значения коэффициента перекрестного контроля для комбинаций дескрипторов и методов машинного обучения.
| Q2 | ASNN | FSMLR | PLS |
| ALogPS, OEstate | 0.6 | 0.24 | 0.39 |
| Fragmentor (Length 2 - 4) | 0.65 | 0.4 | 0.48 |
| GSFrag | 0.64 | 0.32 |
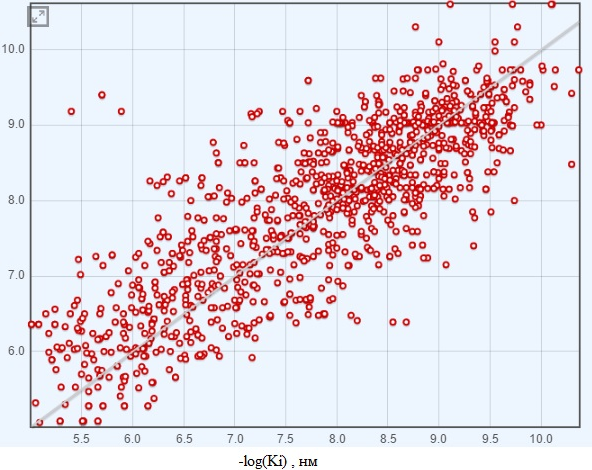
Рис.5 Графическое отображение прогностической модели от фрагментарных дескрипторов ISIDA
Фрагментарные дескрипторы ISIDA базируются на двух классах дескрипторов: подструктурные молекулярные фрагменты и фармакофорные триплеты. Подструктурные молекулярные фрагменты разбиты на три класса: (1) последовательность соединенных атомов и связей, (2) только атомы или пары атомов, (3) расширенный набор атомов с близкой средой и их связей. Фармакофорные триплеты производят поиск и выделение определенных фармакофорных фрагментов (H-доноры, H-акцепторы, анионы, катионы и т.д) на заданных топологических расстояниях [55].
В результаты были получены прогнозируемые значения аффинности для 22 структур (Таблица 7) с различными заместителями у амидной группы.
Таблица 7. Значения прогнозируемой активности от фрагментарных дескрипторов ISIDA.
| № | R1 | R2 | Ki, -log(M) | № | R1 | R2 | Ki, -log(M) |
| Me | H | 5,3 | Ph | n-Bu | 6,2 | ||
| Et | Et | 5,5 | Bz | Me | 6,9 | ||
| Pr | Pr | Bz | Et | 5,7 | |||
| Me | n-Bu | Bz | n-Bu | 6,2 | |||
| Me | i-Bu | Bz | i-Pr | 5,4 | |||
| Me | sec-Bu | 6,4 | Bz | Bz | 5,5 | ||
| цикло | гексил | 5,1 | Ph | Bz | 5,8 | ||
| Bz | H | 5,2 | Ph | Ph | 6,1 | ||
| Ph | Et | 5,7 | Ph | циклогексил | 5,2 | ||
| Ph | Pr | 6,1 | Ph | циклопентил | 5,6 | ||
| Ph | Me | 6,4 | Naph | H | 5,6 |
Молекулярный докинг.
Метод молекулярного докинга удобный инструмент для расчета энергии связи «лиганд-белок» и поиска конформации лиганда связанного с белком. Программа осуществляет поиск глобального минимума, используя генетический алгоритм. В процессе докинга лиганд помещается в пространство, для которого заранее подготовлены электростатические карты для каждого химического элемента лиганда. В процессе моделирования генерируется начальная популяция лигандов порядка 300, затем рассчитывается разница энергий связывания между начальным положением и «мутантным». Выбирается лучшая конформация и процесс повторяется. В результате докинга мы получаем значения ∆G для комплекса лиганд-белок и положение молекулы соответствующее этой энергии. (Рис.3)
Расчет производится при помощи программного обеспечения AutoDock 4.2 [56]. Для оценки аффинности соединений использовалась структура TSPO млекопитающего (мыши) в комплексе с лигандом PK11195, полученная в высоком разрешении методом ЯМР‑спектроскопии [57].
Все исследованные лиганды были переведены в 3D структуры в программе Marvin Sketch, после чего использовались для in silico лиганд-белкового докинга. Молекулярный докинг производился в несколько этапов. Сначала из комплекса 2MGY был удален исходный лиганд PK11195, после чего в программе AutoDock к молекуле белка были добавлены водороды и посчитан заряд по методу Гейстегера[58]. Далее, 3D результат докинга визуализировался в программе PyMOL с обозначением поверхности кармана связывания (Рис.6)
Рис. 6 Трёхмерная модель активного центра TSPO.
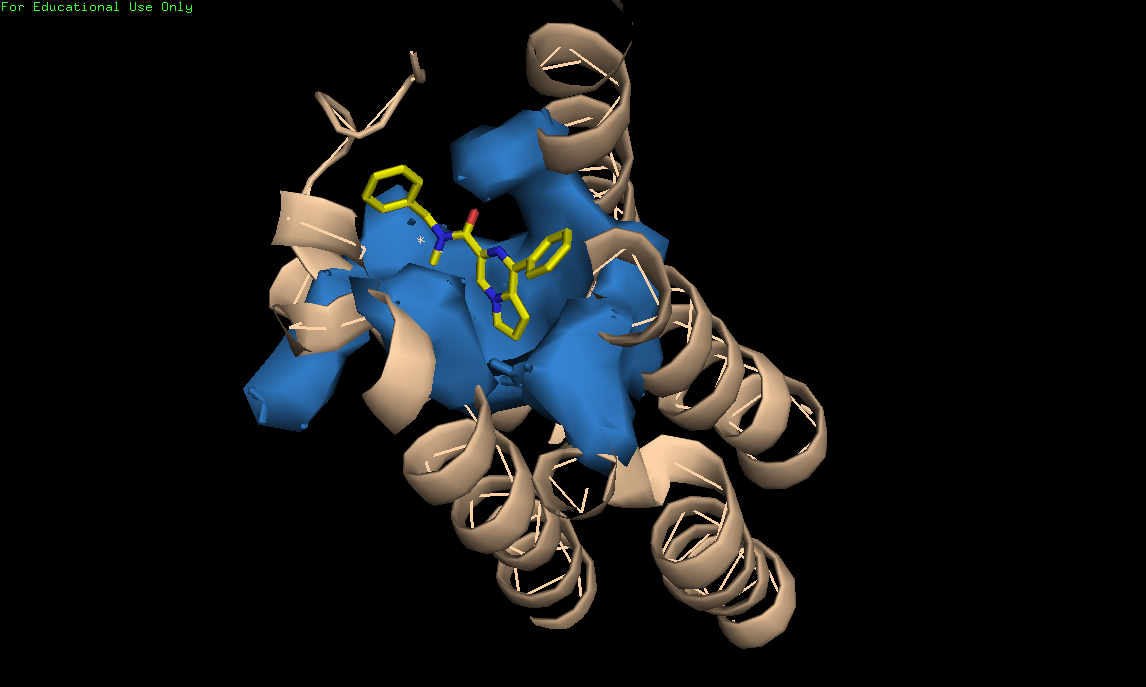
Таблица 8. Результаты молекулярного докинга при помощи программы AutoDock 4.2
| № | R1 | R2 | Ki, nM | Clog P | № | R1 | R2 | Ki, nM | Clog P |
| Me | H | 1,89 | Ph | n-Bu | 5,09 | ||||
| Et | Et | 2,82 | Bz | Me | 3,83 | ||||
| Pr | Pr | 3,87 | Bz | Et | 4,19 | ||||
| Me | n-Bu | 3,43 | Bz | n-Bu | 5,16 | ||||
| Me | i-Bu | 3,35 | Bz | i-Pr | 4,61 | ||||
| Me | sec-Bu | 3,4 | Bz | Bz | 5,56 | ||||
| цикло | гексил | 2,96 | Ph | Bz | 5,49 | ||||
| Bz | H | 3,61 | Ph | Ph | 5,42 | ||||
| Ph | Me | 3,77 | Naph | H | 4,89 | ||||
| Ph | Et | 4,12 | Ph | циклопентил | 5,48 | ||||
| Ph | Pr | 4,65 | Ph | циклогексил | 5,57 |
Дальнейшему анализу подвергли самые аффинные соединения (17,18,19,20) и соединения с Clog P <4,5 (9, 10, 13, 14). В результате докинга определилось два основных мотива связывания.
В одном мотиве пирролопиразиновый остов наиболее аффинных соединений 18 и 19 гидрофобно взаимодействует с ароматическими остатками триптофана (95 ,107), аланина (110, 147) и лейцина 150, а липофильные заместители амидной группы с лейцином 150, серином 41, триптофаном 143, изолейцином 52. Фенильное кольцо у гетероароматического остова располагается около двух остатков триптофана 53 и 95 (Рис 7,8). Соединение 10 имеет похожий мотив связывания, однако фенильное кольцо в гетероцикле несколько сдвинуто к остатку триптофана 143 (Рис. 9), в отличие от соединений 18 и 19, которые не могут сдвинуться из-за наличия объемных заместителей у амидной группы.
Рис.7 Положение соединения 18 в сайте связывания PK-11195.
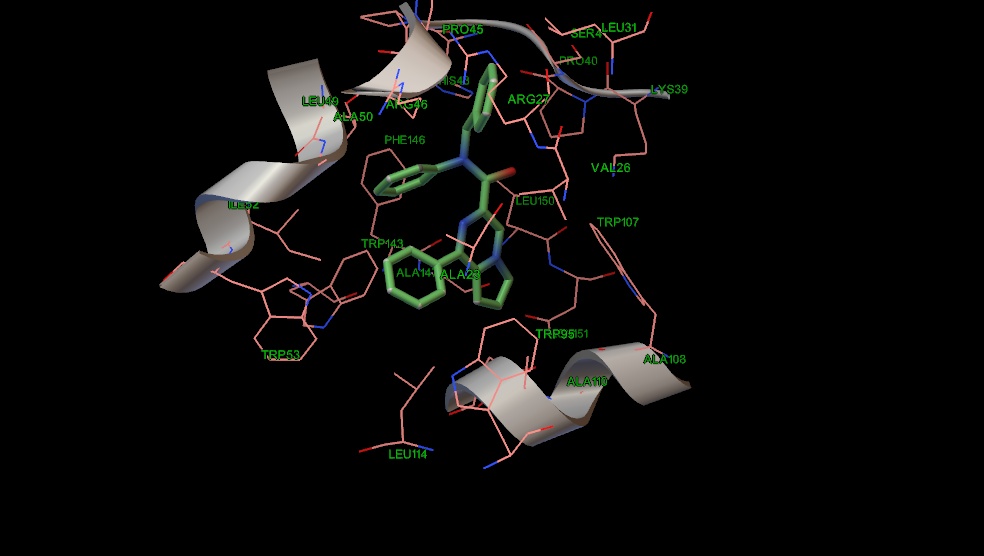
Рис. 8 Положение соединения 19 в сайте связывания PK-11195.
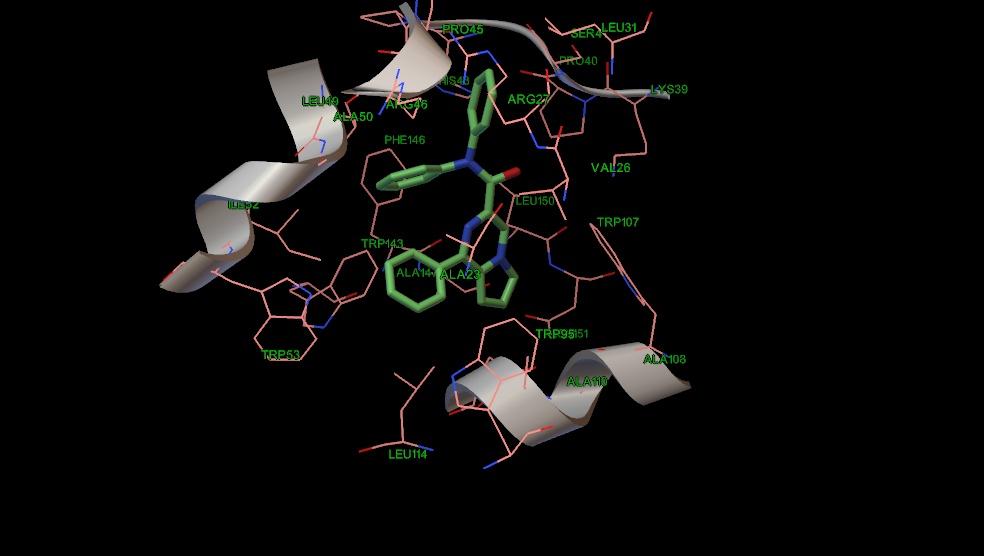
Рис. 9 Положение соединения 10 в сайте связывания PK-11195.
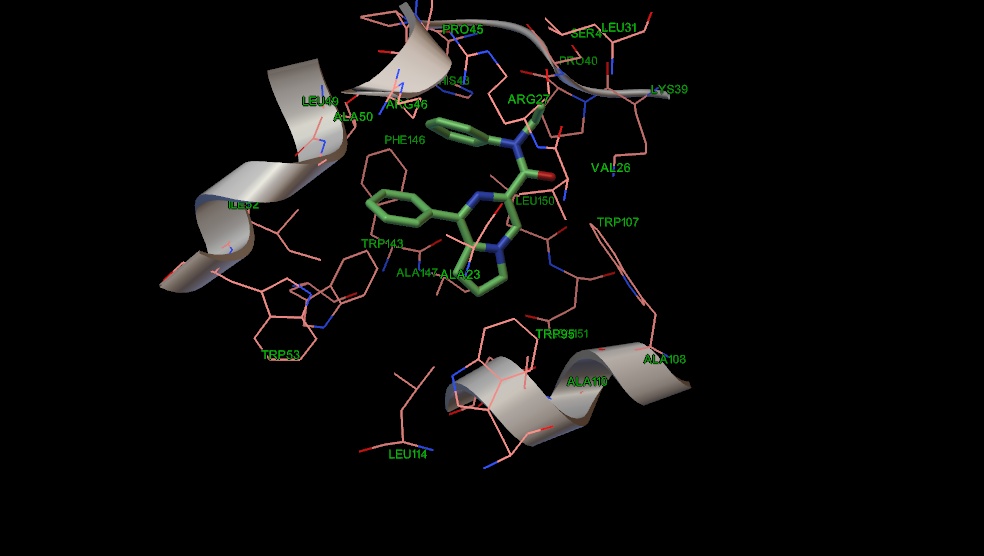
Альтернативный мотив связывания предсказан для структур (9, 13, 14, 17 ,20). В отличие от соединений 10,18,19 гетероциклический остов молекул 13 и 17 (Рис 10,11) взаимодействует с остатками триптофана (53,143), изолейцина 52 и аланина 23. Однако у соединений 9, 14, 20 фенильное кольцо сдвигается в сторону стэкинг взаимодействия с триптофаном 107, что в итоге сдвигает пирролопиразиновый цикл к остатку триптофана 95 и лейцина 114 (Рис 12,13,14). У амидного атома азота соединений 13 и 17 положения бензильной группы совпадают, а насыщенные атомы углерода направлены к лейцину 49. Этильный радикал у амидного азота соединения 14 также направлен к лейцину 49, а бензильная группа к валину 26. Соединение 9 тоже несколько сдвинуто по метильному радикалу к остатку лейцина 49. Нафтильная группа в соединении 20 имеет дополнительную область связывания с валином 26, лейцином 31, серином 41 и аргинином 46. Таким образом, введение электроноакцепторной группы в параположение фенильного кольца у атома амидного азота может увеличить сродство к TSPO.
Рис. 10 Положение соединения 13 в сайте связывания PK-11195.
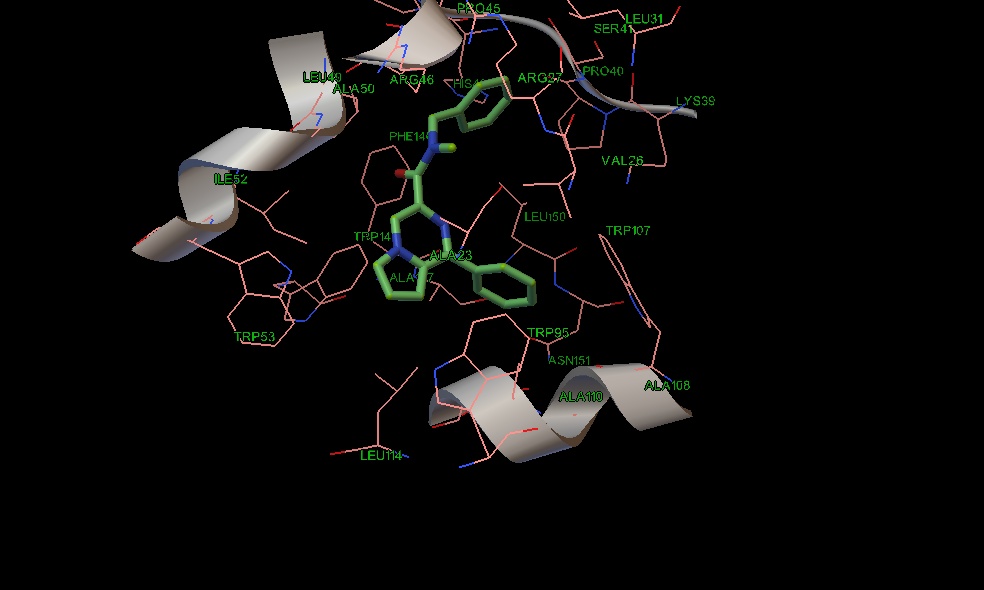
Рис. 11 Положение соединения 17 в сайте связывания PK-11195.
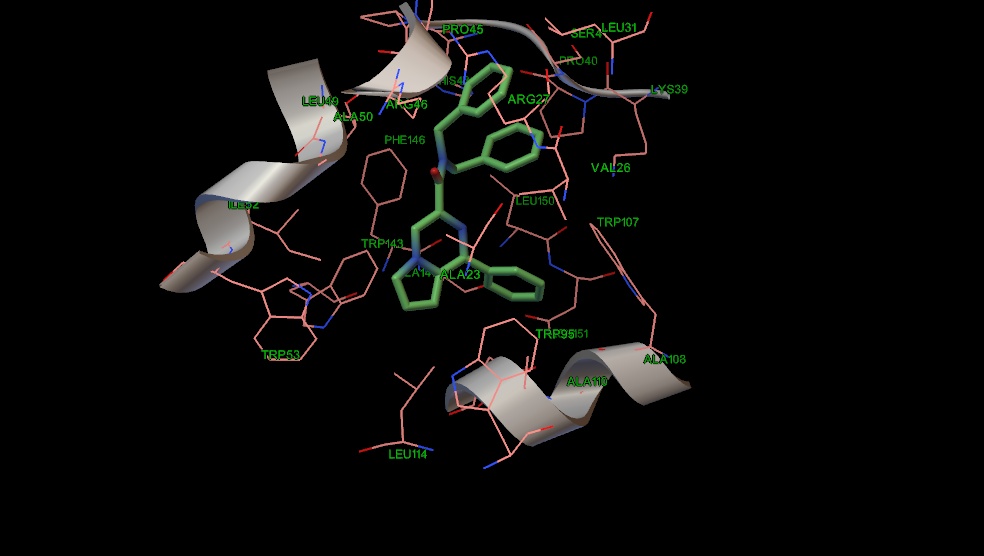
Рис. 12 Положение соединения 9 в сайте связывания PK-11195.
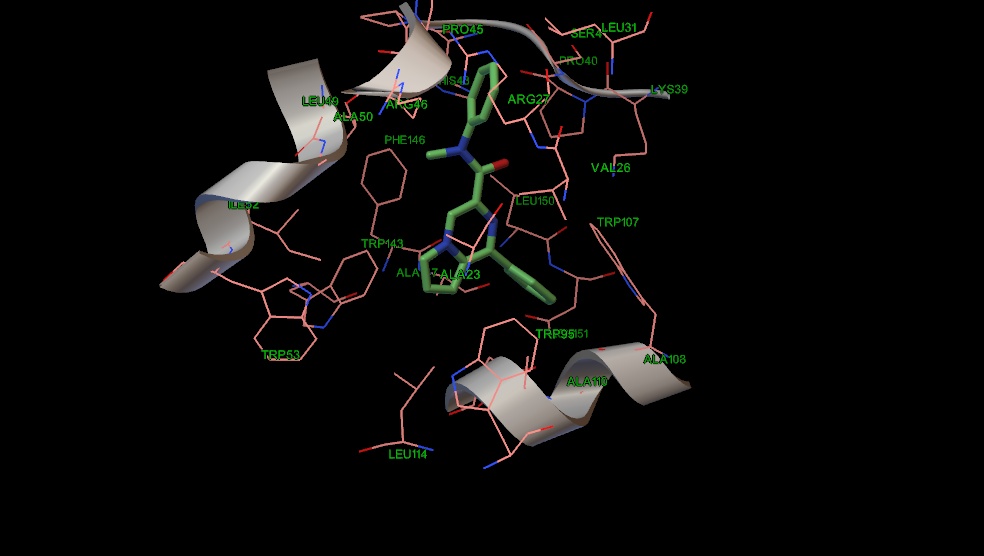
Рис. 13 Положение соединения 14 в сайте связывания PK-11195.
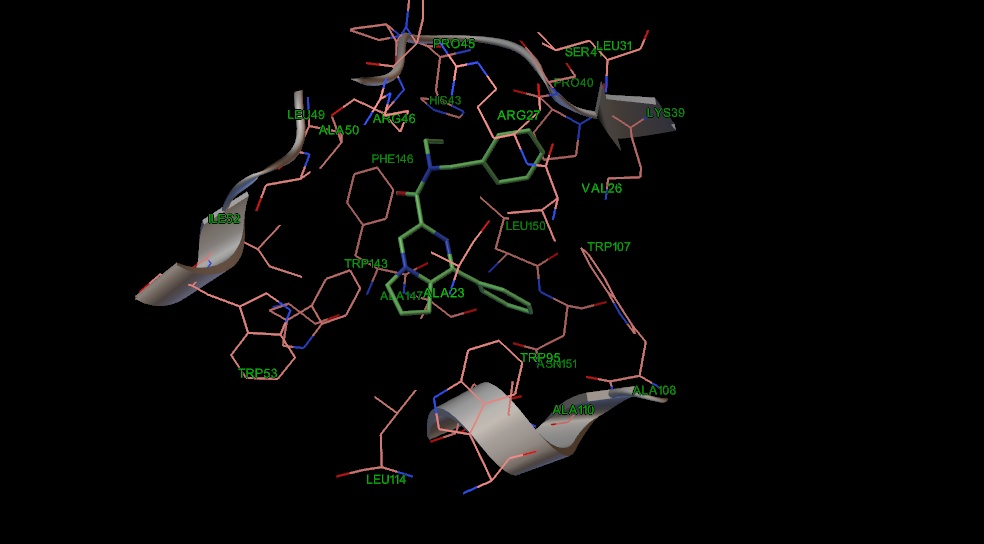
Рис. 14 Положение соединения 21 в сайте связывания PK-11195.
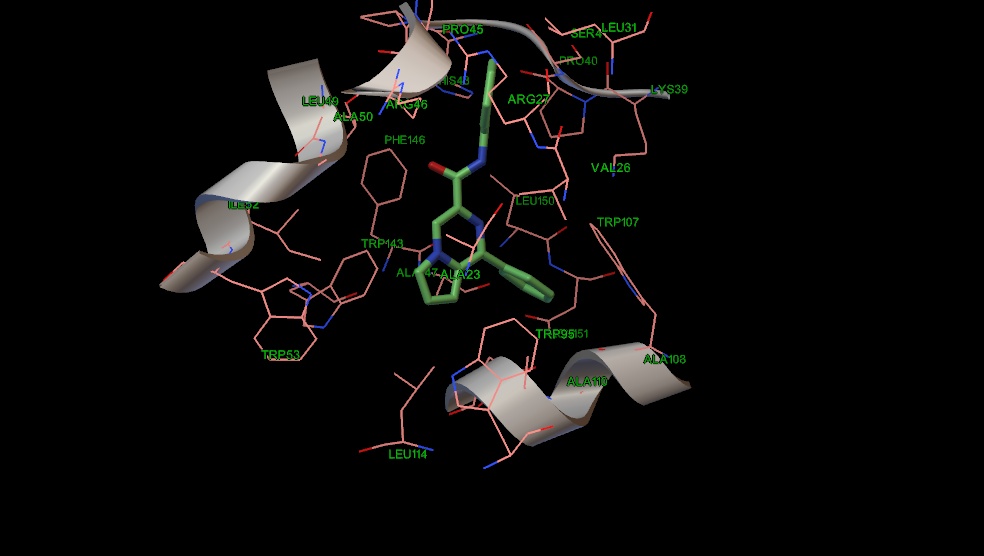
По причине того, что карман активного центра PK-11195 достаточно гидрофобен, проведен анализ соответствия гидрофобной поверхности лиганда к поверхности белка с помощью веб-сервиса PLATINUM. В этом веб-сервисе производятся вычисления, основанные на концепции молекулярного гидрофобного потенциала, который присваивается каждому атому в зависимости от его природы. Затем производится анализ поверхности молекулы лиганда и его окрестностей. Результат -это число, полученное при делении гидрофобно комплементарной поверхности лиганда к белку на общую поверхность лиганда. Также на основе эмпирических функций ведется учет стэкинговых взаимодействий между ароматическими остатками аминокислот и ароматическими фрагментами лигандов. Результаты исследуемых структур сравнивали с результатами классического лиганда TSPO PK-11195 (Таблица 9).
Таблица 9. Результаты проверки гидрофобного соответствия в веб-сервисе PLATINUM.
| Номер молекулы | π – π стэкинг | Соответствие |
| 1,65 | 0,8859 | |
| 0,87 | 0,9459 | |
| 2,42 | 0,9139 | |
| 2,03 | 0,9371 | |
| 1,78 | 0,8971 | |
| 0,71 | 0,9235 | |
| 0,95 | 0,9339 | |
| 1,76 | 0,8701 | |
| PK-11195 | 1,97 | 0,9609 |
В итоге вышеперечисленных прогнозов, принимая во внимание коэффициент clog P и результаты соответствия гидрофобных поверхностей, соединения 13,16,18,19,20 не подходят к правилу Липински clog P < 5[59]. Оптимальные значения log P для проникновения через гематоэнцефалический барьер лежат в интервале 1.5-2.7[60]. Таким образом, перспективными соединениями, учитывая липофильность, аффинность и гидрофобный потенциал, стали соединения 9, 10, 13, 14.
В результате исследований теоретических расчетов липофильности и аффинности к TSPO пирроло[1,2-a]пиразинов был сделан вывод, что N-метил-N-фенил-1-фенилпирроло[1,2-a]пиразин-3-карбоксамид(9) (Рис.15) и N-этил-N-фенил-1-фенилпирроло[1,2-a]пиразин-3-карбоксамид (10) (Рис.16) подходят под фармакофорную модель и могут потенциально являться инновационными анксиолитиками.
Рис.15 Рис.16
Синтез
Исходя из доступных реагентов и методик синтеза фенил замещенных пирролпиразинов, был выбран метод получения гетероароматического цикла из реакции пирролфенилкетона с 2-азидоакриламидами. Нами предложен план синтеза (Схема 3.1).
Схема 3.1
Альтернативный способ получения 1-фенилпирроло[1,2-a]пиразин-3-карбоксамидов заключается в получении 1-фенилпиролло[1,2-a]пиразин-3-карбоновой кислоты и последующем синтезе различных амидов (Схема 3.2)
Схема 3.2
