Химическая связь в координационных соединениях
Метод валентных связей
Применительно к координационным соединениям метод валентных связей утверждает, что между центральным атомом и лигандами реализуются связи, образованные по донорно-акцепторному механизму. Такая связь называется координационной. Обычно донором электронной пары при образовании координационной связи выступает лиганд, а акцептором - центральный атом. В этом случае формирование s-связи происходит по схеме М:L. Упрочнению связи способствует соответствующая гибридизация электронных орбиталей центрального атома. Например, при образовании тетрафторобериллат-иона по уравнению:
Be2+ + 4F- = [BeF4]2-
в роли акцептора выступает катион бериллия с электронной конфигурацией 1s22s02p0 . Четыре вакантные орбитали валентного уровня подвергаются sp3-гибридизации. В качестве доноров выступают фторид-анионы, имеющие неподеленные электронные пары.
sp3-гибридизация
¾¾¾¾¾¾¾¾¾¾¾®
| 2s | 2p | |||
| ¯ | ¯ | ¯ | ¯ |
¾¾¾¾¾¾¾¾¾¾¾®
электронные пары лигандов (F-)
Связь в координационном соединении может формироваться также за счет неподеленной электронной пары центрального атома и вакантных орбиталей лиганда по следующей схеме:

Такая разновидность связи называется p-дативной. Образование дативных связей упрочняет молекулу, так как способствует перетеканию электронной плотности с центрального атома на лиганд и повышению эффективного заряда центрального атома.
В зависимости от того, какие d-орбитали ЦА участвуют в гибридизации, последняя может быть внутренней или внешней.
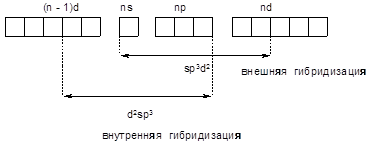
Рассмотрим образование диамагнитного комплекса [Co(NH3)6]3+. В диамагнитных комплексах лиганды должны вызывать спаривание электронов; освободившиеся d-орбитали используются для образования связи. Таким образом, в данном комплексном катионе реализуется внутренняя гибридизация типа d2sp3, а гибридные орбитали заполняются электронными парами лигандов.
Электронная конфигурация Со3+:
| 3d6 | 4s | 4p | ||||||||
| ¯ | | | | | ||||||
| ¯ | ¯ | ¯ | ||||||||
| ¯ | ¯ | ¯ | ¯ | ¯ | ¯ |
¾¾¾¾¾¾¾¾¾¾¾¾®
электронные пары лигандов (NH3)
Однако не все комплексы кобальта(III) диамагнитны; так анион [CoF6]3- - парамагнитен. Метод валентных связей допускает в этом случае участие в гибридизации внешних 4d-орбиталей центрального атома (sp3d2-гибридизация).
| 3d6 | 4s | 4p | 4d | |||||||||||||
| ¯ | | | | | ||||||||||||
| ¯ | ¯ | ¯ | ¯ | ¯ | ¯ |
¾¾¾¾¾¾¾¾¾¾¾®
электронные пары лигандов (F-)
Из рассмотренных типов гибридизации энергетически наиболее выгодной является внутренняя гибридизация, так как в этом случае в гибридизацию вовлекаются (n-1)d-орбитали, энергия которых ниже энергии nd-орбиталей.
Тип гибридизации центрального атома связан с координационным числом и определяет геометрическую форму координационного полиэдра. Наиболее часто встречающиеся формы координационного многогранника и соответствующие им типы гибридизации приведены в табл. 10.
Таблица 10.
Геометрия координационного полиэдра
| КЧ | Тип гибридизации | Геометрия Полиэдра | Примеры |
| sp | Линейная | [Ag(NH3)2]+ | |
| sp3 | Тетраэдрическая | [Zn(NH3)4]2+ | |
| d3s | [MnCl4]2- | ||
| dsp2 | Квадратная | [AuCl4]- | |
| d2sp3 | Октаэдрическая | [Fe(CN)6]3- | |
| sp3d2 | [Ni(NH3)6]2+ |
В рамках метода ВС можно предсказать геометрию координационного полиэдра, если известны магнитные свойства соединения. Например, катион никеля(II) имеет электронную конфигурацию 3d8. Для парамагнитных комплексов никеля(II) с координационным числом 4, например для [NiCl4]2-, все 3d-орбитали должны быть заняты электронами. Электронные пары лигандов разместятся на sp3-гибридных орбиталях, поэтому геометрия комплексов – тетраэдрическая.
Электронная конфигурация Ni2+
| 3d8 | 4s | 4p | ||||||||
| ¯ | ¯ | ¯ | | | ||||||
| ¯ | ¯ | ¯ | ¯ |
¾¾¾¾¾¾®
электронные пары лигандов (Cl-)
В тоже время диамагнитный цианидный комплекс [Ni(CN)4]2- имеет плоскоквадратное строение. Этот факт объясняется в рамках метода валентных связей тем, что в результате спаривания электронов Ni2+ освобождается d-орбиталь и реализуется гибридизация типа dsp2.
| 3d8 | 4s | 4p | ||||||||
| ¯ | ¯ | ¯ | ¯ | |||||||
| ¯ | ¯ | ¯ | ¯ |
¾¾¾¾¾¾¾¾®
электронные пары лигандов (СN-)
Качественные оценки, получаемые на основе метода валентных связей, широко используются в современной координационной химии. Однако МВС имеет ряд ограничений, главное из которых заключается в подчиненности метода экспериментальным данным, т.е. в низкой предсказательной способности.
