Распределительная хроматография
Распределительная хроматография является разновидностью жидкостной (жидко-жидкофазной) хроматографии. Она основана на различии в распределении веществ между несмешивающимися жидкими фазами - подвижной и неподвижной, нанесённой на твёрдый носитель (обычно носителем являются нерастворимые в используемом растворителе органические вещества, в том числе полимерные). Подвижной фазой служат растворы разделяемых компонентов в чистых растворителях или в их смесях. Обязательным условием является взаимная нерастворимость жидкостей, являющихся неподвижной и подвижной фазами. Растворитель подбирается в соответствии со временем удерживания компонентов.
Разделение компонентов смеси происходит в соответствии с их нернстовским коэффициентом распределенияК:
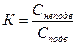 ,
,
где Снеподв и Сподв – концентрации подвергающегося разделению компонента соответственно в неподвижной и в подвижной фазе.
Чем больше значение К, тем ранее задерживается компонент в колонке и тем прочнее удерживается в ней.
Разновидностью распределительной хроматографии является экстракционная жидкостная хроматография,в которой неподвижной фазой служит органический экстрагент, нанесённый на твёрдый носитель, а подвижной – водный раствор веществ, подлежащих разделению. Как правило, с помощью распределительной и экстракционной хроматографии разделяют достаточно концентрированные растворы неорганических веществ, например, солей редкоземельных элементов, соединений актиноидов, в том числе и радиоактивных элементов при переработке отработанного горючего атомных электростанций, солей щелочных металлов и др.
Аффинная хроматография
Этот вид хроматографии основан на образовании компонентами разделяемой смеси со специфическими лигандными группами неподвижной фазы более или менее прочных связей, чаще всего, координационных. Обычно аффинная хроматография используется в биохимии и в биотехнологии для разделения биологически активных веществ. Поэтому в качестве лигандов (или, иначе, аффинантов) используют вещества с соответствующей биологической функцией, например, антитела при разделении белков, коферменты или ингибиторы – ферментов, рецепторы – токсинов и т. п.
Эксклюзионная хроматография
Разделение в этом случае основано на том, что молекулы или ионы различных размеров по-разному задерживаются порами сорбентами, которые имеют одинаковые или почти одинаковые диаметры. Сорбент при этом играет роль сита или фильтра и разделение молекул по размерам напоминает отсеивание крупных частиц (или, соответственно, фильтрацию). Наиболее мелкие молекулы глубоко проникают в поры и удерживаются там достаточно длительное время, средние – более короткое время, а большие молекулы, чьи размеры превышают размеры пор, вообще не удерживаются сорбентом.
В качестве сорбентов применяются т. н. «молекулярные сита», природные минералы группы цеолитов, содержащие поры молекулярных размеров со строго определённым диаметром, или синтетические материалы с подобной структурой. В частности, молекулярными ситами могут служить некоторые гели (лиогели или ксерогели; см. п. 11.1). Поэтому эксклюзионная хроматография иначе называется гель-проникающейили ситовой хроматографией, или гель-фильтрацией.
Ионообменная хроматография
Это разновидность жидкостной хроматографии, основанная на различной способности разделяемых ионов к ионному обмену с ионами, находящимися на поверхности сорбента. Разделение катионов проводят на катионитах (элюент – раствор кислоты), анионов – на анионитах (элюент – раствор щёлочи). Разделение ионов регулируется подбором оптимального значения рН элюента или введением нейтральных электролитов. В этом случае время удерживания будет зависеть ещё и от конкурентного взаимодействия с ионитом исследуемых ионов и ионов этого электролита (например, NaNO3). Возможно применение к элюентам и других добавок. Детектирование в ионообменной хроматографии можно осуществлять любыми пригодными для этих целей методами. Но наиболее приемлемо детектирование с помощью кондуктометра, на чём основан вариант, называемый ионной хроматографией.
Ионообменная хроматография подчиняется всем закономерностям ионообменной адсорбции, а именно: многозарядные ионы удерживаются ионитом сильнее (т. е. у них время удерживания больше), чем однозарядные, а при равных зарядах время удерживания уменьшается с ростом радиуса гидратированного иона.
Ионообменная хроматография применяется в самых различных областях химии, биохимии, биологии, а также в медицине. Так, с её помощью разделяются ионы самых различных металлов, причём даже такие, разделить которые другими методами бывает затруднительно, например, ионы гафния и циркония, молибдена и вольфрама, тантала и ниобия, ионы щелочных и щёлочноземельных металлов, лантаноидов, актиноидов. Высокая эффективность ионообменной хроматографии делает её незаменимой при диагностике ряда заболеваний, так как позволяет анализировать сложные смеси аминокислот, белков, нуклеиновых кислот, нуклеотидов, нуклеозидов, пуриновых и пиримидиновых оснований и др. в биологических жидкостях. В биохимии используется и препаративная ионообменная хроматография, в частности для выделения антибиотиков и алкалоидов.
Хроматография на бумаге
Хроматография на бумаге или бумажная хроматография является разновидностью жидкостной плоскослойной хроматографии. Под этим названием объединяются различные по механизму разделения виды хроматографии, общим для которых является то, что носителем служит бумага. Для бумажной хроматографии используют специально подготовленную т. н. хроматографическую бумагу с равномерной толщиной и плотностью волокон по всей ширине листа.
Методики хроматографирования, проявления хроматограмм и анализа зон в бумажной хроматографии близки к методикам тонкослойной, но возможности бумажной шире, так как бумаге можно придавать любую форму, удобную для технического осуществления элюирования компонентов. Хроматографию на бумаге можно проводить по радиальной, восходящей или нисходящей методике, в условиях градиента температуры и с применением других приёмов, позволяющих повысить эффективность и скорость разделения. Большим преимуществом данного метода является то, что бумага для отделения друг от друга и раздельного анализа хроматографических зон легко разрезается на части, а также может быть сожжена (при анализе неорганических веществ), подвергнута кипячению в свёрнутом виде и т. п.
Различают адсорбционную, ионообменную, распределительную и осадочную бумажную хроматографию. Механизм разделения веществ в первых трёх разновидностях, по существу, не отличается от описанных выше. Остановимся подробнее на осадочной хроматографии.
Осадочная хроматография
Осадочная хроматографияоснована на различной растворимости осадков, образующихся при взаимодействии веществ анализируемой смеси с реагентом-осадителем, который предварительно вводят в состав бумаги пропиткой в его растворе. (В принципе в качестве носителя можно использовать не только бумагу, но и другие высокодисперсные сорбенты). Хроматограммы образуются в результате многократного образования и растворения осадков: менее растворимые соединения закрепляются в начале слоя сорбента, более растворимые - в конце. Таким образом, скорость движения пятна осадка по хроматограмме зависит от его произведения растворимости. Одним из преимуществ осадочной хроматографии является то, что плотность осадка, образуемого каждым данным компонентом, равномерна по высоте зоны, имеющей четкую нижнюю границу.
Однако осадочная хроматография имеет ограничения, так как может быть использована для анализа преимущественно неорганических соединений, главным образом для анализа анионов.
