Характеристика трёх структур белковых молекул
| Структура белковой молекулы | Характеристика структуры | Тип связи, определяющий структуру | Графическое изображение |
| Первичная – линейная | Порядок чередования аминокислот в полипептидной цепи – линейная структура | Пептидная связь -NH – CO - | ––––––––––– |
| Вторичная - спиралевидная | Закручивание полипептидной линейной цепи в спираль – спиралевидная структура | Внутримолекулярные водородные связи | 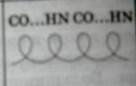 |
| Третичная - глобулярная | Упаковка вторичной спирали в клубок – клубочковидная структура | Дисульфидные и ионные связи |  |
Вторичной структурой обладает большая часть белков, правда, не всегда на всём протяжении полипептидной цепи.
Вторичная структура белков 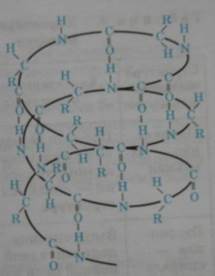
Полипептидные цепочки с определённой вторичной структурой могут быть по-разному расположены в пространстве. Это пространственное расположение получило название третичной структуры.
Третичная структура белков Четвертичная структура белков

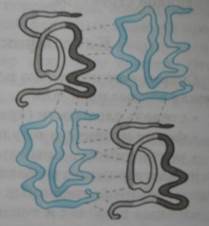
В формировании третичной структуры. Кроме водородных связей, большую роль играет ионное и гидрофобное взаимодействие. По характеру « упаковки» белковой молекулы различают глобулярные, или шаровидные, и фибриллярные, или нитевидные, белки.
Для глобулярных белков характерна ᾴ - спиральная структура, спирали изогнуты, «свёрнуты». Макромолекула имеет сферическую форму. Они растворяются в воде и солевых растворах с образованием коллоидных систем. Большинство белков животных, растений и микроорганизмов относится к глобулярным белкам.
Для фибриллярных белков более характерна нитевидная структура. Они, как правило, не растворяются в воде. Фибриллярные белки обычно выполняют структурообразующие функции. Их свойства (прочность, способность растягиваться) зависят от способа упаковки полипептидных цепочек. Примером фибриллярных белков служат белки мускульной ткани (миозин), кератин (роговая ткань). В ряде случаев отдельные субъединицы белка с помощью водородных связей, электростатического и других взаимодействий образуют сложные ансамбли. В этом случае образуется четвертичнаяструктура белков.
В организации более высоких структур белка исключительная роль принадлежит первичной структуре.
Классификация
Существует несколько классификаций белков. В их основе лежат разные признаки:
Ø степень сложности (простые и сложные0;
Ø форма молекул 9глобулярные и фибриллярные белки);
Ø растворимость в отдельных растворителях (водорастворимые, растворимые в отдельных солевых растворах – альбумины, спирторастворимые – проламины, растворимые в разбавленных щелочах и кислотах – глутелины);
Ø выполняемая функция (например, запасные белки, скелетные и т.п.).
Свойства.
Белки – амфотерные электролиты. При определённом значении рН среды (она называется изоэлектрической точкой) число положительных и отрицательных зарядов в молекуле белка одинаково. Это одно из основных свойств белка. Белки в этой точке электронейтральны, а их растворимость в воде наименьшая. Способность белков снижать растворимость при достижении электронейтральности их молекул используется для выделения их из растворов, например, в технологии получения белковых продуктов.
Гидратация.
Процесс гидратации означает связывание белками воды, при этом они проявляют гидрофильные свойства: набухают, их масса и объём увеличиваются. Набухание белка сопровождается его частичным растворением. Гидрофильность отдельных белков зависит от их строения. Имеющиеся в составе и расположенные на поверхности белковой макромолекулы гидрофильные амидные, аминные и карбоксильные группы притягивают к себе молекулы воды, строго ориентируя их на поверхности молекулы. Окружающая белковые глобулы гидратная оболочка препятствует агрегации и осаждению, а следовательно, способствует устойчивости растворов белка. В изоэлектрической точке белки обладают наименьшей способностью связывать воду, происходит разрушение гидратной оболочки вокруг белковых молекул, поэтому они соединяются, образуя крупные агрегаты. Агрегация белковых молекул происходит и при их обезвоживании с помощью некоторых органических растворителей, например этилового спирта. Это приводит к выпадению белков в осадок. При изменении рН среды макромолекула белка становится заряженной, и его гидратационная способность меняется.
При ограниченном набухании концентрированные белковые растворы образуют сложные системы, называемые студнями. Студни не текучи, упруги, обладают пластичностью, определённой механической прочностью, способны сохранять свою форму. Глобулярные белки могут полностью гидратироваться, растворяясь в воде (например, белки молока), образуя растворы с невысокой концентрацией. Гидрофильные свойства белков, т.е. их способность набухать, образовывать студни, стабилизировать суспензии, эмульсии и пены, имеют большое значение в биологии и пищевой промышленности. Очень подвижным студнем, построенным в основном из молекул белка, является цитоплазма – полужидкое содержимое клетки. Сильно гидратированный студень – сырая клейковина, выделенная из пшеничного теста, она содержит до 65% воды. Различная гидрофильность клейковинных белков – один из признаков, характеризующих качество зерна пшеницы и получаемой из него муки. Гидрофильность белков зерна и муки играет большую роль при хранении и переработке зерна, в хлебопечении. Тесто, которое получают в хлебопекарном производстве, представляет собой набухший в воде белок, концентрированный студень, содержащий зёрна крахмала.
Денатурация белков.
При денатурации под влиянием внешних факторов (температуры, механического воздействия, действия химических агентов и ряда других факторов) происходит изменение вторичной, третичной и четвертичной структур белковой макромолекулы, т.е. её пространственной структуры. Первичная структура, а следовательно, и химический состав белка не меняются. Изменяются физические свойства: снижается растворимость, способность к гидратации, теряется биологическая активность. Меняется форма белковой макромолекулы, происходит агрегирование. В тоже время увеличивается активность некоторых химических групп, облегчается воздействие на белки протеолитических ферментов, а следовательно, он легче гидролизуется.
В пищевой технологии особое практическое значение имеет тепловая денатурация белков, степень которой зависит от температуры, продолжительности нагрева и влажности. Это необходимо помнить при разработке режимов термообработки пищевого сырья, полуфабрикатов, а иногда и готовых продуктов. Особую роль процессы тепловой денатурации играют при бланшировании растительного сырья, сушке зерна, выпечке хлеба, получении макаронных изделий. Денатурация белков может вызываться и механическим воздействием (давлением, растиранием, встряхиванием, ультразвуком). Наконец, к денатурации белков приводит действие химических реагентов (кислот, щелочей, спирта, ацетона).Все эти приёмы широко используются в пищевой и биотехнологии.
Пенообразование
Под процессом пенообразования понимают способность белков образовывать высококонцентрированные системы «жидкость-газ», называемые пенами. Устойчивость пены, в которой белок является пенообразователем, зависит не только от его природы и от концентрации, но и от температуры. Белки в качестве пенообразователей широко используются в кондитерской промышленности (пастила, зефир, суфле). Структуру пены имеет хлеб, а это влияет на его вкусовые свойства.
Молекулы белков под влиянием ряда факторов могут разрушаться или вступать во взаимодействие с другими веществами с образованием новых продуктов. Для пищевой промышленности можно выделить два очень важных процесса: 1) гидролиз белков под действием ферментов и 2) взаимодействие аминогрупп белков или аминокислот с карбонильными группами восстанавливающих сахаров. Под влиянием протеаз – ферментов, катализирующих гидролитическое расщепление белков, последние распадаются на более простые продукты (поли- и дипептиды) и в конечном итоге на аминокислоты. Скорость гидролиза белка зависит от его состава, молекулярной структуры, активности фермента и условий.
Гидролиз белков
Реакцию гидролиза с образованием аминокислот в общем виде можно записать так:
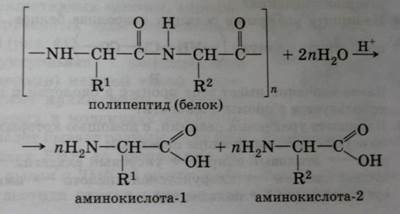
Горение
Белки горят с образованием азота, углекислого газа и воды, а также некоторых других веществ. Горение сопровождается характерным запахом жжёных перьев.
Цветные реакции
Используют следующие реакции:
· ксантопротеиновую, при которой происходит взаимодействие ароматических гетероароматических циклов в молекуле белка с концентрированной азотной кислотой, сопровождающееся появлением желтой окраски;
· биуретовую, при которой происходит взаимодействие слабощелочных растворов белков с раствором сульфата меди (II) с образованием комплексных соединений между ионами меди и полипептидами. Реакция сопровождается появлением фиолетово-синей окраски.
Пищевая ценность белков.
Белок – наиболее важный компонент пищи человека. Основные источники пищевого белка: мясо, молоко, рыба, продукты переработки зерна, хлеб, овощи.
Потребность человека в белке зависит от его возраста, пола. Характера трудовой деятельности. В организме здорового взрослого человека должен быть баланс между количеством поступающих белков и выделяющимися продуктами распада. Для оценки белкового обмена введено понятие азотного баланса. В зрелом возрасте у здорового человека существует азотное равновесие, т.е. количество азота, полученного с белками пищи, равно количеству выделяемого азота. В молодом растущем организме идёт накопление белковой массы, образуется ряд нужных для организма соединений, поэтому азотный баланс будет положительным – количество поступающего азота с пищей превышает количество выводимого из организма. У людей пожилого возраста, а также при некоторых заболеваниях, , недостатке в рационе питания белков, незаменимых аминокислот, витаминов, минеральных веществ наблюдается отрицательный азотный баланс – количество выделенного из организма азота превышает его поступление в организм. Длительный отрицательный азотный баланс ведёт к гибели организма. На белковый обмен влияют биологическая ценность и количество поступающего с пищей белка.
Биологическая ценность белков определяется сбалансированностью аминокислотного состава и атакуемостью белков ферментами пищеварительного тракта.
В организме человека белки расщепляются до аминокислот, часть из них 9заменимые) являются строительным материалом для создания новых аминокислот, однако имеется 8 аминокислот (незаменимые), которые не образуются в организме взрослого человека, они должны поступать с пищей. Снабжение организма человека необходимым количеством аминокислот – основная функция белка в питании. В белке пищи должен быть сбалансирован не только состав незаменимых аминокислот, но и должно быть определённое соотношение незаменимых и заменимых аминокислот, в противном случае часть незаменимых будет расходоваться не по назначению.
Наиболее близки к «незаменимому» белку животные белки. Большинство растительных белков содержат недостаточное количество незаменимых аминокислот (одной или нескольких).
В то же время необходимо помнить. Что некоторые аминокислоты при тепловой обработке, длительном хранении продуктов могут образовать не усвояемые организмом соединения, т.е. становиться «недоступными». Это снижает ценность белка.
Биологическая ценность белков может быть увеличена добавлением лимитирующей аминокислоты или внесением компонента с её повышенным содержанием.
Животные и растительные белки усваиваются организмом неодинаково. На степень усвоения организмом белков оказывает влияние технология получения пищевых продуктов и их кулинарная обработка. В большинстве пищевых производств при соблюдении технологии не происходит деструкции аминокислот. При умеренном нагревании пищевых продуктов усвояемость белков несколько возрастает (частичная денатурация белков облегчает доступ протеаз к пептидным связям). При интенсивной тепловой обработке усвояемость снижается.
Суточная потребность взрослого человека в белке разного вида 1 – 1,5 г белка на 1кг массы тела (детей 4 – 1,5г). Доля животных белков должна составлять приблизительно 55% от общего его количества в рационе.
Для повышения пищевой ценности продуктов питания необходимо увеличение доли белкового компонента, сбалансированности его аминокислотного состава. Один из путей решения этой задачи – получение белковых продуктов из белоксодержащих отходов пищевых производств, например семя масличных после удаления масла, отходов мясной и молочной промышленности, и их использование для улучшения биологической ценности существующих продуктов или создание новых продуктов питания.
Нуклеиновые кислоты
Название этих веществ происходит от латинского слова nuleus – ядро и указывает, что нуклеиновые кислоты являются составной частью клеточных ядер. Нуклеиновые кислоты – высокомолекулярные соединения с молекулярными массами от 200 до нескольких миллионов. Нуклеиновые кислоты обнаружены во всех растительных и животных клетках, вирусах, бактериях и грибах.
Различают два вида нуклеиновых кислот – дезоксирибонуклеиновые (ДНК) и рибонуклеиновые (РНК). Различие в названии объясняется тем, что молекула ДНК содержит моносахарид дезоксирибозу, а РНК – рибоза. В настоящее время известно большое число разновидностей ДНК и РНК, отличающихся друг от друга по строению и значению в обмене веществ. Они являются исключительно важными элементами клетки, обеспечивающими хранение и передачу генетической (наследственной) информации в живых организмах. ДНК находится преимущественно в хромосомах клеточного ядра (99% всей ДНК клетки), а также в митохондриях и хлоропластах. РНК входит в состав ядрышек, рибосом, минохондрий, пластид, цитоплазмы. Молекула ДНК состоит из двух полинуклеотидных цепочек, спирально закрученных одна относительно другой.
Структура молекулы ДНК
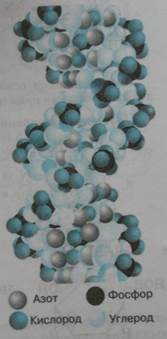
Структурными компонентами (мономерами) каждой такой цепочки служат нуклеотиды, количество которых в молекулах нуклеиновых кислот бывает разным – от 80 в молекулах РНК до нескольких десятков тысяч в ДНК. В состав любого нуклеотида входит одно из азотистых оснований – аденин, гуанин, цитозин и тимин. Нуклеиновые кислоты, как и белки, имеют первичную, вторичную и третичную структуру.
ДНК является основным строительным материалом генов, в которых хранится наследственная информация организма. РНК выполняет различные функции, так как существует в виде трёх разновидностей: рибосомальная, транспортная и информационная.
Контрольные вопросы.
1. Почему аминокислоты являются гетерофункциональными соединениями?
2. Какими особенностями строения должны обладать аминокислоты, используемые для синтеза волокон, и аминокислоты, участвующие в биосинтезе белков в клетках живых организмов?
3. Чем отличаются реакции поликонденсации от реакций полимеризации? В чём их сходство?
4. Охарактеризуйте строение белков. Какую роль играют различные виды химических связей в формировании различных структур белковых молекул?
5. Как соотносятся между собой понятия «пептид», «полипептид», «полиамид», «белок»?
6. Охарактеризуйте важнейшие физические и химические свойства белков.
7. С помощью каких реакций можно распознать белки?
8. Какую роль играют белки в жизни организмов?
9. В чём заключается пищевая ценность белков?
10. Дайте характеристику нуклеиновым кислотам.
Практические задания
1. Запишите уравнения реакций аминопропионовой кислоты с серной кислотой и гидроксидом натрия, а также с метиловым спиртом. Всем веществам дайте названия по систематической номенклатуре.
2. Как получают аминокислоты? Запишите уравнения реакций получения аминопропионовой кислоты из пропана.
3. Напишите уравнения реакций, с помощью которых можно осуществить следующие переходы: этан → этиловый спирт → уксусный альдегид → уксусная кислота → хлоруксусная кислота → аминоуксусная кислота → полипептид
Тема 3. «Углеводы»
План
1. Углеводы, их классификация и значение.
2. Моносахириды. Гексозы. Глюкоза.
3. Полисахариды. Крахмал и целлюлоза.
4. Превращения углеводов в технологических процессах.
5. Пищевая ценность углеводов.
1.Углеводы – органические вещества, молекулы которых состоят из атомов углерода, водорода и кислорода, причём водород и кислород находятся в них, как правило, в таком же соотношении, как и в молекуле воды (2/1).
Общая формула углеводов – Сn (Н2О)m, т.е. они как бы состоят из углерода и воды, отсюда и название класса, которое имеет исторические корни. В дальнейшем было установлено, что имеются углеводы, в молекулах которых не соблюдается указанное соотношение, например дезоксирибоза – С5Н10О4. Известны также органические соединения, состав которых соответствует приведённой общей формуле, но которые не принадлежат к классу углеводов. К ним относятся, например, формальдегид СН2О и уксусная кислота СН3СООН.
Углеводы по их способности гидролизоваться можно разделить на три основные группы: моно-, ди- и полисахариды.
Моносахариды – углеводы, которые не гидролизуются (не разлагаются водой). В свою очередь, в зависимости от числа атомов углерода моносахариды подразделяются на триозы (молекулы которых содержат три углеродных атома), тетрозы, пентозы, гексозы и т.д.
В природе моносахариды представлены преимущественно пентозами и гексозами.
К пентозам относятся, например рибоза – С5Н10О5 и дезоксирибоза – С5Н10О4.
К гексозам, имеющим общую молекулярную формулу С6Н12О6, относятся, например, глюкоза, фруктоза, галактоза.
Дисахариды – углеводы, которые гидролизуются с образованием двух молекул моносахаридов. Общая формула – С12Н22О11. Общее уравнение гидролиза:
С12Н22О11 + Н2О → 2С6Н12О6
дисахарид гексоза
К дисахаридам относятся:
· сахароза (обычный пищевой сахар), который при гидролизе образует одну молекулу глюкозы и молекулу фруктозы. Она содержится в большом количестве в сахарной свекле, сахарном тростнике, клёне, сахарной пальме, кукурузе и т.д.
· мальтоза (солодовый сахар), которая гидролизуется с образованием двух молекул глюкозы. Мальтозу можно получить при гидролизе крахмала под действием ферментов, содержащихся в солоде, - пророщенных, высушенных и размолотых зёрнах ячменя;
· лактоза (молочный сахар), которая гидролизуется с образованием молекулы глюкозы и галактозы. Она содержится в молоке млекопитающих животных (до 4-6%) обладает невысокой сладостью и используется как наполнитель в драже и аптечных таблетках.
Сладкий вкус разных моно- и дисахаридов различен. Так, самый сладкий моносахарид – фруктоза – в полтора раза слаще глюкозы, которую принимают за эталон. Сахароза в 2 раза слаще глюкозы и в 4-5 раз – лактозы, которая почти безвкусна.
Полисахариды – крахмал, гликоген, декстрины, целлюлоза и т.д. – углеводы, которые гидролизуются с образованием множества молекул моносахаридов, чаще всего глюкозы. Общая формула полисахаридов – (С6Н10О5)n.
Роль углеводов в природе и их значение для жизни человека чрезвычайно велики. Образуясь в клетках растений в результате фотосинтеза, они выступают источником энергии для клеток животных. В первую очередь это относится к глюкозе.
Многие углеводы (крахмал, гликоген, сахароза) выполняют запасающую функцию, роль резерва питательных веществ.
Кислоты РНК и ДНК, в состав которых входят некоторые углеводы, выполняют функцию передачи наследственной информации.
Целлюлоза – строительный материал растительных клеток – играет роль каркаса для оболочек этих клеток. Другой полисахарид – хитин – выполняет аналогичную роль в клетках некоторых животных – образует наружный скелет членистоногих (ракообразных), насекомых, паукообразных.
Углеводы служат в конечном итоге источником нашего питания: мы потребляем зерно, содержащее крахмал, или скармливаем его животным, в организме которых крахмал превращается в белки и жиры. Самая гигиеническая наша одежда сделана из целлюлозы или продуктов на её основе: хлопка и льна, вискозного волокна, ацетатного шёлка. Деревянные дома и мебель построены из той же целлюлозы, образующей древесину. В основе производства фото- и киноплёнки всё та же целлюлоза. Книги, газеты, письма, денежные банкноты – всё это продукция целлюлозно-бумажной промышленности. Значит, углеводы обеспечивают нас всем необходимым для жизни: пищей, одеждой, кровом.
Кроме того, углеводы участвуют в построении сложных белков, ферментов, гормонов. Углеводами являются и такие жизненно необходимые вещества, как гепарин (он играет важнейшую роль – предотвращает свёртывание крови), агар-агар (его получают из морских водорослей и применяют в микробиологической и кондитерской промышленности – вспомните знаменитый торт «Птичье молоко»).
Необходимо подчеркнуть, что единственным источником энергии на Земле (помимо ядерной) является энергия Солнца, а единственным способом его аккумулирования для обеспечения жизнедеятельности всех живых организмов является процесс фотосинтеза, превращающий в клетках живых растений и приводящий к синтезу углеводов из воды и углекислого газа. Именно при этом превращении образуется кислород, без которого жизнь на нашей планете была бы невозможна.
