Восстановительным аминированием a-кетонокислот

Поскольку получаемые перечисленными выше способами синтетические аминокислоты представляют собой рацемические смеси, то в промышленности для выделения чистых энантиомеров широко используют препаративное разделение на специальных носителях ферментов.
Кроме синтетических способов в настоящее время широко внедряются биотехнологические приёмы и методы, в основе которых лежат биологические процессы с использованием ферментов или микроорганизмов, избирательно расщепляющих или трансформирующих один конкретный энантиомер.
На основе крахмала и других углеводсодержащих сырьевых источников налажено производство очень многих аминокислот, в том числе и незаменимых.
b-Аминокислоты можно получить взаимодействием a,b-непредельных карбоновых кислот (или их эфиров) с аммиаком. Присоединение всегда происходит по b-положению:
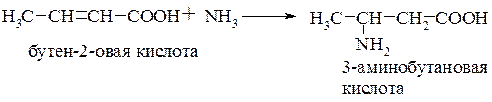
В.М. Родионов (1926 г.) предложил более удобный метод осуществления этой реакции, заключающийся в том, что получение непредельной кислоты и присоединение аммиака происходит в одну стадию. Альдегид конденсируется с малоновой кислотой в присутствии ацетата аммония в растворе уксусной кислоты:
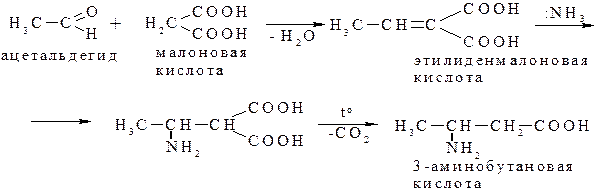
Получение ароматических аминокислот.
Для получения аминобензойных кислот удобно пользоваться нитробензойными кислотами. В случае орто- и пара-изомеров следует исходить из толуола, а мета-изомера – из самой бензойной кислоты:

Для получения о-аминобензойных кислот удобно использовать реакцию расщепления имидов о-дикарбоновых кислот под действием гипобромитов (расщепление по Гофману, разд.17.4.2. ):
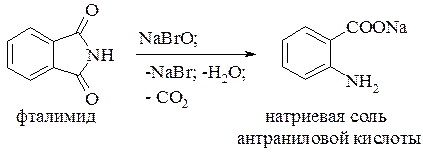
Физические свойства
Аминокислоты представляют собой бесцветные кристаллические вещества, большинство из которых легко растворимы в воде, хуже в спирте и нерастворимы в эфире и хлороформе.
Относящиеся к L-стереохимическому ряду аминокислоты имеют сладкий вкус, а D-ряда – безвкусны.
Для аминокислот характерны высокие температуры плавления (с разложением). Это объясняется тем, что они существуют в виде внутренних солей, которые характеризуются ионизированной, диполярнойструктурой, что подтверждается рентгеноструктурным анализом:

Химические свойства
В молекуле аминокислоты содержатся одновременно две функциональные группы, обладающие кислотными (карбоксил) и основными (аминогруппа) свойствами. По этой причине они претерпевают внутримолекулярное протонирование с образованием внутренней соли, называемой бетаином, или цвиттер-ионом.
Это взаимодействие тем сильнее, чем ближе друг к другу расположены карбокси- и аминогруппы. Наиболее прочные внутренние соли образуются у a-аминокислот. Чем дальше от карбоксила отстоит аминогруппа, тем слабее протонирование, тем меньше доля протонированной формы.
Будучи амфотерными, аминокислоты способны нейтрализовать незначительные количества других кислот или оснований, проявляя тем самым буферные свойства. Значение рН-раствора, при котором положительный и отрицательный заряды в молекуле аминокислоты точно компенсируют друг друга, называется изоэлектрической точкой (табл. 21.1).
В сильнокислой среде на атоме азота преобладает положительный заряд, а в сильнощелочной среде преобладает отрицательный заряд на карбоксилат – анионе. В обоих случаях заряды не скомпенсированы:
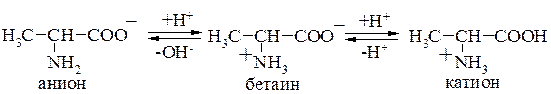
Бетаин является слабой NH-кислотой. Имеется определенное значение рН, при котором содержание бетаина наибольшее, что соответствует изоэлектрической точке (символ рНi). Для моноаминокарбоновых кислот рНi ~ 6,1.
