Реакции нуклеофильного замещения
Образование сложных эфиров
Анализ строения карбоксилат-аниона говорит о том, что в нём отрицательный заряд распределён равномерно на участке О–С–О, поэтому карбонильной группы в карбоксилат-анионе практически нет.
Многие нуклеофилы, будучи также основаниями (аммиак, гидроксиламин и др.), взаимодействуют с карбоновыми кислотами, но только с образованием солей.
Чтобы осуществить нуклеофильное замещение при атоме углерода карбоксильной группы и исключить образование карбоксилат-аниона, следует использовать нуклеофилы, обладающие слабыми основными свойствами. Одновременно с этим необходимо активировать карбонильную группу в карбоксиле, что можно достичь её протонированием:
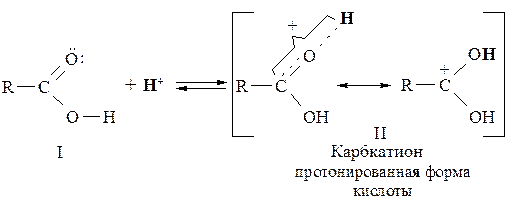
Образование карбкатиона происходит за счёт присоединения протона (кислая среда) к карбонильному кислороду, чья нуклеофильность выше, чем у атома кислорода гидроксильной группы. Это объясняется тем, что неподелённая электронная пара кислорода ОН–группы участвует в р,π-сопряжении с карбоксильной группой.
Углерод карбоксильной группы исходной кислоты характеризуется более слабыми электрофильными свойствами, чем атом углерода в сформировавшемся карбкатионе. По этой причине карбокатион может присоединить такой слабый нуклеофил, как спирт.
После присоединения спирта формируется катион, в котором положительный заряд сосредоточен на атоме кислорода (интермедиат III). Далее интермедиат III переходит в катион IV, который отщепляет воду и протон (катализатор) с образованием конечного продукта – сложного эфира:


В приведённом механизме образования сложного эфира – реакции этерификации – присоединившийся к карбонильному кислороду протон (кислотный катализатор) выделен жирным шрифтом.
С помощью изотопного метода было установлено, что при образовании сложного эфира из карбоновой кислоты и спирта, содержащего изотоп 188О, вода образуется за счёт гидроксила карбоксила и водорода OH–группы спирта:

Образование галогенангидридов кислот
Получение галогенангидридов, называемых иначе ацилгалогенидами, осуществляется взаимодействием карбоновых кислот с трихлоридом фосфора – PCl3, пентахлоридом фосфора – PCl5, тионилхлоридом – SOCl2 и трибромидом фосфора – PBr3.
Реакция карбоновых кислот с перечисленными реагентами происходит через последовательные стадии, первой из которых является образование смешанного ангидрида, а во второй стадии происходит нуклеофильное замещение у атома углерода карбоксигруппы под действием хлорид-иона:
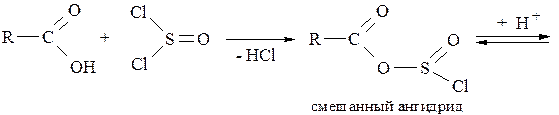

Образование ангидридов кислот
В присутствии сильных водоотнимающих средств, таких, как Р2О5, из карбоновых кислот получают ангидриды кислот:

Ангидриды карбоновых кислот можно получать и взаимодействием солей карбоновых кислот с хлорангидридами. Это позволяет использовать разные карбоновые кислоты, благодаря чему возможно образование так называемых смешанных ангидридов, т.е. ангидридов двух разных кислот:
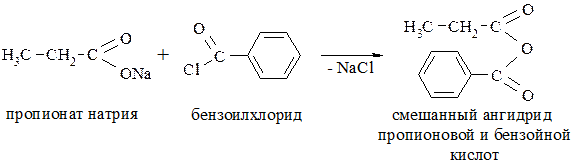
Образование амидов кислот
По сравнению со спиртами аммиак является более сильным нуклеофилом, что позволяет получить амиды кислот путём непосредственного замещения ОН–группы при достаточно жёстких условиях:
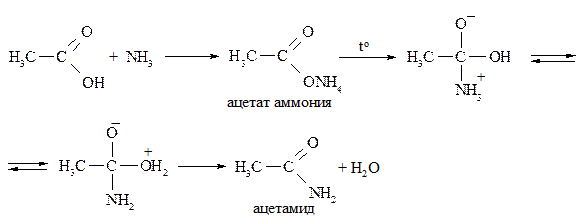
Аналогично из янтарной кислоты получают её имид – сукцинимид:
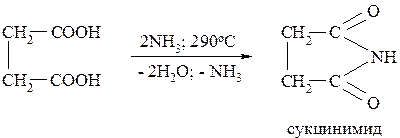
Декарбоксилирование
Декарбоксилирование – отщепление СО2 из карбоксигруппы карбоновых кислот или карбоксилат-аниона солей карбоновых кислот.
В зависимости от условий реакции и строения исходных веществ при декарбоксилировании образуются разные соединения.
Так, например, при сплавлении ацетата натрия с сухим гидроксидом натрия образуется метан:

Однако с другими натриевыми солями алифатических кислот такой процесс сопровождается изменениями углеводородного радикала и соответствующий алкан не получается.
Декарбоксилирование можно осуществить электрохимически:
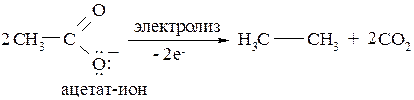
Важное значение для органического синтеза имеет декарбоксилирование с участием серебряной соли карбоновой кислоты при нагревании с бромом. В этом случае образуется алкилбромид:
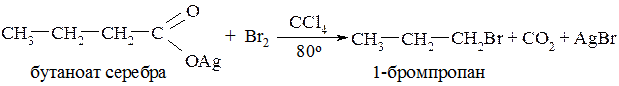
Пиролизом магниевых, кальциевых или бариевых солей карбоновых кислот (кроме соли муравьиной кислоты) можно получить кетоны.
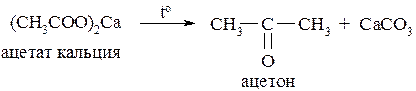
17.3.4. Галогенирование по α-положению
Атомы водорода, связанные с α-углеродным атомом, характеризуются значительной подвижностью и поэтому способны подвергаться замещению. Под действием УФ-облучения на свету или нагревании до 300о-400оС прямое радикальное хлорирование карбоновых кислот происходит неселективно. Например, в условиях радикального хлорирования масляной кислоты образуется смесь всех трех возможных изомеров, среди которых на долю α-хлормасляной кислоты приходится не более 5%.
Избирательное α-галогенирование карбоновых кислот достигается по реакции Геля-Фольгарда-Зелинского: для введения хлора или брома в α-положение карбоновую кислоту обрабатывают галогеном в присутствии каталитических количеств красного фосфора или PCl3 и PBr3:
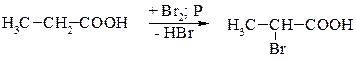
В качестве хлорирующего агента для получения α-хлорзамещенных карбоновых кислот используют хлорид меди (II).
Отдельные представители
Муравьиная кислота (метановая кислота) – бесцветная прозрачная жидкость с резким характерным запахом. В промышленности получают из оксида углерода (II) и гидроксида натрия с последующим действием на полученную соль серной кислотой:

От остальных карбоновых кислот муравьиная кислота отличается тем, что карбоксильная группа в ней связана не с углеводородным радикалом, а с атомом водорода. Поэтому муравьиную кислоту можно рассматривать и как кислоту, и как альдегид:
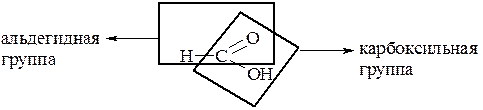
Подобно альдегидам, муравьиная кислота может окисляться:
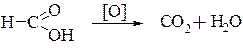
поэтому для нее характерна реакция «серебряного зеркала»:

Под действием концентрированной серной кислоты муравьиная кислота разлагается на СО и воду:
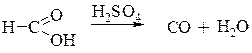
Муравьиную кислоту применяют в промышленном органическом синтезе.
Уксусная кислота (этановая кислота) – бесцветная, прозрачная жидкость, с характерным резким запахом уксуса. Безводная уксусная кислота существует в виде кристаллов, имеющих температуру плавления 16,6оС. Поэтому такую кислоту называют ледяной уксусной кислотой. С водой смешивается во всех соотношениях.
В промышленности кислоту получают различными методами:
окислением уксусного альдегида, который в свою очередь получают либо окислением этилена, либо из ацетилена по реакции Кучерова;
карбонилированием метанола;
каталитическим окислением бутана:
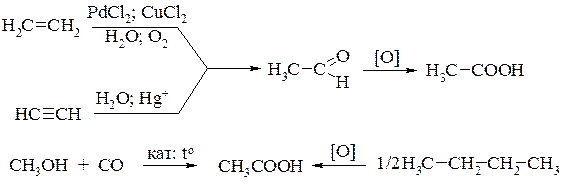
Уксусная кислота находит применение в промышленном органическом синтезе для получения уксусного ангидрида, уксусноэтилового и уксуснобутилового эфиров, красителей и лекарственных веществ, а также в кожевенном производстве и пищевой промышленности.
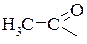 Остаток уксусной кислоты называется ацетильным радикалом (от лат. acetum – уксус). Соли и эфиры уксусной кислоты называют ацетатами.
Остаток уксусной кислоты называется ацетильным радикалом (от лат. acetum – уксус). Соли и эфиры уксусной кислоты называют ацетатами.
 Валериановая– и изовалериановая кислоты –
Валериановая– и изовалериановая кислоты –

Обе кислоты являются компонентами корней с корневищами различных видов валерианы. Обладают успокаивающим действием, однако активность изовалериановой кислоты намного выше. Изовалериановая кислота используется в синтезе такого важного лекарственного препарата, как Валидол.
Введение брома в α-положение способствует усилению седативного действия. В виде этилового эфира α-бромизовалериановая кислота входит в состав комбинированных лекарственных препаратов – Корвалола, Валокордина.
Пальмитиновая C15H31COOH и стеариноваяC17H33COOH кислоты являются важнейшими представителями высших жирных кислот. Они входят в состав твердых жиров.
Олеиновая кислота C17H33COOH является ненасыщенной высшей жирной кислотой. Входит в состав жидких жиров. Содержит непредельную связь в углеводородном радикале: 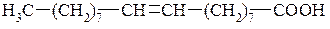
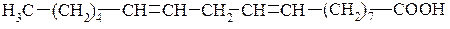 Линолевая кислота С17H31COOH ненасыщенная кислота с двумя двойными связями:
Линолевая кислота С17H31COOH ненасыщенная кислота с двумя двойными связями:
Входит в состав льняного, конопляного и макового масел.
 Линоленовая кислота С17H29COOH сопутствует линолевой кислоте в льняном масле.
Линоленовая кислота С17H29COOH сопутствует линолевой кислоте в льняном масле.
Щавелевая кислота – HOOC–COOH. Бесцветное кристаллическое вещество, растворимое в воде. Относится к сильным кислотам. Широко распространена в растениях. В виде кальциевой соли содержится в оболочках клеток и внутри клеток растений. Оксалатом кальция богаты водоросли, грибы, лишайники, папоротники. В виде монозамещенной калиевой соли («кислая соль») содержится в щавеле и кислице.
Янтарная кислота – HOOC–CH2–CH2–COOH. Бесцветное кристаллическое вещество, растворимое в воде. Название этой кислоты связано с тем, что ее впервые открыли в янтаре. Она содержится в незрелых ягодах крыжовника, винограда, в свекольном соке. Велико биологическое значение янтарной кислоты, поскольку она участвует в цикле трикарбоновых кислот (цикле Кребса). Здесь вследствие дегидрирования из янтарной кислоты образуется фумаровая кислота. Этот процесс ферментативно стереоспецифичен и приводит к транс-фумаровой кислоте. Именно этот изомер вовлекается в дальнейшие превращения.
Энергия, получаемая в результате окислительных процессов в цикле трикарбоновых кислот, становится биохимически доступной благодаря АТФ (аденозинтрифосфорной кислоте).
Малоновая кислота представляет собой кристаллическое вещество, легко разлагающееся при нагревании: происходит декарбоксилирование и образуется уксусная кислота:
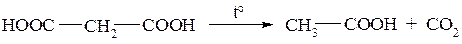
Практическое значение в органическом синтезе имеет полный этиловый эфир малоновой кислоты, который обычно называют малоновым эфиром. В малоновом эфире, благодаря влиянию двух электроноакцепторных карбонилов, метиленовая группа является СН-кислотным центром и, следовательно, атомы водорода способны отщеплятся в виде ионов за счёт гетеролитического разрыва связей С–Н. Для малонового эфира рКα равна 13.
При действии металлического натрия (или этилата натрия) один атом водорода метиленовой группы замещается на натрий с выделением водорода или этанола и образованием енолята, отрицательный заряд которого делокализован между обоими карбонильными группами. При взаимодействии образовавшегося натриймалонового эфира с первичными или вторичными алкилгалогенидами натрий замещается на алкильный радикал и образуется алкилмалоновый эфир. Далее это производное можно подвергнуть кислотному гидролизу, затем провести декарбоксилирование и получить соответствующую карбоновую кислоту.
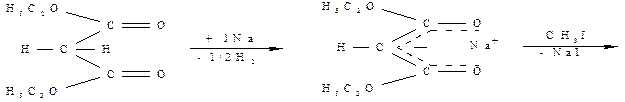
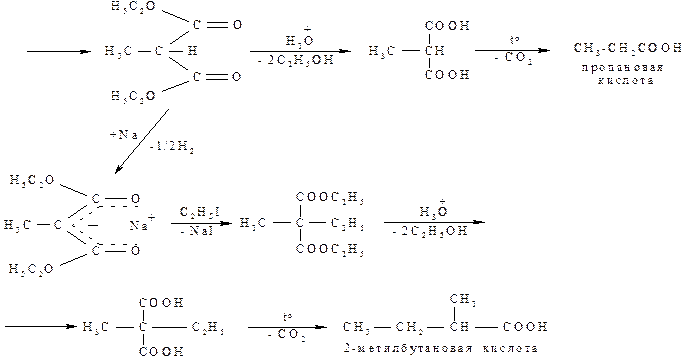
Возможен и другой путь, когда полученный алкилмалоновый эфир вновь взаимодействует последовательно с натрием, затем алкилгалогенидом с последующим гидролизом и декарбоксилированием:
Диэтилмалоновый эфир, получемый таким же путем, используется в синтезе барбитала (см. раздел 25.6).
