Тема: Углеводы – простые и сложные
Контрольные вопросы
1. Углеводы. Классификация по способности к гидролизу.
2. Моносахариды. Альдопентозы. Альдогексозы. Кетогексозы. Строение. Изомерия. Понятие об эпимерах.
3. Кольчато-цепная таутомерия моносахаридов. Аномеры.
4. Химические свойства моносахаридов: свойства многоатомных спиртов; реакции окисления и восстановления; свойства полуацеталей; реакция этерификации.
5. Строение производных моносахаридов. Дезоксисахара. Аминосахара.
6. Классификация дисахаридов. Восстанавливающие дисахариды: мальтоза, лактоза, целлобиоза. Строение. Таутомерные превращения.
7. Мутаротация. Химические свойства: гидролиз, реакции многоатомных спиртов, реакции окисления и восстановления, реакции с участием полуацетального гидроксила.
8. Невосстанавливающие дисахариды: сахароза. Строение. Химические свойства: инверсия сахарозы, реакции многоатомных спиртов.
9. Гомополисахариды: крахмал, гликоген, целлюлоза. Строение и биологическая роль. Химические свойства: гидролиз, качественная реакция на крахмал, образование сложных эфиров целлюлозы.
10. Гетерополисахариды: гиалуроновая кислота. Строение и бироргическая роль.
Демонстрационный вариант билета
1. Покажите строение α,D-галактопиранозы и напишите реакцию этого вещества с метанолом. Назовите продукты реакции.
2. Напишите уравнения реакций образования лактозы и мягкого окисления этого дисахарида. Назовите реагенты и продукты реакций.
3. Гликоген. Покажите строение полисахарида и укажите его биологическую роль.
4. Покажите строение N-ацетил-D-нейраминовой кислоты (сиаловой кислоты). Укажите биологическую роль вещества.
Критерии оценивания контрольной работы:
| Показатели оценивания | Оценки |
| Задания контрольной работы выполнены полностью, без недочетов и грубых ошибок | отлично |
| Задания контрольной работы выполнены полностью, в работе допущены недочеты | хорошо |
| Задания контрольной работы выполнены полностью, в работе допущены грубые ошибки | удовлетворительно |
| Задания контрольной работы выполнены не полностью, в работе допущены грубые ошибки | неудовлетворительно |
Инструкции и методические материалы по процедуре оценивания.
Преподаватель выдает бланки с заданиями контрольной работы по изучаемой теме обучающимся. Обучающиеся выполняют задания контрольной работы в тетрадях для контрольных работ. Задания контрольной работы требуют полного (развернутого) ответа. На выполнение заданий контрольной работы отводиться 60 минут.
Литература
Основная литература
1. Тюкавкина Н. А. Биоорганическая химия [Электронный ресурс] : учебник. Глава 11. Углеводы / Тюкавкина Н.А., Бауков Ю. И., Зурабян С. Э. // Москва : Гэотар-Медиа, 2014. – 416 с. Режим доступа : http://www.studmedlib.ru/ru/book/ISBN9785970427835.html
Дополнительная литература
1. Биоорганическая химия [Электронный ресурс] : руководство к практическим занятиям / под ред. Н. А. Тюкавкина // Москва : Гэотар-Медиа, 2014. – 168 с. Режим доступа : http://www.studmedlib.ru/ru/book/ISBN9785970428214.html
2. Руководство к лабораторным занятиям по биоорганической химии : учеб. пособие для студентов вузов / под ред. Н. А. Тюкавкина // Москва : ДРОФА, 2006. – 319 с.
3. Тюкавкина Н. А. Биоорганическая химия: учеб. для студентов [мед.] вузов / Н. А. Тюкавкина, Ю. И. Бауков // Москва : Дрофа, 2005. – 542 с.
Электронные образовательные ресурсы
Базы данных, информационно-справочные и поисковые системы:
1. Электронная библиотека ОмГМУ: http://weblib.omsk-osma.ru;
2. Электронно-библиотечная система «КнигаФонд»: http://www.knigafund.ru;
3. ЭБС «Консультант студента. Электронная библиотека медицинского вуза» http://www.studmedlib.ru;
4. Научная электронная библиотека: http://elibrary.ru/defaultx.asp;
5. База данных Scopus: http://www.scopus.com.
1.4 a-АМИНОКИСЛОТЫ
СТРОЕНИЕ a-АМИНОКИСЛОТ
Аминокислотами называют бифункциональные производные углеводородов, которые содержат карбоксильную группу -COOH и аминогруппу -NH2.
По заместительной номенклатуре IUPAC аминокислоты называют, испльзуя префикс амино-. и суффикс – овая кислота:
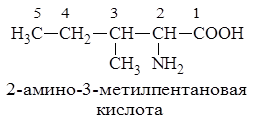
В зависимости от положения аминогруппы по отношению к карбоксильной группе различают α, β, γ и так далее аминокислоты:
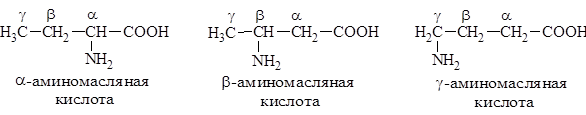
Все природные аминокислоты содержат аминогруппу только в α-положении. Общее число a-аминокислот достигает 300, но из них выделяют группу 20-ти наиболее важных a-аминокислот, встречающихся в составе белков животного и растительного происхождения.
Общая формула a-аминокислот имеет вид:
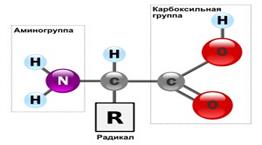
Для природных аминокислот широко распространена тривиальная номенклатура (аланин, валин, лизин и т.д.). Иногда запись аминокислот осуществляют, используя трёх-буквенные сокращения (Aла, Вал, Лиз и др.).
Аминокислоты делят на природные (содержатся в растительных и животных организмах) и синтетические – получены искусственным путем.
Организм синтезирует аминокислоты главным образом из пищевых белков. Но есть целая группа аминокислот, которые организм сам синтезировать не может. Эти аминокислоты называют незаменимыми. К ним относятся (валин, лейцин, изолейцин, лизин, треонин, метионин, фенилаланин и триптофан) Такие аминокислоты должны поступать в организм извне.
Классификация a-аминокислот по составу бокового радикала:
Боковая цепь a-аминокислот имеет специфический состав и строение для каждой a-аминокислоты. Кроме углеводородных радикалов боковой радикал может содержать функциональные группы (-ОН, -SH, -COOH, -NH2) и гетероциклические структуры. Состав боковой цепи определяет основные физико-химические свойства a-аминокислот.
Гидрофильность, то есть способность полярных группировок бокового радикала к образованию водородных связей с молекулой воды объясняется содержанием в вариабельном фрагменте гидрофильных групп (-ОН, -SH, -COOH, -NH2, -N=, -N(H)-).
К гидрофобным группам боковой цепи, снижающим растворимость, относятся углеводородные радикалы, бензольное и индольные ядра.
Ионогенностьбокового радикала, т.е. способность ионизироваться в водном растворе, объясняется наличием в его составе ионогенных групп. Ионногенные группы, диссоциирующие по кислотному механизму:
-COOH ® -COO— + H+ (боковая цепь приобретает отрицательный заряд);
-SH ® -S- + H+ (боковая цепь приобретает отрицательный заряд);
Ar-OH ® Ar-O— + H+ (боковая цепь приобретает отрицательный заряд).
Ионогенные группы, содержащие в своем составе атом с неподеленной электронной парой, способны ионизироваться по основному механизму:
-NH2 + H+ ® -NH3+.
В водном растворе молекулы a-аминокислот и белков, как правило, заряжены.
По строению углеводородного радикалаα-аминокислоты делят на 7 групп:
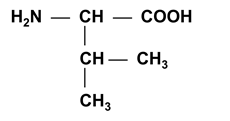
I. Моноаминомонокарбоновые α-аминокислоты (нейтральные):
|
| ||||
|

|
|

|
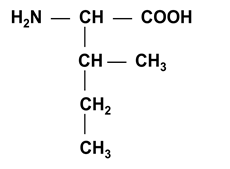
Боковые радикалы a-аминокислот этой подгруппы гидрофобные, неионогенные.
II. Моноаминодикарбоновые α-аминокислоты (кислые):
|

|

Боковые радикалы a-аминокислот этой подгруппы гидрофильные, ионогенные, несут отрицательный заряд (-OOC ¾ CH2 ¾ ).
В состав белков входят амиды данных кислот:
|

|
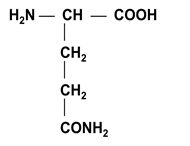
III. Диаминомонокарбоновые α-аминокислоты (основные)
|
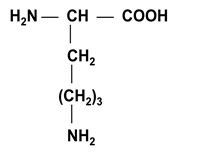
Боковой радикал гидрофильный, ионогенный, несет положительный заряд (H3N+ ¾ (CH2)4 ¾).
|
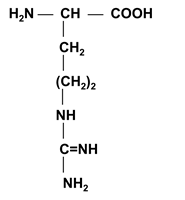
Боковой радикал гидрофильный, ионогенный, несёт положительный заряд (H2N+ = C(NH2)¾ NH ¾ (CH2)3 ¾).
IV. Гидроксиаминокислоты
|
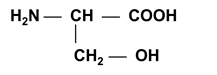
|

Боковые радикалы гидрофильные, неионогенные (имеют спиртовую природу).
