Строение пируватдегидрогеназного комплекса:
3 фермента:
1) пируватдегидрогеназа (Е1)
2) дигидролипоамидацелтрансфераза (Е2)
3) дигидролипоамиддегидрогеназа (Е3)
5 коферментов:
1) тиаминдифосфат (ТДФ)
2) липоевая кислота, связанная с Е2 - липоамид
3) ФАД
4) НАД+
5) СоА
Витамины и коферменты, используемые в процессе:
1 реакция
Пируватдегидрогеназа (Е1), кофермент – тиаминдифосфат(включает витамин В1),
функция – окислительное декарбоксилирование пировиноградной кислоты.
2 и 3 реакции
Дигидролипоамидацетилтрансфераза (Е2), кофермент – липоевая кислота, функция – перенос ацетильной группы на HS-КоА и образование ацетил-SКоА
4 и 5 реакции
Дигидролипоамиддегидрогеназа (Е3), кофермент – ФАД, функция – регенерация окисленной формы липоамида, образование НАДН + Н+ и возвращение комплекса в исходное состояние.
Регуляция комплекса:
Активность пируватдегидрогеназного комплекса регулируется различными способами: доступностью субстратов, ингибированием продуктами реакции, аллостерическим путем, путем ковалентной модификации.
На примере ковалентной модификации:
В состав ПДК входят 2 регуляторных субъединицы - киназа ПДК (фосфорилирует ферменты комплекса и инактивирует ПДК; а фосфатаза (дефосфорилирует ферменты, превращая комплекс в активную форму). Они действуют на фермент Е1(киназа активируется при избытке АТФ, а фосфатаза активируется при поступлении ионов кальция или инсулином).
2. Опишите состав, структуру, номенклатуру и функции дыхательных комплексов и других компонентов цепи переноса электронов.
I комплекс,
НАДН-KoQ-оксидоредуктаза
I комплекс носит рабочее название НАДН-дегидрогеназа, кофермент – ФМН,
Функция
1. Принимает электроны от НАДН и передает их на коэнзим Q (убихинон).
2. Переносит 4 иона Н+ на наружную поверхность внутренней митохондриальной мембраны.
II комплекс
Включает в себя ФАД-зависимые ферменты(напр. сукцианатдегидрогеназа), расположенные на внутренней мембране.
Функция
1. Восстановление ФАД в окислительно-восстановительных реакциях.
2. Обеспечение передачи электронов от ФАДН2 на железосерные белки внутренней мембраны митохондрий. Далее эти электроны попадают на коэнзим Q.
III комплекс
КоQ-цитохром С – оксидоредуктаза
Это комплекс цитохромов b-c1.
Функция
1. Принимает электроны от коэнзима Q и передает их на цитохром с.
2. Переносит 4 иона Н+ на наружную поверхность внутренней митохондриальной мембраны.
IV комплекс,
цитохром с – кислород-оксидоредуктаза
IV комплекс – цитохромоксидазаили комплекс цитохромов аа3.
Функция
1. Принимает электроны от цитохрома с и передает их на кислород с образованием воды.
2. Переносит 2 иона Н+ на наружную поверхность внутренней митохондриальной мембраны.
V комплекс
фермент АТФ-синтаза
Состоит из множества белковых цепей, подразделенных на две большие группы:
субъединица Fо – ее функция каналообразующая, по ней выкачанные наружу протоны водорода устремляются в матрикс.
субъединица F1 – ее функция каталитическая. Она, используя энергию протонов, синтезирует АТФ.
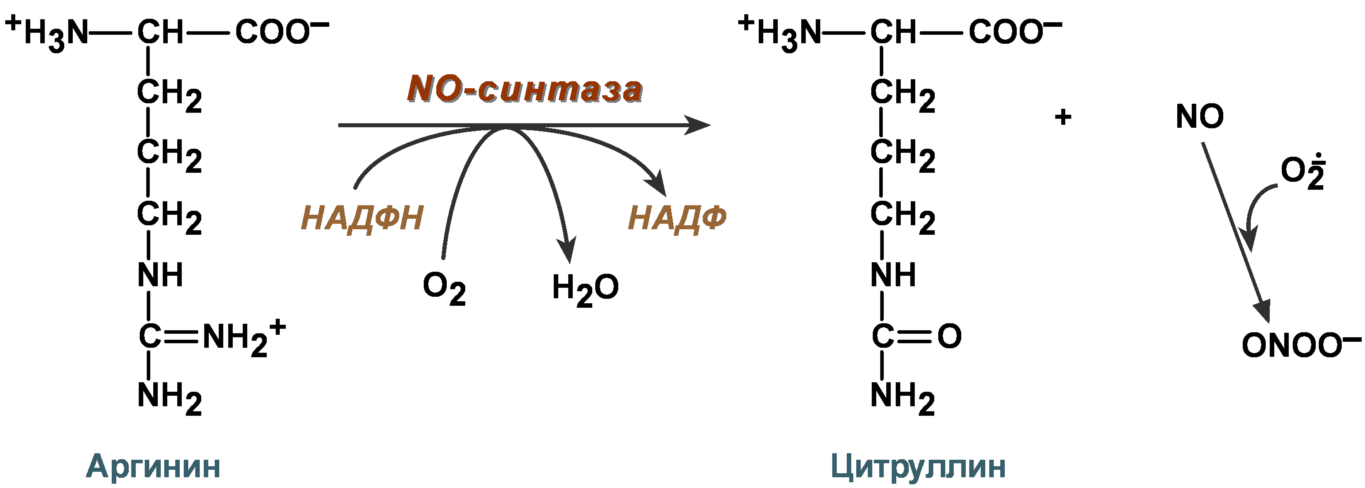
3.Напишите ферментативные реакции образования супероксид анион-радикала, активных форм азота и хлора. Какова дальнейшая судьба и роль этих активных форм?
а) образование супероксид анион-радикала

не обладает сильными окислительными свойствами, но представляет большую опасность, поскольку является источником образования более активных АФК
б) образование активных форм хлора

в) образование активных форм азота
Билет 5
1. Охарактеризуйте цикл трикарбоновых кислот. Укажите его функции и энергетическое значение. Дайте характеристику витаминов и коферментов, используемых в процессе.
ЦТК – заключительный этап катаболизма, в котором углерод ацетильного остатка ацетил Ко-А окисляется до 2 молекул СО2. Атомы водорода, освобождающиеся в ОВР, доставляются в ЦПЭ при участии NAD- и FAD-зависимых дегидрогеназ, в результате чего происходят синтез воды и окислительные фосфорилирование АДФ. Связь между атомами углерода в ацетил Ко-А устойчива к окислению. В условиях организма окисление ацетильного остатка происходит в несколько этапов, образующих циклический процесс из 8 реакций.
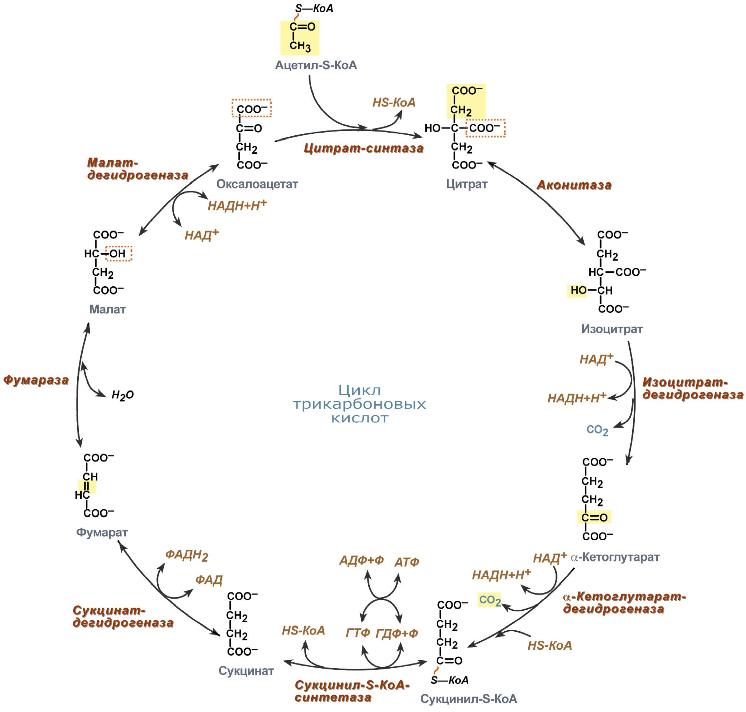
Каждый оборот цикла лимонной кислоты сопровождается синтезом 11 молекул АТФ путем окислительного фосфорилирования. Одна молекула АТФ образуется путем субстратного фосфорилирования. В итоге на каждый ацетильный остаток, включенный в ЦТК, образуется 12 молекул АТФ.
Значение этого процесса в том, что он является главным генератором водорода для цепей транспорта электронов, то есть именно он в основном обеспечивает их функционирование, а, следовательно, и синтез АТФ. Локализован цикл Кребса в матриксе митохондрий. Этот процесс является интегративным – он объединяет пути катаболизма углеводов, белков и липидов: в ходе распада всех этих соединений появляется ацетил Ко-А, который и расщепляется до конца в ЦТК.
Ферменты и коферменты:
1 реакция
Пируватдегидрогеназа (Е1), кофермент – тиаминдифосфат, функция – окислительное декарбоксилирование пировиноградной кислоты,
2 и 3 реакции
Дигидролипоат-ацетилтрансфераза (Е2), кофермент – липоевая кислота, функция – перенос ацетильной группы на HS-КоА и образование ацетил-SКоА
4 и 5 реакции
Дигидролипоат-дегидрогеназа (Е3), кофермент – ФАД, функция – регенерация окисленной формы липоамида, образование НАДН+Н+ и возвращение комплекса в исходное состояние.
Регуляторными являются следующие ферменты ЦТК: цитратсинтаза (ингибируется НАДН и АТФ), изоцитратдегидрогеназа (ингибируется НАДН и АТФ, активируется АДФ), сукцинатдегидрогеназа (ингибируется ЩУК, активируется сукцинатом, фумаратом, Н3РО4)
2. Дайте характеристику процессу окислительного фосфорилирования. Поясните механизм сопряжения окисления и фосфорилирования.
Окислительным фосфорилированием называют синтез АТФ путем фосфорилирования АДФ за счет энергии трансмембранного электрохим потенциала, возникающего при освобождении энергии электронами окисленного субстрата в процессе миграции этих электронов по дыхательной цепи к вдыхаемому кислороду. То есть окисл фосфорилирование – это синтез АТФ, связанный с переносом электронов по дыхательной цепи, это синтез АТФ за счет энергии окисления субстрата. Происходит в аэробных условиях
Основные этапы окислительного фосфорилирования:
1. Образующиеся в реакциях катаболизма НАДН и ФАДН2 передают атомы водорода (т.е. протоны водорода и электроны) на ферменты дыхательной цепи.
2. Электроны движутся по ферментам дыхательной цепи и теряют энергию.
3. Энергия электронов используется на выкачивание протонов Н+ из матрикса в межмембранное пространство.
4. В конце дыхательной цепи электроны попадают на кислород и восстанавливают его до воды.
5. Протоны Н+ стремятся обратно в матрикс и проходят через АТФ-синтазу.
6. При этом они теряют энергию, которая используется для синтеза АТФ.
Под сопряжением окисления с фосфорилированием понимают превращение энергии электронов окисленного субстрата, проходящих по дыхательной цепи, в промежуточную форму – в энергию трансмембранного потенциала с последующим использованием ее для фосфорилирования АДФ, то есть для синтеза АТФ. Протонный градиент создается путем выталкивания ионов водорода в межмебранное пространство в 3 участках дых цепи: при переходе электронов с ФМНН2 через FeS-белок на KoQ, при переходе электронов с KoQH2 через FeS-белок на цитохром Ci при переходе электронов от цитохрома, а через цитохром а3 к кислороду. Эти участки цепи транспорта электронов обозначают как пункты сопряжения дыхания с фосфорилированием.
3. Напишите ферментативные реакции образования пероксида водорода. Какова дальнейшая судьба и роль пероксида водорода?
Пероксид водорода образуется с помощью фермента супероксидазы из:
а) диоксида 2∙О2- + 2H+ → Н2О2 + О2
б) протонированной формы диоксида 2 НО2∙ → Н2О2 + О2
Пероксид водорода не является радикалом и, будучи нейтральной молекулой, легко проникает через гидрофобные мембраны. Токсические эффекты перекиси водорода проявляются при концентрации более 5х10^-5, которая наблюдается в очагах воспаления благодаря активации фагоцитирующих клеток. Пероксид водорода занимает особое место в генерации АФК в лейкоцитах для уничтожения инфицирующих микроорганизмов.
Н2О2 в присутствии миэлопероксидазы и перксидазы эозинофилов служит источником гипогалогенидов (например, HClO), которые тоже токсичны и подавляют микрофлору:
HCl + Н2О2 → HClO + H2O
В организме пероксид водорода постоянно разрушается за счет ферментов каталазы
(2Н2О2 → 2Н2О +О2) и пероксидазы (SH2 + Н2О2 → S + 2H2O).
Свободно проникая внутрь клетки, перокисид водорода взаимодействует с ионами металлов (железо, медь), в результате чего образуется гидроксид-радикал (гидроксильный радикал) НО∙ :
Н2О2+ Cu+ → Cu2+ + ОН- + НО∙
Билет 6
1.Напишите последовательность реакций цикла трикарбоновых кислот. Поясните анаболические функции цикла трикарбоновых кислот . Отметьте анаплеротические реакции и их значение. 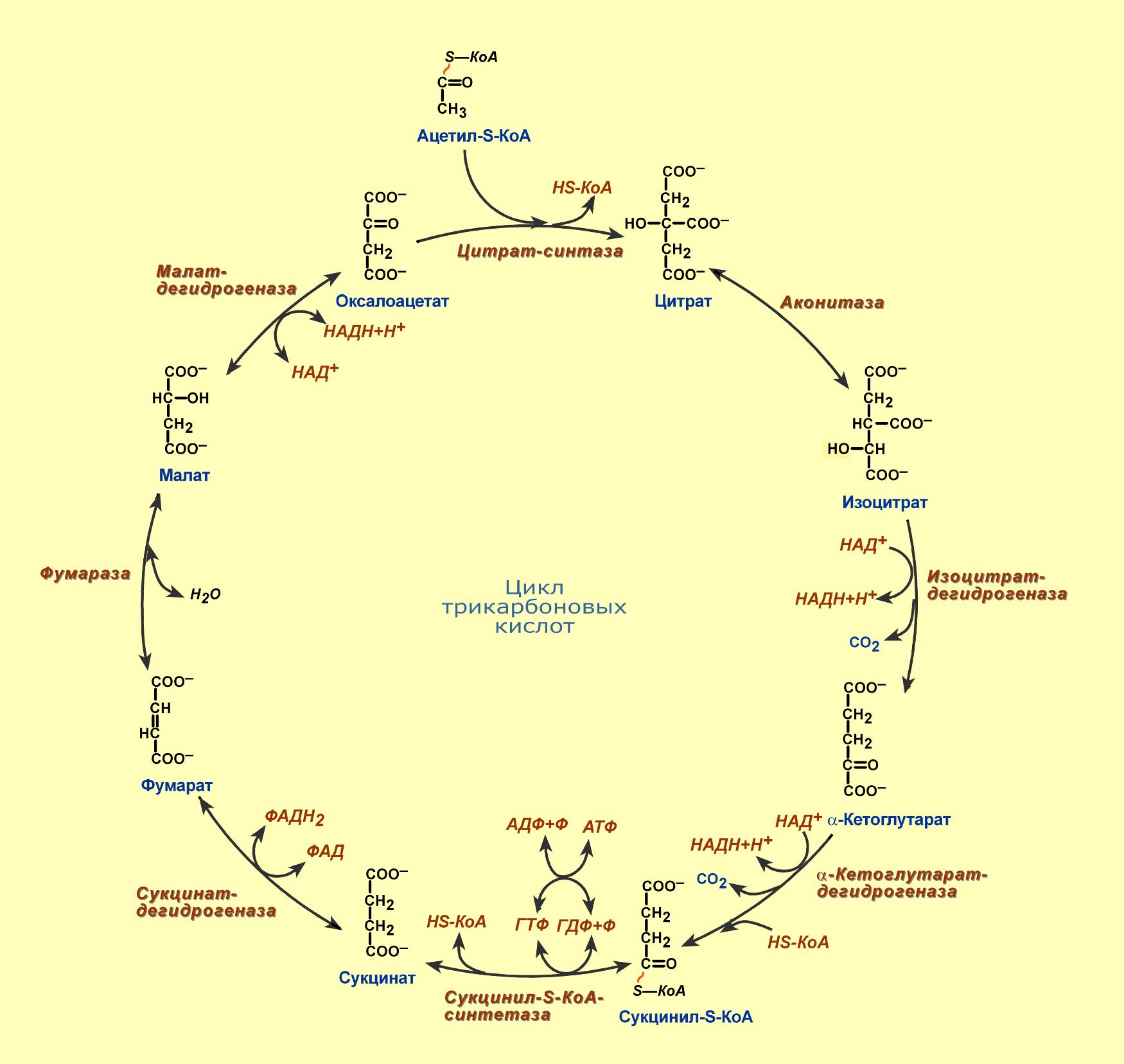
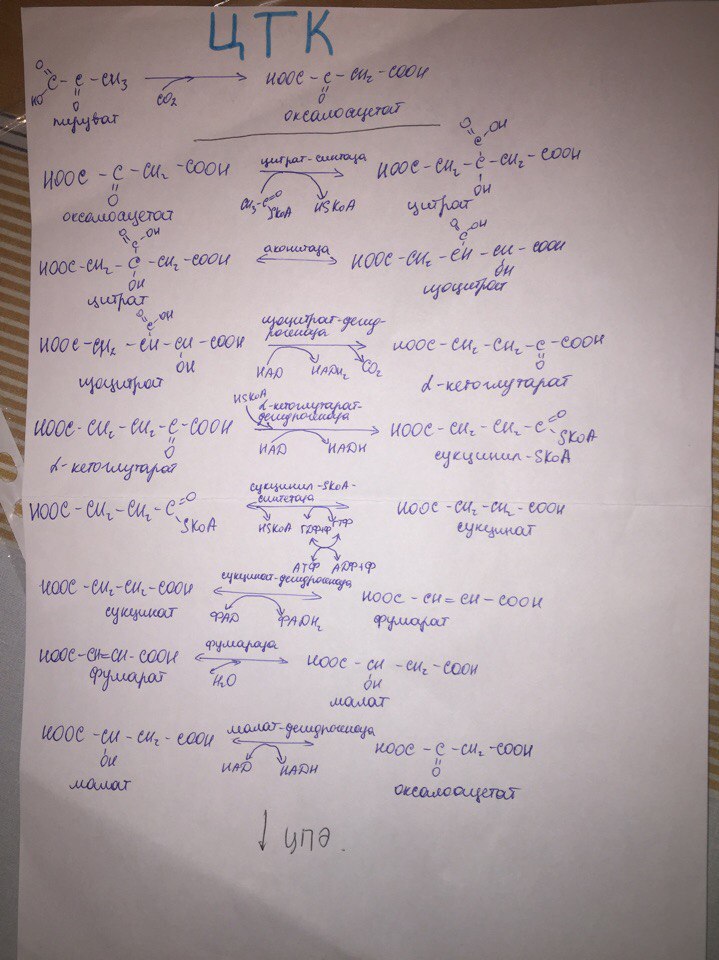
Анаплеротические пути
Промежуточные соединения цикла трикарбоновых кислот, покинувшие цикл и задействованные в синтезе различных соединений, замещаются за счёт специальных анаплеротических реакций. В нормальных условиях реакции, в ходе которых промежуточные соединения цикла вовлекаются в другие метаболические пути, и реакции, возмещающие их уход, находятся в динамическом равновесии, поэтому концентрация промежуточных соединений цикла трикарбоновых кислот поддерживается постоянно.
Ниже в таблице представлены важнейшие анаплеротические реакции:
| Реакция | Фермент | Ткань/организм | |
| пируват + НСО3− + ATP ⇌ оксалоацетат + ADP + Pi | пируваткарбоксилаза | печень, почки | |
| фосфоенолпируват + СО2 + GDP ⇌ оксалоацетат + GTP | фосфоенолпируваткарбоксикиназа | сердце,скелетные мышцы | |
| фосфоенолпируват + НСО3− ⇌ оксалоацетат + Pi | фосфоенолпируваткарбоксилаза | высшие растения,дрожжи, бактерии | |
| пируват + НСО3− + NAD(P)H ⇌ малат + NAD(P)+ | малик-энзим | широко распространена среди эукариот и бактерий |
