Функционально-метаболические расстройства при ОПН
В период олигоанурии, в связи с резким снижением экскреторной функции почек, возникают гиперазотемия и водно-электролитные расстройства. Концентрация мочевины в сыворотке крови может достигать 120-150 ммоль/л, остаточного азота - 200-300 ммоль/л; увеличивается также содержание креатинина (1,3-1,7 ммоль/л), мочевой кислоты, аминокислот, «средних молекул», гуанидинов и др. Развитию гиперазотемии в ряде случаев способствует также усиленный распад белков в травмированных тканях. ,
Нарушения водно-электролитного обмена проявляются в виде гипергидратации, гиперкалие-мии, гипермагниемии, гиперфосфатемии; экскреция почками натрия, хлора и кальция также затруднена, но концентрация их в сыворотке снижена из-за гидремии и нарушения кишеч-
ной абсорбции кальция в связи с пониженным синтезом витамина D3.
Гипергидратация сопровождается развитием периферических Отеков и водянок, иногда отека легких и мозга; в ряде случаев могут развиться артериальная гипертония и левожелудочковая недостаточность. В целях профилактики этих нарушений следует ограничивать поступление жидкости извне. Гиперкалиемия может возникнуть в первые дни олигурического периода и вызвать остановку сердца. Гипокальциемия способствует появлению судорог и развитию гипер-паратиреоза.
У большинства больных ОПН возникает метаболический ацидоз. Этому способствует нарушение образования в почечных канальцах бикарбоната натрия и аммония, в составе которого экскретируются Н*-ионы. Уровень бикарбоната в сыворотке снижается до 13 ммоль/л (в норме 24 ммоль/л). Происходит задержка в крови анионов S042 и Р043-, которые устраняются только через почки. При развитии некомпенсированного ацидоза появляется дыхание Куссмауля, возникают нарушения функции ЦНС. Перечисленные нарушения гомеостаза обусловливают появление симптомов уремии; иногда на 5 - 7-е сут ОПН возникает состояние уремической комы (при анурии).
В период восстановления диуреза (полиурии) может развиться состояние обезвоживания (дегидратации), происходит повышенная потеря с мочой натрия и калия из-за пониженной способности вновь образованного почечного эпителия к реабсорбции этих ионов. В связи с нарушением баланса электролитов возникает гипотония мышц, гипорефлексия, возможно появление парезов и параличей. Основную роль в гене-зе этих расстройств играет гипокалиемия. Уровень остаточного азота, мочевины и креатинина в сыворотке крови остается еще повышенным, но постепенно снижается.
Исходы ОПН зависят в значительной степени от ее вида: при преренальной форме смертность составляет около 7%, а при ренальной, с наличием острого канальцевого некроза, достигает 80%; в среднем летальный исход имеет место в 40-45 % случаев. Основными причинами наступления смерти являются остановка сердца под действием гиперкалиемии; осложнения, связанные с гипергидратацией; уремическая кома; присоединение инфекции (пневмония, пиелонефрит, сепсис и др.). Развитию инфекционных за-
болеваний на фоне ОПН способствуют снижение клеточного и гуморального иммунитета, угнетение фагоцитарной функции и хемотаксиса лейкоцитов. Половина летальных исходов приходится на восстановительный период (инфекция, эмболия). При отсутствии лечения ренальная форма ОПН заканчивается смертью.
18.11.3. Хроническая почечная недостаточность
Состояние хронической почечной недостаточности характеризуется медленно прогрессирующей утратой функции почек, обусловленной постепенной гибелью нефронов с замещением их соединительной тканью, что приводит к образованию сморщенной почки. Этот процесс необратим.
Этиология. К развитию ХПН приводят такие заболевания, как хронический пиелонефрит, хронический гломерулонефрит, тубулоинтерсти-циальный нефрит, диабетическая нефропатия, амилоидоз, поликистоз, системная красная волчанка, длительная обструкция мочевых путей, сосудистая патология - атеросклероз почечных сосудов, артериальная гипертензия и некоторые другие заболевания.
Постепенность развития ХПН объясняется не только медленной гибелью нефронов, но и компенсаторно усиленной функцией нефронов, оставшихся неповрежденными.
Стадии развития ХПН. В зависимости от степени нарушения функции почек и расстройств гомеостаза выделяется несколько стадий. Предложено различать три стадии, каждая из которых подразделяется на фазы А и Б.
Стадия I - латентная. Фаза IA характеризуется нормальными показателями содержания креатинина в плазме крови и объема клубочко-вой фильтрации, но при проведении нагрузочных проб на концентрацию и разведение выявляется уменьшение функционального резерва почек. В фазе IB уровень креатинина в сыворотке соответствует верхней границе нормы, а размер клубочковой фильтрации составляет 50 % от должного. Обнаруживается понижение концентрационной способности почек.
Стадия II - гиперазотемическая (концентрация креатинина в сыворотке крови 0,13 ммоль/л и выше, мочевины - 11 ммоль/л и выше). В фазе ПА клубочковая фильтрация понижена до 40-20 %, а в фазе ПБ - до 19-10 % от должной.
Часть III. ПАТОФИЗИОЛОГИЯ ОРГАНОВ И СИСТЕМ
Стадия III - уремическая,характеризуется снижением объема клубочковой фильтрации до 10-5 % от должного, имеется высокая степень гиперазотемии и клинические признаки уремии.
Особенности функционирования почек при ХПН.В процессе развития болезни изменяются объем и относительная плотность выделяющейся мочи. Различают стадии полиурии и олигу-рии. В стадии полиурииобъем суточной мочи возрастает до 2-4 л, причем наиболее ранним отклонением от нормы является увеличение объема ночного диуреза (никтурия). Вместе с тем моча имеет низкую относительную плотность, близкую к таковой первичной мочи (1010-1014). Дляобъяснения механизма развития этих изменений предложена гипотеза «интактного нефрона»,согласно которой неповрежденные, продолжающие функционировать нефроны гипертрофируются и работают с повышенной нагрузкой. В них увеличивается скорость клубочковой фильтрации за счет расширения афферентных и повышения тонуса эфферентных артериол. В результате увеличивается гидростатическое давление в полости капсулы клубочка, что сопровождается ускоренным перемещением жидкости по канальцам и сокращением времени пребывания ее в контакте с канальцевым эпителием. Это ограничивает процесс реабсорбции растворенных в первичной моче веществ, и они удерживают внутри канальцев воду, препятствуя ее всасыванию. В результате развивается осмотический диурез. Кроме того, обнаружено снижение чувствительности эпителия дистальных канальцев и собирательных трубочек к действию альдостерона и АДГ. Вследствие этого еще в большей степени снижается реабсорбция натрия, воды и мочевины и выделяется в повышенном объеме слабо концентрированная моча. Уменьшению концентрационной способности также способствует укорочение времени пребывания жидкости в петле Генле. В результате снижается поступление в интерстиций мозгового вещества почек различных электролитов, привлекающих сюда воду из дистальных отделов нефрона. Поскольку общий объем клубочковой фильтрации понижен из-за уменьшения количества функционирующих не-фронов, то выведение с мочой большого количества воды и натрия рассматривается как приспособительная реакция, препятствующая развитию гипергидратации и гипернатриемии.
Длительное повышение гидростатического давления в клубочкахинтактных нефронов вы-
зывает их повреждение в виде дилатации и фокального гломерулосклероза.
В результате количество действующих нефронов продолжает снижаться, что и обусловливает переход в стадию олигурии, когда клубочковая фильтрация уменьшается до 10 мл/мин или в еще большей степени, а объем суточной мочи становится менее 500 мл. На этой стадии полностью утрачивается способность почек к разведению и концентрированию мочи, наблюдается изостенурия. Расстройства гомеостаза достигают выраженной степени. Развивается уремия.
Функционально-метаболические расстройства при ХПН
Развитие ХПН сопровождается гиперазотемией, ацидозом, нарушениями электролитного, водного и других видов обмена. Гиперазотемия обусловлена уменьшением объема клубочковой фильтрации. Стойкое увеличение содержания в крови креатинина, мочевины и мочевой кислоты происходит на той стадии болезни, когда объем фильтрации составляет менее 40 % от нормы. Показателем развития хронической почечной недостаточности является концентрация креатинина 0,13 ммоль/л и выше, а мочевины -10 ммоль/л и выше. В поздние сроки ХПН концентрация этих веществ в крови возрастает в 4-5 раз и более по сравнению с нормой.
При задержке экскреции с мочой конечных продуктов обмена отмечается выделение мочевины и других азотистых метаболитов через пищеварительный тракт, потовые железы, дыхательные пути, а также через серозные оболочки и в полость суставов. Задержка в организме мочевой кислоты сопровождается отложением уратов в тканях, развитием подагры. Нарушения минерального обмена проявляются в виде гипокальциемии, гиперфосфатемии, гиперкали-емии, гипо- или гипернатриемии, гипермагние-мии. Развитие гипокальциемии связано с нарушением образования в проксимальных канальцах витамина D3, при недостатке которого снижается всасывание кальция в кишечнике. Вместе с тем снижаются клубочковая фильтрация и выделение с мочой неорганических фосфатов, что ведет к развитию гиперфосфатемии. Избыток фосфатов в сыворотке сопровождается образованием нерастворимой фосфорно-кальциевой соли, которая откладывается в мягких тканях, в том числе и в почках. Это способствует разви-
тию еще более выраженной гипокальциемии, которая стимулирует секрецию паратгормона. В результате возникает состояние вторичного ги-перпаратиреоза. Для предупреждения этого необходимо ограничить поступление фосфатов с пищей. Гиперкалиемия развивается у больных ХПН только на поздней стадии болезни, когда клубочковая фильтрация становится ниже 15 мл/ мин, а диурез менее 600 мл/сут. В течение длительного срока резкое снижение фильтрации калия в клубочках компенсируется усиленной секрецией его в канальцевую жидкость в дис-тальных отделах нефрона, а также повышенной экскрецией через стенку толстого кишечника. При повышенном поступлении калия с пищей механизм компенсации становится недостаточным, поэтому потребление его следует ограничить.
В течение довольно длительного времени почки сохраняют способность освобождать организм от избытка натрия благодаря тому, что наряду с резким ограничением фильтрации снижается реабсорбция его в канальцах и повышается размер экскреции. В некоторых случаях на стадии полиурии наблюдается чрезмерная потеря натрия с мочой, в результате происходит «солевое истощение», возникает гипонатриемия, сопровождающаяся гипотонией и слабостью. В поздние сроки в связи с прогрессирующим снижением клу-бочковой фильтрации развивается гипернатрие-мия. Поэтому на стадии олигурии необходимо ограничить прием соленой пищи. Развитию гипо-или гипернатриемии способствуют нарушения водного баланса. Почки утрачивают способность контролировать объем внеклеточной жидкости путем удаления избытка воды при водной нагрузке или задержки ее при недостаточном поступлении извне. Стойкая задержка воды в организме происходит на стадии олигурии. Это ведет к гипергидратации, которая в сочетании с гипернатриемией способствует развитию отеков и артериальной гипертензии.
При ХПН развивается метаболический ацидоз, чему способствует потеря бикарбонатов с мочой вследствие понижения их реабсорбции в канальцах оставшихся немногочисленных нефро-нов. Кроме того, снижается экскреция почками Н+-ионов в связи с недостаточным аммониогене-зом. Играет роль также задержка в организме фосфатов и сульфатов. Больным ХПН часто требуется введение щелочей для нейтрализации задержанных в организме кислот.
Другие нарушения метаболизма связаны с гипоксией, недостаточностью функции печени и гормональными расстройствами, которые обусловлены понижением катаболизма в почках гормонов полипептидной природы (глюкагон, инсулин, СТГ, пролактин, вазопрессин, гормоны гипоталамуса); содержание их в крови повышается. Снижается использование глюкозы тканями. Замедлен метаболизм триглицеридов. Развивается гиперлипидемия. Усилен катаболизм белков. Развитие гипоксии связано с анемией и сердечно-сосудистыми расстройствами.
18.12. УРЕМИЯ
Уремия (мочекровие, от греч. uron - моча и haima - кровь) - клинический синдром прогрессирующей почечной недостаточности, характеризующийся разнообразными нарушениями метаболизма и функций многих органов.
Уремия может развиться на второй и третьей стадиях ОПН и закономерно возникает на терминальной стадии ХПН.
18.12.1. Клинические проявления уремии
Наиболее ранними являются неспецифические общие симптомы - слабость, быстрая утомляемость, бессонница.
Далее появляются симптомы нарушения функций и структуры различных органов:
- органов пищеварения (анорексия, тошнота, рвота, диарея, глоссит, стоматит, колит, гастро-дуоденит, гепатит, изъязвления слизистой, что в значительной степени связано с экскрецией через нее азотистых шлаков);
- сердечно-сосудистой системы (артериальная гипертензия, сердечная недостаточность, аритмия, перикардит, остановка сердца);
- органов дыхания (одышка, кашель, отек легких, дыхание Куссмауля);
- системы крови (анемия, лейкоцитоз, тром-боцитопатия);
- системы гемостаза (кровоизлияния в кожу, маточные, из слизистой пищеварительного тракта, носовые);
- центральной и периферической нервной системы (головная боль, ослабление памяти, спутанное сознание, психическая депрессия, кома, судороги, тремор, мышечные подергивания, зуд, полиневриты);
Часть III. ПАТОФИЗИОЛОГИЯ ОРГАНОВ И СИСТЕМ
- иммунной системы (угнетение гуморального и клеточного иммунитета, понижение устойчивости к инфекции);
- кожи - обнаруживается желтоватая окраска, налет на ней мочевины, расчесы, петехиаль-ная сыпь;
- остеопороз, остеомаляция.
18.12.2. Патогенез уремии
В механизме развития наблюдаемых при уремии нарушений большое значение имеют расстройства метаболизма, отравление эндогенными токсинами, гормональные расстройства.
К метаболическим сдвигам, которые играют роль в развитии синдрома уремии, относятся: гиперкалиемия, гиперфосфатемия, гипермагни-емия, гипо- или гипернатриемия, гипокальцие-мия, гипергидратация, ацидоз и др.
Гиперкалиемия вызывает снижение потенциала покоя, приближает его к потенциалу действия, что сопровождается вначале повышением возбудимости нервных и мышечных клеток (это может быть причиной мышечных подергиваний, судорог), а затем, когда потенциалы покоя и действия сравняются, возбудимость утрачивается и может произойти паралич мышц, остановка сердца. В развитии неврологических расстройств, кроме того, играют роль гипермаг-ниемия, гипернатриемия, гипокальциемия, ацидоз. Гиперфосфатемия, гипермагниемия и гипокальциемия способствуют развитию остеопоро-за, фиброзной остеодистрофии и остеомаляции.
Гипернатриемия в сочетании с гипергидратацией является основной причиной развития артериальной гипертензии, сердечной недостаточности и отеков, в том числе отека мозга и легких.
В развитии сердечной недостаточности играют роль и другие электролитные расстройства, гиперпаратиреоз и анемия. Метаболический ацидоз, к которому может присоединиться газовый при отеке легких, обусловливает появление дыхания Куссмауля, оказывает влияние на активность различных ферментов и сосудистый тонус.
В развитии уремии общепризнанной является роль эндогенных токсинов. Первоначально к ним относили продукты азотистого обмена, однако в экспериментах на животных была установлена очень слабая токсичность мочевины. Креатинин также мало токсичен, но повреждающее действие могут оказать продукты его распада, такие как саркозин, метиламин, N-метил-
гидантоин. Главный токсический эффект связывают с накоплением в крови фенолов и «средних молекул» (олигопептиды с м.м. от 300 до 5000 Д). Предполагается, что одни из них являются продуктами внутриклеточной деградации белков, другие образуются из белков пищи под действием кишечной микрофлоры. При введении животным они вызывают ряд изменений, подобных наблюдаемым при уремии (замедление проведения нервных импульсов, понижение активности ряда ферментов, состояние иммуно-депрессии). В настоящее время роль универсального уремического токсина отводится паратгор-мону, с гиперпродукцией которого под действием гипокальциемии и гиперфосфатемии связывают нарушение функции сердца, развитие остеодистрофии, полиневропатии, анемии, гипер-триглицеридемии и др. Токсическое действие приписывается также производным пиридина, полиаминам, маннитолу и сорбитолу. Токсическое действие оказывает алюминий, поступающий в организм с водой (в особенности при гемодиализе) и пищей.
В развитии уремического синдрома играют роль гормональные нарушения, обусловленные почечной недостаточностью, в связи с которой происходит задержка в организме гормона роста, глюкагона, инсулина, пролактина и др. Следствием этих гормональных сдвигов являются расстройства углеводного и жирового обмена, развитие аменореи и импотенции. Недостаточное образование в почках эритропоэтина сопровождается развитием анемии, а понижение синтеза в проксимальных канальцах кальцитриола играет главную роль в развитии гипокальциемии со всеми вытекающими из этого последствиями. В механизме развития комы, которой завершается уремический синдром, наряду с нарушениями обмена электролитов, гипергидратацией и ацидозом, играют роль гипоксия, возникающая в связи с анемией, сердечной недостаточностью и нарушением газообмена в легких, а также интоксикация центральной нервной системы эндогенными токсинами. Нередко причиной летального исхода является присоединение инфекции, например пневмонии. Этому способствует снижение активности иммунной системы (ослабление реакции лимфоцитов на антигенное воздействие, снижение хемотаксиса лейкоцитов и др.). Возможна смерть от остановки сердца под действием гиперкалиемии и гипермагниемии. Развитие различных проявлений уремии зна-
 чительно замедляется при длительном лечении гемодиализом, который позволяет снизить азотемию, нарушения электролитного баланса и очистить кровь от эндогенных токсинов. Радикальным методом лечения является пересадка донорской почки.
чительно замедляется при длительном лечении гемодиализом, который позволяет снизить азотемию, нарушения электролитного баланса и очистить кровь от эндогенных токсинов. Радикальным методом лечения является пересадка донорской почки.
ГЛОМЕРУЛОНЕФРИТЫ
Это группа заболеваний, характеризующихся развитием воспаления клубочков обеих почек и клеточной пролиферацией, которые сочетаются с гематурией. По механизму развития гломерулонефриты относятся к заболеваниям иммунного генеза. В настоящее время выделяют по патогенезу два варианта гломерулонефри-та: иммунокомплексный и обусловленный образованием аутоантител к антигенам базальной мембраны капилляров клубочков.
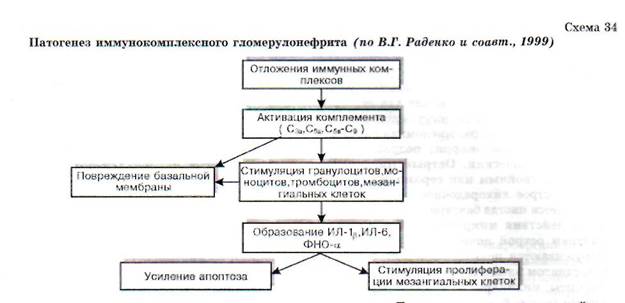
Иммунокомплексный гломерулонефритразвивается в связи с отложением на базальной мембране капилляров клубочков циркулирующих в крови иммунных комплексов, состоящих из экзогенных или эндогенных антигенов и направленных против них антител. Эти комплексы обнаруживаются в почечных клубочках посредством иммунофлюоресцентной или электронной микроскопии. В качестве источника экзогенных антигенов могут выступать чужеродные белки (например, белки аллогенной сыворотки крови, вакцины), различные бактерии и вирусы, паразиты и др.; эндогенными антигенами могут являться продукты распада опухолевых или нормальных тканей (например, ДНК или комплекс ДНК с гистонами при системной красной волчанке). Осевшие на базальной мембране иммунные комплексы вызывают активацию системы комплемента, свертывающей и калликре-иновой систем, привлекают лейкоциты, которые освобождают лизосомальные ферменты и активные формы кислорода, повреждающие стенку капилляров клубочков; последняя при этом становится проницаемой для эритроцитов и белка. Агрегация на поврежденной стенке капилляров тромбоцитов и преципитация фибрина, так же как и освобождение из инфильтрующих клубочки лейкоцитов и мезангиальных клеток различных медиаторов воспаления, обусловливает дальнейшее его развитие, которое может закончиться восстановлением нормальной структуры и функции клубочков или их фиброзом и развитием почечной недостаточности (схема 34).
Гломерулонефрит, обусловленный образованием антител к антигенам базальной мембраны клубочков,развивается довольно редко. Наиболее ярким его примером является синдром Гудпасчера, при котором в базальной мембране обнаружен нефритогенный антиген. Образование в клубочках аутоантигенов, стимулирующих возникновение соответствующих аутоантител, может быть обусловлено действием металлов (золото, литий), лекарственных препаратов, ионизирующей радиации. Как и при иммунокомп-лексном варианте, при аутоиммунном гломеру-лонефрите происходят повреждение базальной мембраны капилляров клубочков и активация различных факторов, стимулирующих в конечном счете развитие воспаления. Ряд экспериментальных наблюдений свидетельствует о том, что повреждение клубочков может быть связано и с активацией клеточно-опосредованного иммунитета. У людей участие Т-клеток было установлено в развитии как пролиферативного, так и не-пролиферативного гломерулонефрита. Лечение циклоспорином, ингибитором функции Т-лимфоцитов, является эффективным при некоторых заболеваниях почечных клубочков у человека.
По течениюразличают несколько форм гло-мерулонефритов: асимптоматическую гематурию, острый гломерулонефрит, быстропрогрессирую-щий и хронический гломерулонефриты.
Асимптоматическая гематурияхарактеризуется микро- и макроскопически обнаруживаемым наличием крови в моче у пациентов с нормальной функцией почек. У многих, но не у всех больных выявляется протеинурия (менее 1,5 г/ сут). В большинстве случаев в основе этого заболевания лежит иммуноглобулин А - нефропа-тия,которая характеризуется отложением в почечных клубочках иммуноглобулина А, связанного с Са-комплементом. В результате развивается фокальный, или сегментарный, гломерулонефрит. У 20-40 % таких больных в сроки от 5 до 25 лет развивается конечная стадия хронической почечной недостаточности.
Острый гломерулонефрит.Это заболевание характеризуется острым началом, большой гематурией, олигурией, острой почечной недостаточностью, проявляющейся внезапным снижением скорости клубочковой фильтрации. Происходит задержка жидкости в организме, что сопровождается отеками и гипертензией. Содержание белка в суточной моче обычно менее 3 г. Любая инфекция с разной частотой может ос-
Часть III. ПАТОФИЗИОЛОГИЯ ОРГАНОВ И СИСТЕМ

 |
ложниться развитием острого нефрита, но наиболее частой формой является постстрептококковый гломерулонефрит, который осложняет различные виды стрептококковой инфекции, причем наиболее частым нефритогенным возбудителем являются стрептококки группы А (особенно тип 12). В развитии заболевания играют роль переохлаждение и генетическая предрасположенность. Болеют в основном дети. В большинстве случаев заболевание заканчивается спонтанным выздоровлением.
Быстропрогрессирующий гломерулонефрит составляет 2-4% всех случаев гломерулонефри-га. Основные его проявления - гематурия, про-теинурия, быстрое снижение функций почек, которое может привести к конечной стадии почечной недостаточности в течение нескольких цней или недель. Может быть результатом первичного поражения почечных клубочков или проявлением системного заболевания (васкули-гы, системная красная волчанка, криоглобули-немия). В половине случаев отложение иммунных комплексов в клубочках не происходит. Выявлена связь этой разновидности гломеруло-нефрита с образованием антител к цитоплазме нейтрофилов. При световой микроскопии обнаруживаются полулунные пролифераты в капсуле Боумена вокруг клубочков.
Хронический диффузный гломерулонефритпредставляет собой медленно прогрессирующее воспаление почечных клубочков, завершающееся замещением их фиброзной тканью и развитием хронической почечной недостаточности. Может быть следствием острого, но чаще возника-
ет первично. Довольно часто хронический гломерулонефрит является осложнением системной красной волчанки и гепатита С.
При иммунофлюоресцентной микроскопии обнаруживаются отложения иммунных комплексов в клубочках субэндотелиально и в области мезангиума, а также часто под эпителием. Кли-нико-лабораторными признаками этого заболевания являются гематурия, лейкоцитурия, про-теинурия, гиперазотемия. Одним из надежных показателей прогрессирующего заболевания почек считается содержание креатинина в сыворотке крови (более 212 мкмоль/л). Плохим прогностическим признаком является также наличие гипертензии. В ряде случаев болезнь может длительное время протекать в скрытой форме. Постепенно нарастают симптомы почечной недостаточности, завершающиеся уремией.
ПИЕЛОНЕФРИТ
Пиелонефрит(от греч. pyelos - лоханка) представляет собой неспецифическое инфекционное воспаление почечной лоханки с системой чашечек и интерстициальной ткани почки, преимущественно в области мозгового слоя. Процесс может быть одно- и двухсторонним. Пиелонефрит наиболее частое заболевание почек.
Причинами развития пиелонефрита являются преимущественно кишечная палочка, стафилококк, протей, псевдомонас, реже - стрептококк, энтерококк и др. В большинстве случаев играет роль смешанная инфекция. В зависимости от путей поступления инфекции различают пиело-
нефрит гематогенныйи уриногенный.В последнем случае инфекция поступает в мочеточник, а затем в лоханку из нижележащих отделов мочеполового тракта путем заброса инфицированной мочи. В этом случае способствующим фактором является затруднение для ее оттока. Развитием пиелонефрита могут осложняться сахарный диабет, подагра, миеломная болезнь.
По течению пиелонефрит подразделяют на острый и хронический. Острый пиелонефритможет быть гнойным или серозным. Он протекает как острое лихорадочное заболевание, осложняющееся иногда бактериальным шоком (результат действия микробных эндотоксинов) и развитием острой почечной недостаточности. Обнаруживаются повышенная СОЭ и лейкоцитоз со сдвигом влево. В осадке мочи содержатся лейкоциты, цилиндры, единичные эритроциты. Имеются резкие боли в области поясницы.
Хронический пиелонефритможет быть следствием острого или возникает первично. Наряду с воспалением лоханки происходит массивная воспалительная инфильтрация ткани почки в области мозговой зоны, сопровождающаяся обструкцией дистальных канальцев и дилатацией и атрофией проксимальных. Имеют место прогрессирующий фиброз игиалиноз интерстици-альной ткани, что может привести к сморщиванию почки.
В ряде случаев обнаруживается умеренная лейкоцитурия с появлением активных лейкоцитов, бактериурия, иногда микрогематурия и про-теинурия (до 1 г/сут). Вследствие поражения канальцев может происходить повышенная потеря с мочой натрия. Экстраренальные нарушения могут выражаться в развитии артериальной гипертонии и гипохромной анемии, нейтрофиль-ного лейкоцитоза со сдвигом влево и увеличения СОЭ. Следует иметь в виду, что заболевание может протекать годами в латентной форме, почти бессимптомно или с минимальными клиническими нарушениями. Функция почек может являться достаточной в течение долгого времени, но при двухстороннем поражении в конечном итоге развивается хроническая почечная недостаточность.
Принципы лечения пиелонефрита.Основное значение имеет комплексная противомикробная терапия (сульфаниламиды, антибиотики идр.), ускорение оттока мочи. Лечение должно быть длительным, противорецидивным.
