Кора надпочечников. минералокортикоиды
В коре надпочечников имеются три зоны: наружная — клубочковая, или гломеруляр-ная, средняя — пучковая, или фасцикулярная, и внутренняя—сетчатая, или ретикулярная. Считается, что во всех этих зонах продуцируются стероидные гормоны, источником для которых служит холестерин.
В клубочковой зоне в основном продуцируются минералокортикоиды, в пучковой — глюкокортикоиды, а в сетчатой — андрогены и эстрогены, т. е. половые гормоны.
К группе минералокортикоидов относятся: альдостерон, дезоксикортикостерон, 18-ок-сикортнкостерон, 18-оксидезоксикортикостерон. Основной представитель минералокортикоидов — альдостерон.
Механизм действия альдостерона связан с активацией синтеза белка, участвующего в реабсорбции ионов натрия. Этот белок можно назвать как калий-натрий-активируемая АТФ-аза, или белок, индуцированный альдостероном. Место действия (клетки-мишени) — это эпителий дистальных канальцев почки, в которых за счет взаимодействия альдостерона с альдостероновыми рецепторами повышается продукция мРНК и рРНК и активируется синтез белка — переносчика натрия. В результате этого почечный эпителий усиливает процесс обратного всасывания натрия из первичной мочи в интерстициальную ткань, а оттуда — в кровь. Механизм активного транспорта натрия (из первичной мочи в интерстиций) сопряжен с противоположным процессом — экскрецией калия, т. е. удалением ионов калия из крови в конечную мочу. В процессе реабсорбции натрия пассивно возрастает и реабсорб-ция воды. Таким образом, альдостерон является натрийсберегающим, а также калийурети-ческим гормоном. За счет задержки в организме ионов натрия и воды альдостерон способствует повышению уровня артериального давления.
Альдостерон также влияет на процессы реабсорбции натрия в слюнных железах. При обильном потоотделении альдостерон способствует сохранению натрия в организме, препятствует его потере не только с мочой, но и с потом. Калий же, наоброт, с потом удаляется при действии альдбстерона.
Регуляция продукции альдостерона осуществляется с помощью нескольких механизмов: главный из них — ангиотензиновый — под влиянием ангиотензина-Н (а его продукция возрастает под влиянием ренина — см. выше), повышается продукция альдостерона. Второй механизм — повышение продукции альдостерона под влиянием АКТГ, но в этом случае усиление выброса альдостерона намного меньше, чем под влиянием ангиотензина-И. Третий механизм — за счет прямого влияния натрия и калия на клетки, продуцирующие альдостерон. Не исключено существование других механизмов (простагландинового, ки-нинового и пр.). Выше уже отмечалось, что натрийуретический гормон, или атриопептин, является антагонистом альдостерона: он, во-первых, сам по себе снижает реабсорбцию натрия, а во-вторых, блокирует продукцию альдостерона и механизм его действия.
ГЛЮКОКОРТИКОИДЫ
Среди различных глюкокортикоидов наиболее важными являются кортизол, кортизон, кортикостерон, 11-дезоксикортизол, 11-дегидрокортикостерон. Наиболее сильный физиологический эффект принадлежит кортизолу.
В крови глюкокортикоиды на 95% связываются с альфа-2-глобулинами. Этот транспортный белок получил название транскортин, или кортикостероидсвязывающий глобулин. До 5% глюкокортикоидов связывается с альбумином. Эффект глюкокортикоидов определяется свободной его порцией. Метаболизируются глюкокортикоиды в печени под влиянием ферментов 5-6ета- и 5-альфа-редуктазы.
Физиологические эффекты глюкокортикоидов весьма разнообразны. Часть из них представляют собой полезный для организма эффект, позволяющий организму выживать в условиях критических ситуаций. Часть эффектов глюкокортикоидов является своеобразной платой за спасение.
Итак:
1) Глюкокортикоиды вызывают повышение содержания в крови глюкозы (поэтому —
соответствующее название). Это повышение происходит за счет того, что гормоны вызыва
ют активацию глюконеогенезз — образование глюкозы из аминокислот и жирных кислот.
Этот процесс происходит в печени за счет того, что глюкокортикоиды, соединяясь в гепато-
цитах с соответствующими рецепторами, попадают в ядра, где вызывают активацию про
цесса транскрипции — повышение уровня мРНК и рРНК, активацию синтеза белков-фер
ментов, участвующих в процессах глюконеогенеза — тирозинаминотрансферазы, трипто-
фанпирролазы, серинтреониндегидратаэы и т. д. Одновременно в других органах и тканях,
в частности, в скелетных мышцах глюкокортикоиды тормозят синтез белков для того, что
бы создать депо аминокислот, необходимых для глюконеогенеза.
2) Глюкокортикоиды вызывают активацию липолиза для появления еще одного источни
ка энергии — жирных кислот.
Итак, главный эффект глюкокортикоидов — это мобилизация энергетических ресурсов организма.
3) Глюкокортикоиды угнетают все компоненты воспалительной реакции — уменьшают
проницаемость капилляров, тормозят экссудацию, снижают интенсивность фагоцитоза. Это
свойство используется в клинической практике — для снятия воспалительных реакций, на
пример, после проведения операции на глазу по поводу катаракты больному рекомендуется
ежедневно вводить глазные капли, содержащие глюкокортикоиды (кортизон, гидрокортизон).
4) Глюкокортикоиды резко снижают продукцию лимфоцитов (Т- и В-) в лимфоидной
ткани — при массивном повышении уровня в крови глюкокортикоидов наблюдается опус
тошение тимуса, лимфатических узлов, снижение в крови уровня лимфоцитов. Под влияни
ем глюкокортикоидов снижается продукция антител, уменьшается активность Т-киллеров,
снижается интенсивность иммунологического надзора, снижается гиперчувствительность
и сенсибилизация организма. Все это позволяет рассматривать глюкокортикоиды как ак
тивные иммунодепрессанты. Это свойство глюкокортикоидов широко используется в кли
нической практике для купирования аутоиммунных процессов, для снижения иммунной
защиты организма хозяина и т. п. В то же время получены данные о том, что из-за депрессии
иммунологического надзора возрастает опасность и вероятность развития опухолевого
процесса, т. к. появляющиеся ежедневно опухолевые клетки не могут эффективно элими
нироваться из организма в условиях повышенного уровня глюкокортикоидов.
5) Глюкокортикоиды, вероятно, повышают чувствительность гладких мышц сосудов к
катехоламинам, поэтому на фоне глюкокортикоидов повышается спазм сосудов, особенно
мелкого калибра, и возрастает артериальное давление. Это свойство глюкокортикоидов,
вероятно, лежит в основе таких явлений, как язвы желудка и двенадцатиперстной кишки,
нарушение микроциркуляции в сосудах миокарда и как следствие — развитие аритмий, на
рушение физиологического состояния кожных покровов — экземы, псориаз.
Все эти явления наблюдаются в условиях повышенного содержания эндогенных глюкокортикоидов (при стресс-реакции) или в условиях длительного введения глюкокортикоидов с лечебной целью.
6) В низких концентрациях глюкокортикоиды вызывают повышение диуреза — за счет
увеличения скорости клубочковой фильтрации и, возможно, за счет угнетения выброса АДГ.
Но при высоких концентрациях глюкокортикоиды ведут себя как альдостерон — вызывают задержку натрия и воды в организме.
7) Глюкокортикоиды повышают секрецию соляной кислоты и пепсина в желудке, что
вместе с сосудосуживающим эффектом приводит к появлению язв желудка.
8) При избыточном количестве глюкокортикоиды вызывают деминерализацию костей,
остеопороз, потерю кальция с мочой, снижают всасывание кальция в кишечнике, ведут себя
как антагонист витамина Д3.
В этих же условиях вследствие торможения синтеза белка в скелетных мышцах наблюдается у человека мышечная слабость.
9) За счет активации липолиза при действии глюкокортикоидов повышается интенсив
ность перекисного окисления липидов (ПОЛ), что приводит к накоплению в клетках про
дуктов этого окисления, существенно нарушающих функцию плазматической мембраны.
10) Глюкокортикоиды влияют и на деятельность ЦНС, на функцию ВНД — они повыша
ют обработку информации, улучшают восприятие внешних сигналов, действующих на мно
гие рецепторы — вкусовые, обонятельные и т. п. Однако при недостатке и особенно при
избыточном содержании глюкокортикоидов наблюдаются существенные изменения в со
стоянии ВНД — вплоть до возникновения шизофрении (при длительном стрессе!).
Регуляция продукции глюкокортикоидов осуществляется за счет двух гормонов — кор-тиколиберина и АКТГ
Кортиколиберин представляет собой 41-аминокислотныЙ пептид, который продуцируется нейронами аркуатного, дорсомедиального, вентромедиального ядер гипоталамуса, но особенно его много продуцируется в паравентрикулярных ядрах гипоталамуса. Этот гормон, поступая через портальную систему в аденогипофиз, взаимодействует с кортнколибе-риновыми рецепторами клеток, продуцирующих АКТГ (гипофиз) и за счет цикла событий (активация аденилатциклазы, повышение внутриклеточной концентрации цАМФ, активация протеинкиназы, фосфорилирование белка), увеличивает продукцию и выброс АКТГ.
На продукцию кортиколиберина влияют многие факторы. Ее усиливают всевозможные стрессоры, которые через кору, лимбическую систему и ядра гипоталамуса влияют на кор-тиколиберинпродуцирующие нейроны. Аналогичный эффект вызывают ацетилхолин, серо-тонин, а также импульсы, идущие из центра суточной биоритмики — супрахиазматическо-го ядра гипоталамуса. Торможение продукции кортиколиберина происходит под влиянием ГАМК (гамма-аминомасляная кислота, компонент стресс-лимитирующеЙ системы!), нора-дреналина, мелатонина (гормон эпифиза) и за счет самих глюкокортикоидов: когда их концентрация в крови возрастает, то по механизму отрицательной обратной связи происходит торможение продукции кортиколиберина.
АКТГ продуцируется в аденогипофизе. Представляет собой 39-аминокислотныЙ пептид, который синтезируется из предшественника проопиомеланокортина.
Достигая клеток пучковой зоны коры надпочечников АКТГ взаимодействует со специфическими рецепторами, расположенными на этих клетках, активирует аденилатциклаэу, увеличивает внутриклеточную концентрацию цАМФ, повышает активность протеинкиназы, в результате чего возрастает ряд процессов:
а) АКТГ ускоряет поступление свободного холестерина из плазмы в клетки надпочеч
ников, усиливает синтез холестерина, активирует внутриклеточный гидролиз эфира холес
терина, в конечном итоге существенно повышает внутриклеточную концентрацию холес
терина;
б) усиливает активность фермента, переносящего холестерин в митохондрии, где осу
ществляется превращение холестерина в прегненолон;
в) усиливает скорость образования прегненолона в митохондриях из поступающего туда
холестерина;
г) за счет повышения синтеза белка (цАМФ — зависимая активация) нарастает масса
надпочечников, что повышает возможности органа как продуцента глюкокортикоидов;
д) одновременно АКТГ за счет взаимодействия с рецепторами жировой ткани вызывает
усиление лйполиза (побочный эффект АКТГ);
е) за счет способности АКТГ активировать переход тирозина в меланин под влиянием АКТГ происходит усиление пигментации.
Для продукции АКТГ характерна ритмичность, которая определяется ритмичностью выделения кортиколиберина; максимальная секреция либерина, АКТГ и глюкокортикоидов наблюдается утром в 6—8 часов, а минимальная — между 18 и 23 часами. Торможение продукции АКТГ происходит под влиянием самих глюкокортикоидов — кортизола и других. В тех случаях, когда надпочечники поражены (например, туберкулезный процесс), то из-за низкого содержания глюкокортикоидов гипофиз постоянно продуцирует в повышенных количествах АКТГ, что вызывает ряд эффектов, в том числе пигментацию (бронзовая болезнь).
Такая подробная информация о глюкокортикоидах, кортиколиберине, АКТГ обусловлена важностью этой системы в процессах жизнедеятельности организма, в том числе в процессах адаптации организма к действию неблагоприятных факторов среды, которые получили название стресс-реакции. Изучение проблемы стресса является одной из важных задач теоретической медицины.
СТРЕСС ИЛИ ОБЩИЙ АДАПТАЦИОННЫЙ СИНДРОМ
Учениео стрессе — один из ведущих разделов современной медицины. Основоположником этого направления является Ганс Селье (1907—1982 гг.), бывший студент Пражского университета, который в 1926 г. опубликовал первые наблюдения о больных, страдающих самыми разными соматическими недомоганиями. У всех таких больных наблюдалась потеря аппетита, мышечная слабость, повышенное артериальное давление, утрата мотивации к достижениям. Он обозначил эти симптомы как «синдром просто болезни». Одновременно он показал, что в организме у многих людей при болезни наблюдаются однообразные нарушения: изменения в коре надпочечников (гипертрофия, кровоизлияния), истощение лимфо-идной ткани (лимфатических узлов, тимуса), изъязвление желудка. Для описания совокупности всех неспецифических изменений внутри организма он ввел понятие «стресс». В последующем он долгие годы — до конца своей жизни — работал в институте экспериментальной медицины и хирургии в Монреале, который в последующем стал Международным институтом стресса.
В 1936 г. в известном журнале «Нейче» (Природа) в разделе «Письма к редактору» в небольшой по размеру статье Г. Селье сформулировал свое представление о стрессе и одновременно ввел новое понятие — «Синдром, вызываемый разными повреждающими агентами», или «общий адаптационный синдром», или «синдром биологического стресса». В нашей литературе иногда его называют «генерализованный адаптационный синдром».
Термин «стресс» взят из области физики, он отражает явление напряжения, давления или силы, прикладываемой к системе. Этот термин применялся и до Селье в художественной литературе. Так, английский поэт Роберт Маннинг в 1903 г. писал: «И эта мука была манной небесной, которую господь послал людям, пребывающим в пустыне 40 зим и находившимся в большом стрессе».
Современные определения стресса звучат так:
Стресс — это неспецифическая реакция организма на любое требование извне (Г. Селье, 1974).
Стресс — это реакция организма на значимый раздражитель. А по своей природе стрессовая реакция является психофизиологической.
Стресс — это способ достижения резистентности (устойчивости) организма при действии на него повреждающего фактора. Стресс одновременно является и способом тренировки защитных механизмов организма.
По мнению Селье и его сторонников, стресс — это врожденный защитный механизм, который на ранних этапах эволюции дал возможность человеку выжить в первобытных условиях; стрессовая реакция позволяет подготовиться организму к возбуждению.
 |
Итак, в нормальном здоровом организме человека существует механизм, направленный на борьбу с неблагоприятным фактором, воздействие которого может привести к гибели организма. Этот механизм и получил название стресс-реакция, или общий адаптационный синдром.
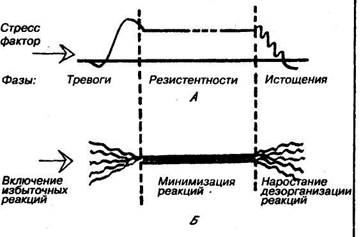
| Рис. 47. Схематическое представление о формировании фаз реакции на стрессовый раздражитель (по Г. Селье). А — изменения общего энергетического уровня на протяжении фаз. Б — характерная динамика количественного включения реакций и систем в ходе развития фаз стресса. |
Виды стресса. Различают стресс острый и хронический. В первом случае механизмы защиты включаются на короткое время — на момент действия раздражителя-стрессора, во втором случае стрессор действует длительно, и поэтому реакция на него, механизм защиты от этого стрессора имеет свои особенности, что потребовало введения понятия «хронический стресс». Различают физический стресс и эмоциональный (психогенный) — в первом случае имеет место защита от воздействия физических факторов (ожог, травма, сверхсильный шум), во втором случае — защита от психогенных факторов, вызывающих отрицательные эмоции.
Г. Селье ввел также понятия — эустресс и дистресс. Эустресс—это (дословно) — хоро
ший стресс, защитная реакция протекает без потерь для организма, безболезненно, дис
тресс — (дословно) — это чрезмерный стресс, защита от повреждающего фактора происхо
дит с ущербом для организма, с ослаблением его возможностей. Ясно, что чем выше интен
сивность стрессорного воздействия, тем выше вероятность перехода эустресса в дистресс.
Стрессоры. В современной литературе под этим термином понимают все факторы внеш
ней или внутренней среды, которые вызывают реакцию стресс, такие факторы, которые яв
ляются опасными для здоровья и целостности организма. К таким факторам относят следу
ющие ситуации: #
1) вредные стимулы окружающей среды (загазованность, высокий уровень радиации,
неблагоприятный микроклимат, например, охлаждающий или жаркий климат и т. д.);
2) нарушение физиологических процессов в организме, например, при различных забо
леваниях, в том числе — инфекционных, соматических и т. п.;
3) необходимость ускоренной обработки информации, т. е. работа в условиях дефицита
времени;
4) работа в условиях риска для собственной жизни или жизни других людей;
5) осознаваемая угроза жизни;
6) изоляция и заключение;
7) остракизм (изгнание, гонение), групповое давление;
8) отсутствие контроля над событиями;
9) отсутствие цели в жизни;
