Гиперфункция передней доли гипофиза
Избыточная секреция соматотропного гормона(гормон роста). Избыточная секреция этого гормона наблюдается чаще всего при эозинофильной аденоме гипофиза.
Клинически это проявляется развитием акромегалиии гигантизма(рис. 20-10). Акромегалия - заболевание у людей с закончившимся ростом, проявляющееся диспропорциями скелета, мягких тканей (увеличение размеров кистей, стоп, носа, ушей, нижней челюсти) (рис. 20-11), кифосколиозом, спланхномегалией (увеличение размера внутренних органов). Избыточная секреция СТГ в детском возрасте приводит к развитию гигантизма, сопровождающегося увеличением роста более 190 см в сочетании с признаками акромегалии. В 90% случаев развитие акромегалии и гигантизма связано с наличием гормонально-активной эозинофильной адено-
 Рис. 20-10.Акромегалический гигантизм у больного 25 лет, рост 220 см (вокруг стоят люди нормального роста). Случай Ланнуа и Роя (по Н.А. Шерешевскому)
Рис. 20-10.Акромегалический гигантизм у больного 25 лет, рост 220 см (вокруг стоят люди нормального роста). Случай Ланнуа и Роя (по Н.А. Шерешевскому)
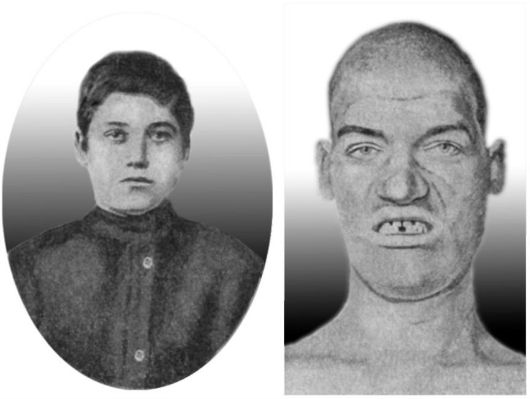 Рис. 20-11.Юноша 16 лет до заболевания акромегалией. Тот же человек в 20-летнем возрасте во время болезни (по W. Schultze, 1904)
Рис. 20-11.Юноша 16 лет до заболевания акромегалией. Тот же человек в 20-летнем возрасте во время болезни (по W. Schultze, 1904)
мы гипофиза. В ряде случаев опухоль не обнаруживается, а развитие гиперплазии гипофиза может быть объяснено, по-видимому, либо избыточной секрецией соматолиберина, либо недостаточной секрецией соматостатина, возникающей в результате повреждения гипоталамуса. Такими повреждениями могут быть травмы (в том числе родовые), инфекции (вирусные инфекции, скарлатина, сыпной тиф, туберкулез, сифилис), нарушения кровообращения. Увеличенное образование СТГ приводит к нарушению обмена белков, углеводов и жиров.
Нарушения белкового обмена.Усиление роста свидетельствует об активации синтеза белков или торможении их разрушения. Действительно, введение СТГ животным вызывает задержку азота в организме, положительный азотистый баланс и понижение распада белков. При этом установлено увеличение включения разных аминокислот в белки тканей и снижение отношения остаточного азота к белковому.
Считается, что действие СТГ опосредовано действием пептидных ростовых факторов - инсулиноподобных факторов роста (ИФР), синтезируемых в тканях и прежде всего в печени. Именно с их действием связывают такие анаболические эффекты, как:
1) стимуляция включения SO4 в протеогликаны;
2) стимуляция включения тимидина в ДНК;
3) стимуляция синтеза РНК;
4) стимуляция синтеза белка СТГ.
Анаболический эффект СТГ обусловливают два момента:
1. Наличие инсулина. На фоне экспериментального диабета у животных и сахарного диабета у людей СТГ обычно не усиливает синтеза белков. Очевидно, это связано с тем, что инсулин активирует обмен углеводов и стимулирует синтез белка.
2. Концентрация глюкокортикоидов. Малые их дозы способствуют реализации анаболического эффекта СТГ, а большие дозы, наоборот, тормозят анаболический эффект СТГ и задерживают рост, что может быть связано с тем, что кортизол в больших дозах угнетает образование ИФР. У больных с эозинофильной аденомой гипофиза часто усилена продукция глюкокортикоидов. Не исключено, что это один из компенсаторных процессов, направленных на ограничение эффекта избыточных количеств СТГ.
Нарушение углеводного обмена.Это нарушение имеет различную степень выраженности. В своей крайней форме проявляется в виде сахарного диабета. Механизм этих нарушений сложен и включает участие следующих факторов:
а) СТГ активирует выход глюкозы из печени за счет активации секреции глюкагона альфа-клетками островков поджелудочной железы, который усиливает гликогенолиз;
б) в поджелудочной железе СТГ стимулирует продукцию инсулина, что усиливает утилизацию глюкозы тканями, однако на уровне клеток тканей СТГ совместно с глюкокортикоидами выступает как антагонист инсулина, т.е. тормозит поглощение глюкозы. Механизм торможения связан с активацией ингибирующей активности β-липопротеиновой фракции сыворотки крови, которая угнетает гексокиназную реакцию, являющуюся пусковой в углеводном обмене;
в) СТГ активирует инсулиназу печени, расщепляющую инсулин. Конечный результат влияния СТГ на углеводный обмен зависит от всех указанных факторов.
Нарушение жирового обмена.СТГ активирует липолиз в жировой ткани, что ведет к увеличению содержания свободных неэстерифицированных жирных кислот в крови, их накоплению в печени и окислению. Усиление окисления выражается, в частности, в увеличении образования кетоновых тел. Этот катаболический эффект осуществляется в присутствии небольших концентраций глюкокортикоидов. Увеличение их количества тормозит мобилизацию жира и его окисление СТГ.
Избыточная секреция адренокортикотропного гормона.Повышенная секреция АКТГ гипофизом приводит к развитию болезни Иценко-Кушинга,которая проявляется двусторонней гиперплазией надпочечников и повышенной секрецией гормонов коры надпочечников. От болезни Иценко-Кушинга следует отличать синдром Иценко-Кушинга,имеющий аналогичную клиническую картину, но обусловленный гормонально-активной аденомой или аденокарциномой коры надпочечников, а также злокачественными опухолями вненадпочечниковой локализации, продуцирующими АКТГ-подобные пептиды (например, бронхогенный рак легких).
В 1924 г. Н.М. Иценко опубликовал наблюдение за больными со следующими признаками: изменение очертаний лица (ожирение его нижней части), перераспределение жира (ожирение туловища при отсутствии ожирения конечностей), мраморность кожных покровов, стрии (багрово-синюшные полосы) на передней стенке живота и бедрах, атрофия мышц конечностей и увеличение живота, повышение артериального давления, остеопороз, нарушение половых функций. Патологоанатомически Н.М. Иценко в ряде случаев определял изменения в гипоталамусе, что и позволило ему связать наблюдаемую клиническую картину с этими изменениями.
В 1932 г. Кушинг описал ту же клиническую картину, связав ее с базофильной аденомой гипофиза. В настоящее время вопрос этиологии болезни Иценко-Кушинга все еще не решен. Было установлено, что данное заболевание возникает на фоне развития стресса, нейроинфекций, травм мозга, абортов, родов, полового созревания и чрезмерной физической нагрузки. По-видимому, действие этих факторов опосредуется через центральные нейромедиаторы (ацетилхолин, серотонин, норадреналин и др.), которые, в свою очередь, регулируют секрецию кортиколиберина в гипоталамусе. В патогенезе болезни Иценко-Кушинга может иметь значение невосприимчивость нейронов мозга к ингибирующим влияниям механизма обратной связи, развивающаяся и закрепляющаяся в результате повреждения гипоталамуса и высших отделов ЦНС. Так или иначе продукция кортиколиберина в гипоталамусе увеличивается, что приводит к гиперплазии базофильных клеток гипофиза, вырабатывающих повышенные количества АКТГ. Если причина, вызвавшая повышение продукции кортиколиберина, сохраняется длительно, то гиперплазия превращается в микроаденому, а затем и в аденому. Повышенный уровень АКТГ при этом заболевании
сочетается с повышением уровня и других продуктов проопиомеланокортина.
Избыточно образующийся АКТГ оказывает свое действие двояко: а) через надпочечники и б) вненадпочечниковым путем.
В надпочечниках АКТГ стимулирует пучковую и (в меньшей степени) сетчатую зону, усиливая образование главным образом кортизола и кортикостерона, выражением чего является гиперкортизолизм.
Избыточная секреция глюкокортикоидов, в свою очередь, приводит к развитию гипергликемии, поскольку она угнетает утилизацию глюкозы на периферии и усиливает глюконеогенез. Следствием этого является повышенная секреция инсулина, чувствительность к которому в тканях снижается. Усиливая образование кортизола, АКТГ тем самым увеличивает катаболизм белка. С повышенным распадом белка связано развитие ряда симптомов заболевания, таких, как остеопороз (деградация белковой матрицы кости), мышечная слабость (атрофия мышц), стрии.
Избыток кортизола приводит помимо этого к задержке натрия и воды, а также синергически с катехоламинами кортизол действует на периферические сосуды, что вызывает их спазм. Все это приводит к развитию артериальной гипертонии. Повышенное выведение калия способствует развитию мышечной слабости. Избыток кортизола может быть в некоторой степени причиной развития гирсутизма (избыточного оволосенения) у больных женщин.
Вненадпочечниковое действие АКТГ на некоторые обменные процессы отличается от его действия на эти же процессы через усиление секреции кортизола. Так, АКТГ способен увеличивать активность тирозиназы в меланоцитах, что приводит к такому нередкому клиническому признаку заболевания, как гиперпигментация. На жировой обмен АКТГ воздействует следующим образом: добавление его непосредственно к жировой ткани стимулирует ее липолитическую активность (распад жира) и тем самым мобилизацию жира с образованием свободных высших неэстерифицированных жирных кислот. Однако усиливая образование кортизола, АКТГ оказывает следующее влияние: а) тормозит мобилизацию жира; б) активирует глюконеогенез и тем самым способствует образованию жира; в) тормозит действие СТГ, активирующее окисление жира. Очевидно, конечный результат зависит от соотношения надпочечникового и вненадпочечникового действия гормона.
Избыточная секреция тиреотропного гормона.Избыточное образование ТТГ стимулирует функцию щитовидной железы, что приводит к усиленному образованию тиреоидных гормонов, развитию так называемого вторичного гипертиреоза и тиреотоксикоза (см. ниже). Кроме того, ТТГ увеличивает содержание кислых мукополисахаридов в коже, мышцах и ретроорбитальной клетчатке как интактных, так и тиреоидэктомированных животных. Причиной данного нарушения могут выступать аденомы из базофильных клеток, секретирующих тиротропин. Они являются редкой формой опухолей передней доли гипофиза. В этом случае к симптоматике гипертиреоза и токсикоза прибавляются и офтальмологические нарушения (изменение полей зрения и глазного дна), возникающие вследствие сдавливания опухолью перекреста зрительного нерва при выходе ее за пределы турецкого седла.
Избыток кортизола приводит помимо этого к задержке натрия и воды, а также синергически с катехоламинами кортизол действует на периферические сосуды, что вызывает их спазм. Все это приводит к развитию артериальной гипертонии. Повышенное выведение калия способствует развитию мышечной слабости. Избыток кортизола может быть в некоторой степени причиной развития гирсутизма (избыточного оволосенения) у больных женщин.
Вненадпочечниковое действие АКТГ на некоторые обменные процессы отличается от его действия на эти же процессы через усиление секреции кортизола. Так, АКТГ способен увеличивать активность тирозиназы в меланоцитах, что приводит к такому нередкому клиническому признаку заболевания, как гиперпигментация. На жировой обмен АКТГ воздействует следующим образом: добавление его непосредственно к жировой ткани стимулирует ее липолитическую активность (распад жира) и тем самым мобилизацию жира с образованием свободных высших неэстерифицированных жирных кислот. Однако усиливая образование кортизола, АКТГ оказывает следующее влияние: а) тормозит мобилизацию жира; б) активирует глюконеогенез и тем самым способствует образованию жира; в) тормозит действие СТГ, активирующее окисление жира. Очевидно, конечный результат зависит от соотношения надпочечникового и вненадпочечникового действия гормона.
Избыточная секреция тиреотропного гормона.Избыточное образование ТТГ стимулирует функцию щитовидной железы, что приводит к усиленному образованию тиреоидных гормонов, развитию так называемого вторичного гипертиреоза и тиреотоксикоза (см. ниже). Кроме того, ТТГ увеличивает содержание кислых мукополисахаридов в коже, мышцах и ретроорбитальной клетчатке как интактных, так и тиреоидэктомированных животных. Причиной данного нарушения могут выступать аденомы из базофильных клеток, секретирующих тиротропин. Они являются редкой формой опухолей передней доли гипофиза. В этом случае к симптоматике гипертиреоза и токсикоза прибавляются и офтальмологические нарушения (изменение полей зрения и глазного дна), возникающие вследствие сдавливания опухолью перекреста зрительного нерва при выходе ее за пределы турецкого седла.
Избыточная секреция гонадотропных гормонов.К их числу относятся: а) ФСГ (фоллитропин); б) ЛГ (лютропин), или ГСИК; в) пролактин, или лактотропный гормон. Их секреция тесно связана с функцией гипоталамуса. В гипоталамусе выделяются соответствующие либерины, которые, спускаясь в гипофиз, стимулируют там образование ФСГ и ЛГ (ГСИК). Образование же пролактина при этом тормозится. Повреждение срединного возвышения, как и гипофизэктомия, ведет к уменьшению секреции ГТГ и к атрофии половых желез. Наоборот, повреждение задних образований гипоталамуса вызывает усиление секреции ГТГ и в детском возрасте приводит к преждевременному половому созреванию. Определенное значение в патогенезе одного из видов преждевременного полового созревания - макрогентосомиипридают нарушению функции шишковидной железы, так как считают, что в физиологических условиях она до определенного возраста тормозит секрецию ГТГ, поскольку мелатонин, секретируемый эпифизом, угнетает секрецию гонадотропинов. Преждевременное угнетение функции этой железы (гипопинеализм)растормаживает секрецию ГТГ и приводит к раннему половому созреванию. Согласно другим представлениям, имеют значение опухоли подбугорья вообще, которые каким-то образом стимулируют секрецию ГТГ гипофизом. Секреция ГТГ увеличивается и при первичном выпадении инкреторной активности половых желез, однако это не ведет к повышению продукции половых гормонов.
Избыточное образование пролактина отмечено у больных синдромом лактореи - аменореи, возникающим в связи с первичным
повреждением гипоталамуса. При этом нередко находят опухоль гипоталамуса или хромофобную аденому гипофиза.
