Магнитные свойства атома
Магнетизм атома порождается тремя причинами:
· орбитальным движением электронов, создающим орбитальный механический 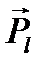 и магнитный момент
и магнитный момент 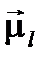 каждого из них;
каждого из них;
· спиновыми свойствами электрона – существованием у него собственных механического 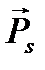 и магнитного
и магнитного 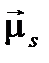 моментов;
моментов;
· такими же свойствами многих атомных ядер, обладающих собственными механическим 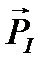 и магнитным
и магнитным 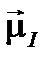 моментами.
моментами.
Обращение каждого электрона вокруг ядра представляет собой аналог кругового тока силой 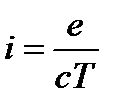 , создающего орбитальный магнитный момент
, создающего орбитальный магнитный момент
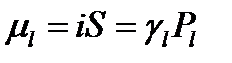 , (1.1)
, (1.1)
где S – площадь контура, обегаемого электроном;
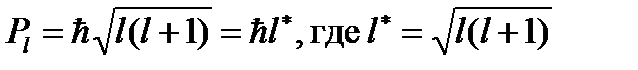
механический момент орбитального движения электрона; l – орбитальное квантовое число, а
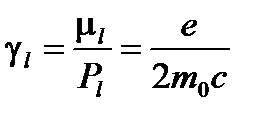 (1.2)
(1.2)
так называемое гиромагнитное отношение орбитального движения электрона[2].
Складываясь векторно, орбитальные магнитные моменты всех электронов атома образуют результирующий магнитный момент 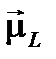 всей электронной оболочки:
всей электронной оболочки:
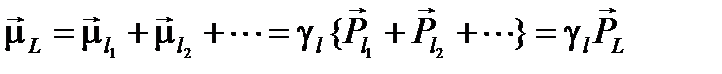 (1.3)
(1.3)
Здесь
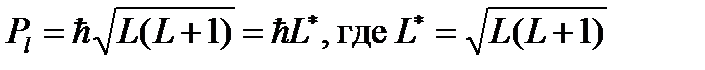
– суммарный орбитальный механический момент атом; L – орбитальное квантовое число атома.
Спиновый магнитный момент 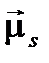 электрона связан с его механическим моментом
электрона связан с его механическим моментом 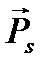 соотношением
соотношением
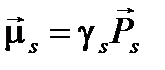 , (1.4)
, (1.4)
где
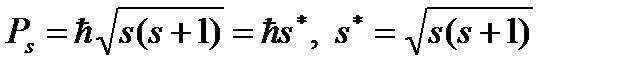
– спиновый механический момент электрона; s – спиновое квантовое число, а
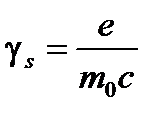 (1.5)
(1.5)
– его спиновое гиромагнитное отношение. Оно, как видим, вдвое больше аналогичной величины для орбитального движения:
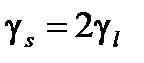 . (1.6)
. (1.6)
Это обстоятельство получило в свое время название гиромагнитной аномалии и, хотя с современной точки зрения здесь нет ничего аномального, название удержалось до сих пор.
Сумма спиновых магнитных моментов всех электронов оболочки образует результирующий спиновый магнитный момент 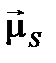 атома:
атома:

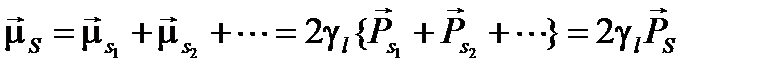 (1.7)
(1.7)
где 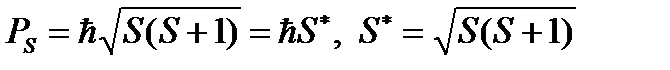 .
.
Здесь 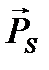 – суммарный спиновый механический момент атома; S – спиновое квантовое число атома.
– суммарный спиновый механический момент атома; S – спиновое квантовое число атома.
Если в формулах (1.1) и (1.4) заменить входящие в них величины соответствующими значениями, то получим для орбитального и спинового магнитных моментов электрона соотношения:
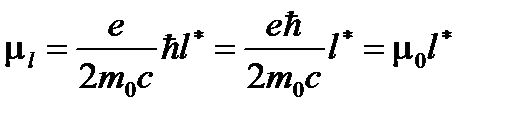 , (1.8)
, (1.8)
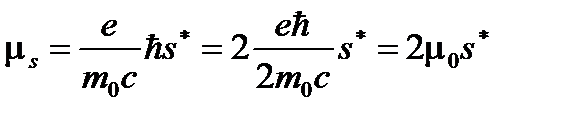 . (1.9)
. (1.9)
Величина
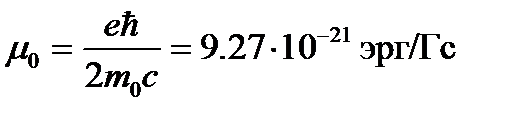 (1.10)
(1.10)
называется магнетоном Бора и служит единицей для измерения атомных магнитных моментов.
Квантовые числа l и s принимают значения:
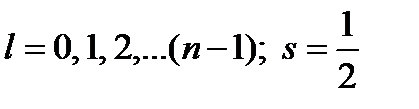 (1.11)
(1.11)
где n = 1, 2, 3,… – главное квантовое число.
Это значит, что спиновый магнитный момент электрона приблизительно равен двум магнетонам Бора:
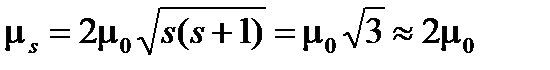 , (1.12)
, (1.12)
в то время как его орбитальный магнитный момент имеет величины разные для различных состояний электрона в атоме, причем при
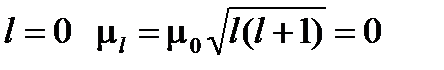
Заметим, что равенство (1.12) не имеет большого физического значения, поскольку в эксперименте проявляется не 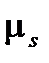 , a его проекция на заданное полем направление; проекция же эта, как показывают данные, равна по абсолютной величине одному магнетону Бора
, a его проекция на заданное полем направление; проекция же эта, как показывают данные, равна по абсолютной величине одному магнетону Бора 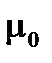 (см. формулу (1.14)).
(см. формулу (1.14)).

Магнитные моменты 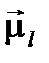 и
и 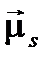 ориентированы антипараллельно соответствующим механическим моментам
ориентированы антипараллельно соответствующим механическим моментам 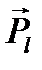 и
и 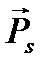 , так как заряд электрона отрицателен (см. рис. 1).
, так как заряд электрона отрицателен (см. рис. 1).
Рис. 1. Механические и магнитные моменты электрона в атоме
Направления 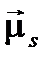 и
и 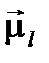 . относительно друг друга (так же, как направления квантовых векторов вообще относительно заданной оси в пространстве) определяются правилами пространственного квантования: можно точно указать значение проекции квантового вектора на заданную ось, но нельзя одновременно с тем определить другие компоненты этого вектора. Проекции орбитального и спинового механических и магнитных моментов электрона на ось, заданную направлением постоянного намагничивающего поля
. относительно друг друга (так же, как направления квантовых векторов вообще относительно заданной оси в пространстве) определяются правилами пространственного квантования: можно точно указать значение проекции квантового вектора на заданную ось, но нельзя одновременно с тем определить другие компоненты этого вектора. Проекции орбитального и спинового механических и магнитных моментов электрона на ось, заданную направлением постоянного намагничивающего поля 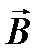 , соответственно равны:
, соответственно равны:
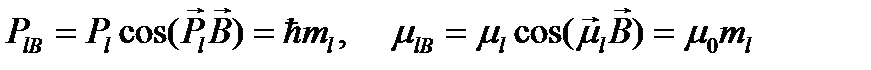 , (1.13)
, (1.13)
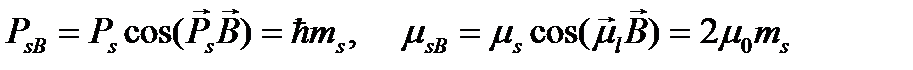 , (1.14)
, (1.14)
где 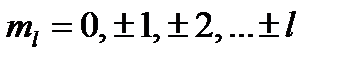 – орбитальное магнитное квантовое число электрона;
– орбитальное магнитное квантовое число электрона; 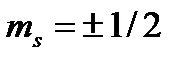 – его спиновое магнитное квантовое число.
– его спиновое магнитное квантовое число.
Таким образом, орбитальные механический и магнитный моменты 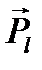 и
и 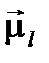 могут относительно поля
могут относительно поля 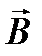 принимать 2l+1 различные ориентации, а их проекции
принимать 2l+1 различные ориентации, а их проекции 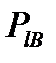 и
и 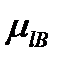 имеют 2l+1 возможные значения.
имеют 2l+1 возможные значения.
Проекции вектора 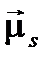 направлены либо вдоль
направлены либо вдоль 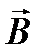 , либо против него и равны
, либо против него и равны 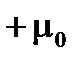 и
и 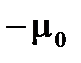 соответственно.
соответственно.
Сумма результирующих орбитального 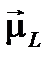 и спинового
и спинового 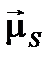 магнитных моментов атома определяет его результирующий магнитный момент:
магнитных моментов атома определяет его результирующий магнитный момент:
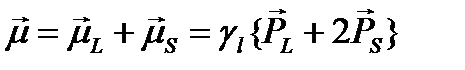 . (1.15)
. (1.15)
Поскольку полный механический момент атома 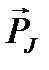 равен
равен
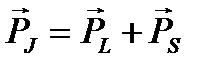 , (1.16)
, (1.16)
где
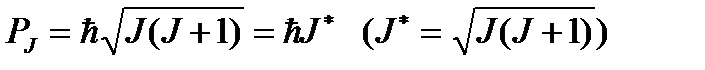 , (1.17)
, (1.17)
(J – внутреннее квантовое число атома, применяющее значения из ряда J = L+S, L+S–1, …, L–S), то из (1.15) и (1.16) следует, что вектор 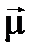 составляет с вектором
составляет с вектором 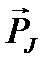 угол, отличный от 180° (следствие гиромагнитной аномалии).
угол, отличный от 180° (следствие гиромагнитной аномалии).
Схема сложения моментов 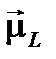 и
и 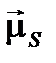 в результирующий магнитный момент
в результирующий магнитный момент 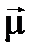 всей электронной оболочки представлена на рис. 2. (в избранном на рис. 2 масштабе длина вектора
всей электронной оболочки представлена на рис. 2. (в избранном на рис. 2 масштабе длина вектора 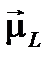 равна длине вектора
равна длине вектора 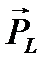 ; в силу гиромагнитной аномалии в этом масштабе длина вектора
; в силу гиромагнитной аномалии в этом масштабе длина вектора 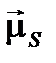 , вдвое больше длины
, вдвое больше длины 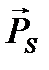 .).
.).
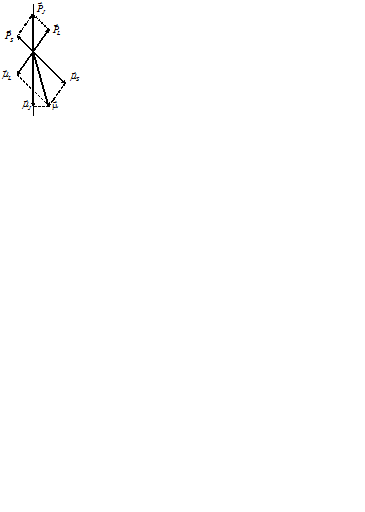
| Рис. 2. Сложение механических и магнитных моментов электронной оболочки атома |
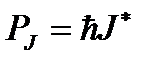
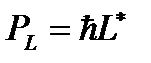
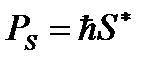
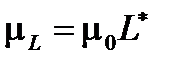
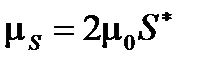
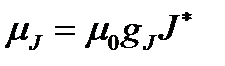
Так как вся система векторов вращается вокруг оси совпадающей с направлением вектора 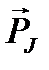 , то физическое значение имеет не вектор
, то физическое значение имеет не вектор 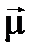 , а только его слагающая
, а только его слагающая 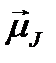 . Вектор
. Вектор 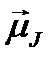 называется эффективным магнитным моментом атома или просто магнитным моментом атома.
называется эффективным магнитным моментом атома или просто магнитным моментом атома.
Таким образом, эффективный магнитный момент атома 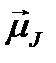 антипараллелен
антипараллелен 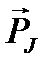 и численно равен
и численно равен
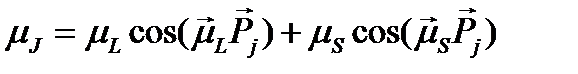 . (1.18)
. (1.18)
Несложные вычисления (см. рис. 2) дают:
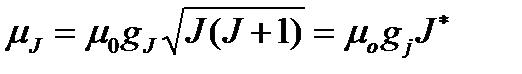 , (1.19)
, (1.19)
где
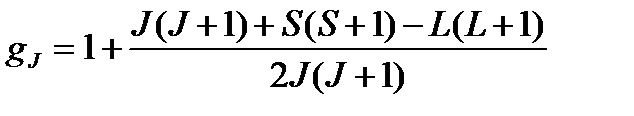 (1.20)
(1.20)
– так называемый фактор Ланде, или фактор спектроскопического расщепления электронной оболочки атома. Из (1.20) следует, что величина фактора Ланде зависит от состояния атома. По величине этого множителя можно сделать качественные заключения о происхождении магнетизма данного атома: если 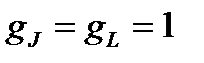 , то это возможно при S = 0, но тогда mS = 0, и магнетизм создается только за счет орбитального движения электронов. Если же
, то это возможно при S = 0, но тогда mS = 0, и магнетизм создается только за счет орбитального движения электронов. Если же 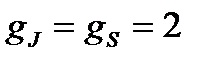 (точнее 2,00238), то это возможно при mL = 0, но тогда L = 0, и магнетизм имеет чисто спиновое происхождение. Разумеется, возможны и промежуточные случаи.
(точнее 2,00238), то это возможно при mL = 0, но тогда L = 0, и магнетизм имеет чисто спиновое происхождение. Разумеется, возможны и промежуточные случаи.
В случае же конденсированных веществ, когда взаимодействие данного атома с атомами вещества может быть значительным, g-фактор по своей величине может отличаться от того, что дает формула (1.20). Эти различия дают возможность судить как о характере взаимодействия атомов, таи и о природе магнетизма данного вещества.
