Основные формулы. атомная физика
Атом водорода
Первый постулат Бора. Атомы могут длительно пребывать только в таких состояниях, находясь в которых они не излучают энергии. Этим стационарным состояниям соответствуют определенные энергии Е1, Е2, … Еn атома.
Второй постулат Бора. При переходе из одного стационарного состояния в другое атом испускает или поглощает излучение строго определенной частоты, определяемой условием
hν = Em – En.
Стационарным состояниям атома соответствуют вполне определенные орбиты, по которым движутся электроны. Момент импульса (количества движения) L электрона для стационарных орбит кратен 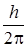 .
.
Радиусы круговых орбит электрона определяются равенством
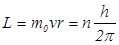 , где r – радиус орбиты; v – скорость электрона на этой орбите; n – целое число, называемое квантовым числом (n = 1, 2, 3, …).
, где r – радиус орбиты; v – скорость электрона на этой орбите; n – целое число, называемое квантовым числом (n = 1, 2, 3, …).
Энергия электрона, находящегося на n – й орбите: 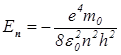 .
.
Длина волны λ света, излучаемого атомом водорода при переходе с одной орбиты на другую, может быть определена из сериальной формулы
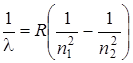 , где R – постоянная Ридберга; n1 и n2 – квантовые числа, определяющие номера орбит электрона.
, где R – постоянная Ридберга; n1 и n2 – квантовые числа, определяющие номера орбит электрона.
Энергия кванта света, излучаемого атомом водорода при переходе с одной орбиты на другую, 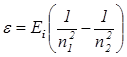 , где Еi – энергия ионизации атома водорода: Еi = -13,6 эВ.
, где Еi – энергия ионизации атома водорода: Еi = -13,6 эВ.
Энергия ионизации, выраженная в электрон-вольтах, численно равна потенциалу ионизации, выраженному в вольтах. Потенциалом ионизации называется ускоряющая разность потенциалов, которую должен пройти бомбардирующий электрон, чтобы приобрести кинетическую энергию, достаточную для ионизации атома.
Волны де Бройля
Формула де Бройля. Длина волны λ, связанная с частицей, обладающей импульсом р, выражается равенством 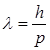 .
.
Так как импульс р в классическом приближении (v<<c) выражается формулой p = m0v, то 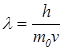 , где m0 – масса покоя частицы.
, где m0 – масса покоя частицы.
В релятивистском случае, когда скорость частицы сравнима со скоростью света в вакууме, импульс 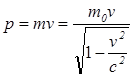 . Тогда
. Тогда 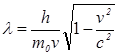 .
.
Иногда при вычислениях длины волны де Бройля импульс р частицы удобно выражать через ее кинетическую энергию Т. При этом следует пользоваться соотношением 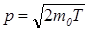 , в релятивистском случае
, в релятивистском случае 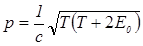 , где Е0 – энергия покоя частицы (Е0 = m0c2).
, где Е0 – энергия покоя частицы (Е0 = m0c2).
Радиоактивность
Основной закон радиоактивного распада: число нераспавшихся атомов в образце радиоактивного изотопа уменьшается со временем экспоненциально: N = N0e-λt, где N – число нераспавшихся атомов в момент времени t; N0 – число нераспавшихся атомов в момент, принятый за начальный (t = 0); е – основание натуральных логарифмов; λ – постоянная радиоактивного распада.
Число атомов, распавшихся за время t: N0 – N = N0(1 – e-λt).
Если промежуток времени Δt очень мал по сравнению с периодом полураспада Т1/2, то для определения числа распавшихся атомов служит приближенная формула ΔN ≈ λNΔt.
Период полураспада Т1/2 – промежуток времени, за который число не распавшихся атомов уменьшается в два раза. Период полураспада связан с постоянной распада соотношением 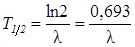 .
.
Среднее время жизни τ радиоактивного нуклида – промежуток времени, за который число не распавшихся атомов уменьшается в е раз: 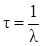 .
.
Число атомов, содержащихся в образце нуклида: 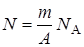 , где m – масса образца; А – масса килограмм - атома нуклида; NA – число Авогадро.
, где m – масса образца; А – масса килограмм - атома нуклида; NA – число Авогадро.
Активность а образца измеряется числом ядер, распавшихся в единицу времени: 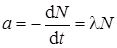 или после замены N : а = λN0 e-λt.
или после замены N : а = λN0 e-λt.
Активность образца в начальный момент (при t = 0) а0 = λN0.
Активность образца изменяется со временем по тому же закону, что и число не распавшихся ядер а =а0 е-λt.
