Понятие об идеальном растворе. Разбавленные растворы неэлектролитов. Законы Рауля
1. Идеальные растворы. Физической моделью идеального раствора является совокупность невзаимодействующих частиц, имеющая объем, аддитивно складывающийся из объемов отдельных компонентов. Наиболее важными свойствами идеальных растворов являются:
а) Идеальные растворы образуются из чистых компонентов, находящихся в том же агрегатном состоянии, что и раствор, без теплового эффекта.
б) Объем идеального раствора, образованного из чистых компонентов, находящихся в том же агрегатном состоянии, что и раствор, аддитивно складывается из объемов отдельных компонентов.
2. Предельно разбавленные растворы. Предельно разбавленным (п.р.) раствором называют раствор, в котором свойства растворителя практически остались неизменными по сравнению с чистым растворителем ввиду низкой концентрации раствора, в то время как свойства растворенного вещества могут очень сильно отличаться от его свойств в чистом виде ввиду попадания в среду растворителя. Свойствами п.р. растворов обладают обычно все разбавленные растворы вплоть до определенной концентрации, характерной для каждой системы. Чем ближе свойства компонентов, тем до более высокой концентрации сохраняют их растворы свойства п.р. растворов. Для растворов электролитов этот предел очень низок, так как ионы заметно изменяют свойства растворителя уже при миллимолярных концентрациях.
3. Реальные растворы. Различные свойства реальных растворов в той или иной степени отклоняются от идеальных (например, термодинамические). Для адекватного описания этих отклонений обычно требуются различные физические модели, учитывающие межчастичные парные и коллективные взаимодействия, размеры частиц, расстояния между ними и т.д. В некоторых простейших случаях такие модели приводят к результатам, хорошо совпадающим с экспериментом. Однако наиболее универсальный и полностью формальный способ учета неидеальности компонентов раствора был предложен Г. Льюисом в 1907 г., который сохранил ту же форму выражения химического потенциала компонента в реальном растворе, что и в идеальном, но вместо концентрации компонента использовал в нем активности.
По концентрации растворенного вещества растворы можно подразделить на концентрированные (с большой концентрацией растворенного вещества) и разбавленные (с малой концентрацией растворенного вещества).
Коллигативными свойствами раствора называются свойства, зависящие от концентрации частиц растворенного вещества и мало или совсем не зависящие от природы растворителя. К таким свойствам относят:
- осмотическое давление.
- давление насыщенного пара растворителя;
- понижение температуры замерзания раствора;
- повышение температуры кипения раствора;
1. Осмотическое давление.
Все растворы независимо от агрегатного состояния обладают способностью к диффузии.
Диффузия – это свойство вещества равномерно распределяться по всему предоставленному объему.
Скорость диффузии в газах велика, в твердых телах при обычных темпратурах диффузия может длиться годами.
Если в сосуд налить концентрированный раствор, а сверху налить чистый растворитель, то диффузия будет протекать в обоих направлениях: растворенное вещество будет диффундировать в растворитель, а растворитель – в раствор. Если раствор и растворитель разделить пленкой, через которую проходят только молекулы растворителя и не проходят молекулы растворенного вещества (полупроницаемая мембрана), то будет наблюдаться только односторонняя диффузия растворителя в раствор.
Процесс односторонней диффузии растворителя в раствор через полупроницаемую мембрану называется осмосом.
Процесс диффузии будет идти до тех пор, пока не получится полностью гомогенная система, т.е. пока весь растворитель не перейдет в раствор. Однако по мере диффузии растворителя объем раствора увеличивается и возрастает давление на мембрану со стороны раствора. Таким образом, возникает гидростатическое давление, препятствующее диффузии растворителя. При некотором давлении наступает равновесие: сколько молекул растворителя пройдет в раствор, столько же вытеснит обратно увеличившимся давлением.
Равновесное давление раствора, препятствующее диффузии растворителя через полупроницаемую мембрану, называется осмотическим давлением.
Процесс осмоса, в свою очередь, характеризуется самопроизвольным проникновением молекул растворителя через полупроницаемые перегородки.
В 1886 г. Вант-Гофф cформулировал закон (закон Вант-Гоффа), согласно которому «в разбавленном растворе растворенное вещество ведет себя подобно идеальному газу»и показал, что для растворов неэлектролитов невысоких концентраций осмотическое давление Росм равно:
Росм = С·R·Т=103·(m/M)·RT,
где С=  – молярность, моль/м3;
– молярность, моль/м3;
R=8,31 Дж/(моль·К) – универсальная газовая постоянная;
Т – абсолютная температура раствора, К.
Для растворов электролитов величина Росм составляет:
Росм = i·С·R·Т,
где i – изотонический коэффициент, показывающий, во сколько раз осмотическое давление данного раствора выше нормального. Для каждого раствора этот коэффициент определяется экспериментально.
Осмотическое давление подчиняется закону Вант-Гоффа:
Росм = CМ∙R∙T,
где СМ – молярная концентрация, R – газовая постоянная, Т – температура.
Если в данное уравнение подставить выражение молярной концентрации:

(mВ – масса растворенного вещества, MВ – молярная масса растворенного вещества,
Vр – объем раствора), получится полная аналогия уравнения Вант-Гоффа с уравнением сосояния идеального газа Менделеева-Клайперона:
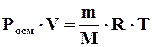
Осмотическое давление разбавленных идеальных растворов численно равно тому давлению, которое оказывало бы растворенное вещество, если бы при данной температуре оно в виде газа занимало объем раствора.
2. Давление насыщенного пара растворителя.
Важной характеристикой веществ, находящихся в жидком или твердом состоянии, является давление насыщенного пара. Давление насыщенного пара определяет при данной температуре равновесие между жидким (твердым) и газообразным состоянием вещества, которое устанавливается на границе раздела фаз. В любом растворе концентрация молекул растворителя в поверхностном слое меньше, чем в чистом растворителе, и равновесие может быть достигнуто при меньшем давлении насыщенного пара.
Под давлением насыщенного пара вещества понимают давление его паров в отсутствие других газов, в частности воздуха.
Первый закон Рауля:
Для разбавленных растворов относительное понижение давления насыщенного пара растворителя над раствором равно молярной доле растворенного вещества в растворе.
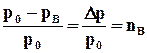
где р0 – давление насыщенного пара растворителя над чистым растворителем;
р - давление насыщенного пара растворителя над раствором;
nв – мольная доля растворенного вещества.
Следующая закономерность, характеризующая поведение растворов, относится к изменению температур кристаллизации и кипения при переходе от чистого растворителя к раствору.
3. Понижение температуры замерзания раствора (криоскопия).
При понижении температуры давление пара над раствором снижается, и когда оно становится равным давлению пара соответствующей твердой фазы, жидкость замерзает. Давление пара над раствором ниже давления пара над чистым растворителем, поэтому раствор будет замерзать при более низкой температуре, т.е. температура кристаллизации раствора всегда ниже температуры кристаллизации чистого растворителя.
Тзамерз– температура, при которой Рн.п. над жидкостью становится равным Рн.п. над кристаллами этой жидкости (при Тзам начинают выделяться первые кристаллы).
ΔТзам = Тз/ - Тз
ΔТзам - понижение температуры замерзания
Тзамизмеряется с помощью специальных метастатических ртутных термометров (термометров Бекмана) с ценой деления 0.01 К. Такие термометры имеют шкалу только на 5 К, но снабжены дополнительным резервуаром для ртути, позволяющим настроить его на любые абсолютные температуры от 260 до 380 К.
Второй закон Рауля:
