Основні термодинамічні процеси ідеальних газів
ТД аналіз будь-якої системи складається з наступного:
1. Виявити рівняння процесу. 2. Встановити зв'язок між початковими і кінцевими параметрами робочого тіла. 3. Розрахувати величину роботи зміни об’єму робочого тіла. 4. Розрахувати кількість теплоти, підведеної під час процесу до робочого тіла або відведеної від нього, і величину теплоємності робочого тіла. 5. Розрахувати величину зміни внутрішньої енергії. 6. Розрахувати величину зміни ентальпії робочого тіла. 7. Рорахувати величину зміни ентропії робочого тіла.
Політропний процес
Політропними процесами звуться процеси, які відбуваються при постійній теплоємності і які викликають підведення теплоти до робочого тіла або відведення теплоти від нього. Отже, у будь-якому політропному процесі, розподіл теплоти між значеннями, які характеризують зміну внутрішньої енергії і роботу газу, залишається незмінним, тобто відношення:
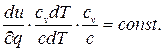
де с– постійна для даного процесу теплоємність газу або: 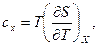 т.ч.
т.ч. 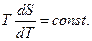
Для того, щоб вивести рівняння оборотного політропного процесу ідеального газу і, скориставшись їм, проаналізувати основні властивості цього процесу, використовуємо загальне рівняння 1-го закону ТТД, яке виражає витрату теплоти в будь-якому процесі:
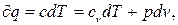 (4.1)
(4.1) 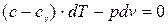 , (4.2)
, (4.2)
Скористаємося характеристичним рівнянням стану газу (p v = R T), продиференціював яке, отримаєм: p dv + v dp = RdT, тобто dT = (pdv + vdp) / R
Вирішивши спільно рівняння (4.1) і (4.2), отримаєм: 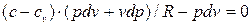
Розкривши скобки, маєм 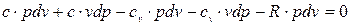
Згрупувавши доданки, які містять добутки vdp і pdv, а також з огляду на те, що 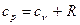 , після алгебраїчних перетворень будемо мати:
, після алгебраїчних перетворень будемо мати: 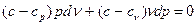
Розділивши цю рівність на (c-cv), отримаєм: 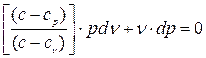
Позначивши через n дріб 
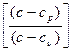 отримаєм: n p dv + v dp = 0
отримаєм: n p dv + v dp = 0
Розділивши цю рівність на p v, після інтегрування і наступного потенціювання, отримаєм:
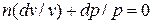 ;
; 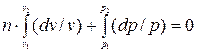 ;
; 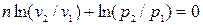
звідкіля маємо: 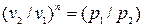 ; і остаточно:
; і остаточно: 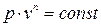 , (4.3)
, (4.3)
Рівняння (4.3) зветься рівняння політропного процесу, 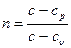 - показник політропи.
- показник політропи.
Показник політропи може приймати будь-яке чисельне значення в межах від 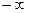 до
до 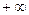 , але для даного процесу він є величиною постійною.
, але для даного процесу він є величиною постійною.
Зв'язок між параметрами p, v, T, а саме:
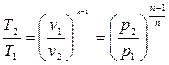 , (4.4);
, (4.4); 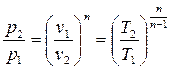 , (4.5)
, (4.5)
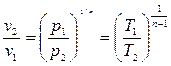 , (4.6)
, (4.6)
Робота політропного процесу.Оскільки робота зміни об’єму газу в будь-якому процесі виражається рівнянням 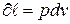 , то для політропного процесу відповідно до рівнянь політропи, маємо:
, то для політропного процесу відповідно до рівнянь політропи, маємо: 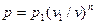 , отже:
, отже:
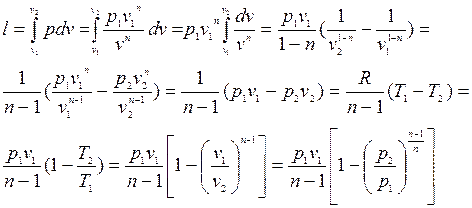 , (4.7)
, (4.7)
Кількість теплоти, яка підводиться до системи (або відводиться від неї) у політропному процесі, визначається таким чином:
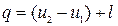 , так як du = сv dT і
, так як du = сv dT і 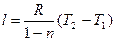 то одержуємо:
то одержуємо:
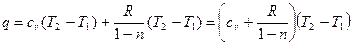
але 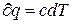 тобто q =c (T2-T1) і отже
тобто q =c (T2-T1) і отже
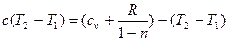 після перетворень (з огляду на те, що
після перетворень (з огляду на те, що 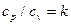 ) маємо:
) маємо:
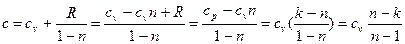
Звідкіля: 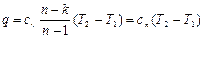 , (4.8)
, (4.8)
де 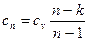 - теплоємність ідеального газу в політропному процесі.
- теплоємність ідеального газу в політропному процесі.
При  , k, n = const тому і сn = const, тому політропний процес іноді визначають як процес з постійною теплоємністю.
, k, n = const тому і сn = const, тому політропний процес іноді визначають як процес з постійною теплоємністю.
Зміна внутрішньої енергіїв політропному процесі:
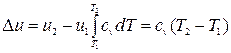 , (4.9)
, (4.9)
Зміна ентальпії в політропному процесі: 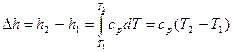 , (4.10)
, (4.10)
Зміна ентропії в політропному процесі:
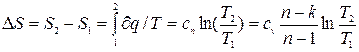 , (4.11)
, (4.11)
При русі газу в потоці, розташовувана роботау політропному процесі дорівнює:
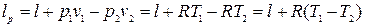 , (4.12)
, (4.12)
