Зміна ентропії в необоротних термодинамічних процесах ізольованих систем
Розглянемо принципову відмінність необоротних процесів від оборотних на прикладі розширення газу в циліндрі під поршнем (мал 6.2), одержуючого теплоту q від джерела з температурою T1 і що здійснює роботу проти зовнішньої сили Р, що утримує поршень.
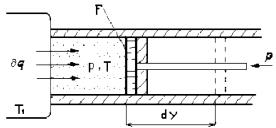 Розширення буде оборотним (рівноважним) тільки в тому випадку, якщо температура газу Т дорівнює температурі джерела Т1 (Т = T1), зовнішня сила Р дорівнює тиску газу на поршень Р = pF і при розширенні газу немає ні зовнішнього, ні внутрішнього тертя. Робота розширення газу в цьому випадку рівна
Розширення буде оборотним (рівноважним) тільки в тому випадку, якщо температура газу Т дорівнює температурі джерела Т1 (Т = T1), зовнішня сила Р дорівнює тиску газу на поршень Р = pF і при розширенні газу немає ні зовнішнього, ні внутрішнього тертя. Робота розширення газу в цьому випадку рівна
Мал.6.2  = P . dv, а зміна ентропії робочого тіла в такому процесі dSo6p =
= P . dv, а зміна ентропії робочого тіла в такому процесі dSo6p = 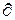 q / Т.
q / Т.
Невиконання хоч би однієї з вказаних умов робить розширення газу необоротним. Якщо безповоротність викликана тертям поршня об стінки циліндра, то робота 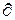 l, що здійснюється проти зовнішньої сили Р, виявляється менше, ніж p.dv, оскільки частина її витрачається на подолання тертя і переходить в теплоту
l, що здійснюється проти зовнішньої сили Р, виявляється менше, ніж p.dv, оскільки частина її витрачається на подолання тертя і переходить в теплоту 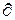 qmp. Вона сприймається газом разом з підведеною теплотою, q, внаслідок чого зростання ентропії газу в необоротному процесі dS =(
qmp. Вона сприймається газом разом з підведеною теплотою, q, внаслідок чого зростання ентропії газу в необоротному процесі dS =( 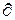 q +
q + 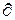 qmp)/ Т виявляється більше, ніж в оборотному при тій же кількості підведеної від джерела теплоти
qmp)/ Т виявляється більше, ніж в оборотному при тій же кількості підведеної від джерела теплоти 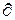 q . Отже, зміна ентропії всієї даної системи в результаті здійснення циклу дорівнює:
q . Отже, зміна ентропії всієї даної системи в результаті здійснення циклу дорівнює:
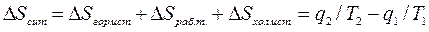 (6.13)
(6.13)
Цей стан справедливий для будь-яких оборотних і необоротних циклів,який здійснюється між двома джерелами теплоти.
Зростання ентропії системи при необоротних процесах пов'язано з тим, що ентропія робочого тіла за цикл не змінюється, а зменшення ентропії гарячих джерел менше за абсолютною величиною, ніж збільшення ентропії холодних джерел теплоти.
Таким чином, в результаті здійснення необоротного циклу ентропія ізольованої системи зростає:dScucm > 0.
Таким чином, які б процеси не протікали в ізольованій системі, її ентропія не може зменшуватися: 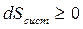 , (6.14)
, (6.14)
тут знак рівності відповідає оборотним процесам, а знак нерівності - необоротним.
Звідси слідує важливий висновок: ізольована система, що досягла рівноважного стану, надалі в цьому стані і перебуває, тобто є нездібною до мимовільної зміни стану. Насправді, будь-який мимовільний процес є необоротним і, отже, протікає із зростанням ентропії. Проте ентропія ізольованої системи має максимум в стані рівноваги, отже, в рівноважній ізольованій системі неможливі мимовільні процеси.
Таким чином, мимовільні процеси продовжуються в ізольованій системі до тих пір, поки ентропія системи не досягне максимуму. Після досягнення стану рівноваги, якій відповідає максимально можливе для даної системи значення ентропії, мимовільні процеси в системі припиняються і система перебуває в стані рівноваги.
ЛЕКЦІЯ 7
