Зонная структура некоторых металлов
Щелочные металлы
Внутренние электроны конфигурации инертных газов, [Ne] - Na, [Ar] - K и т.д., сильно связаны с ядром, поэтому они дают низколежащие зоны, которые очень узки, полностью заполнены и описываются приближением сильной связи. Вне ионного кора находится один электрон проводимости. Если бы мы считали, что эти электроны ведут себя как свободные, то поверхность Ферми представляла собой сферу радиусом kF, которая определялась бы соотношением (1.23):
kF = (3 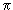 2n)1/3 = 0.62 (2 2n)1/3 = 0.62 (2 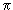 /a), /a), | (5.13а) |
Кратчайшее расстояние от центра зоны Бриллюэна до ее граней, ГN, (r-оцк (r) k-гцк) будет равно
ГN = (2 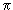 /a)[(1/22+(1/2)2+(0)]1/2 = 0.707 (2 /a)[(1/22+(1/2)2+(0)]1/2 = 0.707 (2 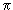 /a) /a) | (5.13б) |
Т.о. сфера свободных электронов целиком лежит внутри 1-й з.Бр.. Ближе всего она подходит к ее границам в направлении ГN, а именно, kF/ГN = 0.877 (5.13в)
Отличие поверхности Ферми от сферы свободных электронов мало - исчисляется долями процентов. Благодаря этой особенности, кинетические свойства щелочных металлов описываются хорошо в рамках теории свободных электронов Зоммерфельда.
Благородные металлы.
В отличие от щелочных металлов, в благородных металлах, помимо s-электрона на внешней атомной s-оболочке, имеются еще электроны на промежуточных d-орбиталях: Cu = [Ar]3d104s1, Ag = [Kr]4d105s1, Au = [Kr]4f145d106s1. Поэтому, если для щелочных металлов один s-электрон хорошо умещается в 1-ю з.Бр., то, например, для Cu требуется уже 6 зон для размещения 11-ти d- и s- электронов. [Как и в щелочных металлах, уровни электронов, принадлежащих заполненным инертно-подобным оболочкам, описывают в приближении сильной связи.] Расчеты показывают, что в Cu d-орбитали лежат в сравнительно узком интервале энергий от 2 до 5 эВ ниже EF, а s-орбиталь колеблется от 7 эВ выше EF до 9 эВ ниже EF. s-зона для всех k , за исключением тех, где она близко подходит к d-зонам, ведет себя как уровень свободных электронов.
Измерения с помощью эффекта dHvA показывают, что у всех 3х благородных металлов поверхности Ферми очень похожи на сферу свободных электронов, но в направлении <111> в действительности они касаются граней зоны Бриллюэна (рис.5.1). Восемь "шеек" вытягиваются и касаются восьми шестиугольных граней зоны. В эффекте dHvA при В || направлению <111> имеются два четко выраженных периода колебаний (рис. 5.1). Они определяются экстремальными траекториями на "пузе" и на "шейке".
Двухвалентные металлы.
Внешняя электронная s-оболочка элементов 2й группы заполнена, см табл.5.1. Вследствие этого,
Таблица 5.1
Группа IIA: Be:1s22s2 гпу, ; Mg: [Ne]3s2 гпу; Ca: [Ar]4s2 гцк; Sr:[Kr]5s2 гцк; Ba[Xe]6s2 оцк;
Группа IIБ: Zr: [Ar]3d104s2 гпу; Cd: [Kr] 4d105s2 гпу; Hg [Xe] 4f145d106s2 р.э.;
верхняя s-зона также будет заполнена, и можно было бы ожидать, что эти элементы будут диэлектриками. В действительности они, хоть и не очень хорошие, но все же проводники. Это объясняется перекрытием самой верхней заполненной зоной с вышележащей зоной.
Присутствие или отсутствие заполненных d-зон играет в элементах 2й группы существенно меньшую роль по сравнению со щелочными и благородными металлами. Расчеты зонной структуры показывают, что в Zn и Cd d-зона полностью лежит ниже дна зоны проводимости, а в Hg она перекрывается с зоной проводимости лишь в очень узкой области вблизи ее дна. Различие свойств элементов 2й группы, в основном, связано с особенностями их структуры.
В кубических 2х валентных металлах (Ca, Sr, Ba) объем сферы Ферми примерно равен объему 1й з.Бр.. Поэтому сфера Ферми пересекает грани зоны. Т.о. поверхность Ферми свободных электронов имеет довольно сложную структуру в 1-й з.Бр. и дырочные "карманы" во 2й зоне. Эффективный (псевдо) потенциал недостаточен чтобы сжать до нуля "карманы" 2й з.Бр. и заполнить т.о. все незанятые уровни в 1-й з.Бр.. Если бы это происходило, то эти элементы были бы диэлектриками. Очевидно, это не происходит, т.к. они являются металлами.
У ртути измерения показывают наличие электронных карманов во 2-й зоне и сложной протяженной структуры в 1й зоне Бриллюэна.
У гпу-металлов 2й группы (Be, Mg, Zn, Cd) поверхность Ферми представляет собой чрезвычайно сложную структуру, которую можно получить из сферы свободных электронов, содержащей по четыре уровня на каждую элементарную ячейку (в гпу - 2 атома на одну ячейку).
