Ядерная модель атома Резерфорда. Формула Резерфорда.
 Основная задача опыта Резерфорда по рассеянию
Основная задача опыта Резерфорда по рассеянию 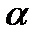 -частиц состояла в том, чтобы определить распределение электрического заряда в атоме. Основная идея заключалась в использовании того факта, что законы рассеяния заряженных частиц атомами зависят от распределения заряда в атоме. Зная эту зависимость, можно по рассеянию заряженных частиц на атомах определить распределение заряда в нем, т.е. экспериментально исследовать строение атома. Угол
-частиц состояла в том, чтобы определить распределение электрического заряда в атоме. Основная идея заключалась в использовании того факта, что законы рассеяния заряженных частиц атомами зависят от распределения заряда в атоме. Зная эту зависимость, можно по рассеянию заряженных частиц на атомах определить распределение заряда в нем, т.е. экспериментально исследовать строение атома. Угол 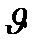 , на который рассеивается заряженная частица кулоновским полем неподвижного ядра, определяется формулой
, на который рассеивается заряженная частица кулоновским полем неподвижного ядра, определяется формулой 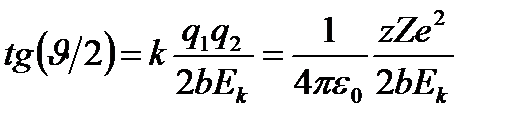 , где
, где 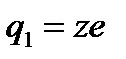 и
и 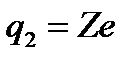 − заряды частицы и ядра,
− заряды частицы и ядра, 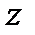 и
и 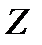 − зарядовые числа частицы и ядра,
− зарядовые числа частицы и ядра, 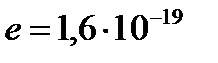 Кл − элементарный электрический заряд,
Кл − элементарный электрический заряд, 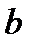 − прицельный параметр,
− прицельный параметр, 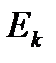 − кинетическая энергия налетающей частицы, коэффициент
− кинетическая энергия налетающей частицы, коэффициент 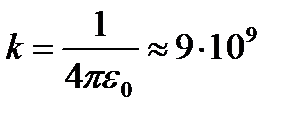 (Н∙м2)/Кл2 в СИ и
(Н∙м2)/Кл2 в СИ и 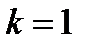 в СГСЭ. Формула Резерфорда позволяет рассчитать относительное число частиц, рассеянных ядрами фольги в элементарном телесном угле
в СГСЭ. Формула Резерфорда позволяет рассчитать относительное число частиц, рассеянных ядрами фольги в элементарном телесном угле 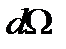 под углом
под углом 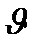 к первоначальному направлению их движения:
к первоначальному направлению их движения: 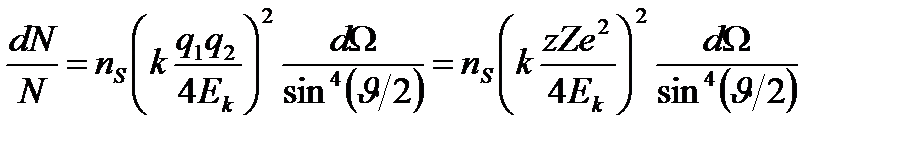 , где
, где 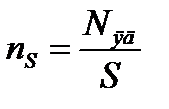 − число ядер на единицу площади поверхности рассеивающего слоя (фольги),
− число ядер на единицу площади поверхности рассеивающего слоя (фольги), 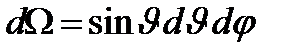 − элементарный телесный угол.
− элементарный телесный угол.
15. Постулаты Бора. Опыты Франка и Герца.Первый постулат: Атом может длительное время находится только в определенных, так называемых стационарных состояниях, которые характеризуются дискретными значениями энергии 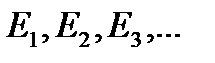 В этих состояниях атом не излучает. Правило квантования: Из всевозможных круговых орбит электрона в атоме стационарным состояниям соответствуют лишь те орбиты, при движении по которым момент импульса электрона равен целому числу постоянных Планка:
В этих состояниях атом не излучает. Правило квантования: Из всевозможных круговых орбит электрона в атоме стационарным состояниям соответствуют лишь те орбиты, при движении по которым момент импульса электрона равен целому числу постоянных Планка: 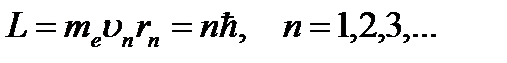 , где
, где 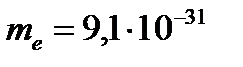 кг − масса электрона;
кг − масса электрона; 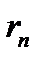 − радиус
− радиус 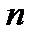 -ой орбиты электрона;
-ой орбиты электрона; 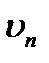 − скорость электрона на
− скорость электрона на 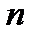 -ой орбите. Второй постулат: при переходе атома из стационарного состояния с большей энергией
-ой орбите. Второй постулат: при переходе атома из стационарного состояния с большей энергией 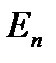 в стационарное состояние с меньшей энергией
в стационарное состояние с меньшей энергией 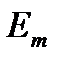
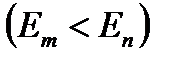 происходит излучение кванта света (фотона) с энергией
происходит излучение кванта света (фотона) с энергией 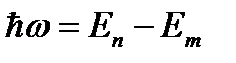 такое же соотношение выполняется и в случае поглощения, когда падающий фотон переводит атом с низшего энергетического уровня
такое же соотношение выполняется и в случае поглощения, когда падающий фотон переводит атом с низшего энергетического уровня 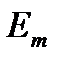 на более высокий
на более высокий 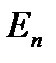 .
.
Стеклянный баллон заполнен парами ртути, при давл. 1 мм.рт.ст.=133 Па. В опыте рассм.столкновение эл-ов с атомами ртути методом задерж.потенциала. Электрон на уч.м/у К и С разгон.эл.полем(Еке=еИ). Когда И<4,9 В при столкновении эл-в с атомами Hg, эл-н передает атому малую часть Еке.Когда И>=4,9 В, Еке достаточно для того,чтобы при столкновении с атомами, чтобы перевести его в 1 возб.сост.(Е1в Е2). В рез. Еке эл-ов попадает на сетку 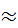 0 и преодолеть задерж. разность потенц. эл-ов не может,след., ток уменьш. При И>=9,8В эл-н на К-С успевает передать эн.двум атомам Hg. Вывод: Эн.ур.атома дискретны; первый потенц.ионизации
0 и преодолеть задерж. разность потенц. эл-ов не может,след., ток уменьш. При И>=9,8В эл-н на К-С успевает передать эн.двум атомам Hg. Вывод: Эн.ур.атома дискретны; первый потенц.ионизации 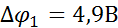 ; при И>=4,9В пары Hg испуск. УФ излуч.с λ=253,7 нм(Еке=Е2-Е1)
; при И>=4,9В пары Hg испуск. УФ излуч.с λ=253,7 нм(Еке=Е2-Е1)
