Лабораторна робота № 10 (14)
ВИЗНАЧЕННЯ ЕЛЕКТРОХІМІЧНОГО ЕКВІВАЛЕНТА МІДІ І ВЕЛИЧИНИ ЕЛЕМЕНТАРНОГО ЗАРЯДУ
Мета роботи. Ознайомитися з методом визначення електрохімічного еквівалента речовини, визначити величину елементарного електричного заряду.
Прилади і приладдя: електролітична ванна, джерело постійного струму, амперметр, вимикач, сушильне обладнання, терези, наждачний папір, секундомір.
Література
1. Грабовский Р.И. Курс физики: Учеб. пособие для с.-х. ин-тов. – М., 1979. – 552 с.
2. Розумнюк В.Т., Якименко І.Л. Фізика. Основні поняття, явища і закони. – Біла Церква, 2004. – 71 с.
Теоретичні відомості
Електролітами називаються речовини, молекули яких в розчині чи в розплаві розпадаються на іони.
Нагадаємо, що іон – це атом або група атомів, що несуть нескомпенсований електричний заряд внаслідок від’єднання чи приєднання від (чи до) них зовнішніх орбітальних електронів. Наприклад, іон міді Cu2+має не скомпенсований заряд +2 внаслідок від’єднання від нейтрального атома міді двох електронів.
До електролітів належать солі, кислоти та луги. Молекули електроліту та розчинника (вода, спирт, ацетон) є дипольними – в одному кінці молекули знаходиться більше позитивних зарядів, а в другому – негативних. Тому кожну молекулу електроліту в розчині оточують молекули води так, що кожна частина молекули електроліту оточена протилежними за знаком кінцями молекул води (рис.10.1).
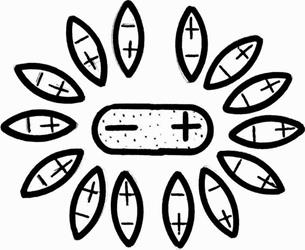
Рис. 10.1.
Сили взаємодії протилежних зарядів електроліту та води (розчинника) намагаються розірвати молекулу електроліту, в результаті чого більшість молекул електроліту розпадається на позитивні іони (аніони) та негативні іони (катіони). (рис. 10.2)
Електролітичною дисоціацієюназивається процес розпаду молекул на іони.
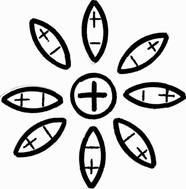
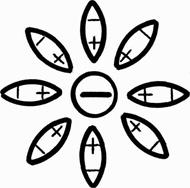
Рис. 10.2.
Прикладом електричної дисоціації є розпад молекул водного розчину мідного купоросу CuSO4 на позитивні іони Cu2+ та негативні іони 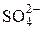 , тобто відбувається реакція:
, тобто відбувається реакція:
CuSO4 = Cu2+ + 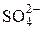 .
.
Якщо в такий розчин електроліту ввести два мідних електроди і приєднати їх до джерела постійного струму, то під впливом електричного поля іони почнуть рухатися. Позитивні іони будуть рухатися до негативного електрода, а негативні – до позитивного. Рух іонів приводить до утворення електричного струму в колі. Такі провідники називаються провідниками другого роду. Іони Cu2+, надходячи до катода, відбирають від нього два електрони і виділяються на катоді у вигляді нейтральних атомів. Іони 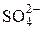 – надходять до позитивного електрода, віддають йому свій заряд і, ставши нейтральними, реагують з анодом, утворюючи CuSO4, що надходить в розчин.
– надходять до позитивного електрода, віддають йому свій заряд і, ставши нейтральними, реагують з анодом, утворюючи CuSO4, що надходить в розчин.
В результаті кількість речовини катода збільшується, а анода – зменшується, сама ж кількість електроліту в розчині не зменшується. Описане явище отримало назву електролізу.
Електролізомназивається процес виділення речовини на електроді при проходженні через розчин електроліту електричного струму.
Електроліз використовується в техніці для одержання деяких матеріалів, а також в медицині для введення через шкіру ліків (електрофорез). Вивчаючи процеси електролізу Фарадей встановив наступні два закони:
Перший закон Фарадея: Маса речовини (m), яка виділяється на електроді, прямо пропорційна величині заряду (q), що пройшов через електроліт.
m = k · q (1)
деk – електрохімічний еквівалент речовини, який чисельно дорівнює масі речовини, що виділяється на електроді при проходженні через електроліт заряду рівного 1 кулону.
Оскільки:
q = I · t, то m = kIt . (2)
Звідси:
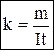 (3)
(3)
Електрохімічний еквівалент (k) є сталою і певною величиною для кожної речовини. Як випливає з формули (3), k вимірюється в кг/Кл.
Другий закон Фарадея: Електрохімічний еквівалент речовини пропорційний його хімічному еквіваленту.
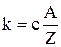 , (4)
, (4)
де А – атомна маса речовини; Z – валентність речовини; с – універсальна стала.
Відношення 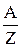 є хімічним еквівалентом речовини, який чисельно дорівнює масі даної речовини в кілограмах, що заміщує в хімічних сполуках 1,0078 кг водню. Число
є хімічним еквівалентом речовини, який чисельно дорівнює масі даної речовини в кілограмах, що заміщує в хімічних сполуках 1,0078 кг водню. Число 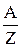 кілограмів речовини є кілограм-еквівалентом цієї речовини.
кілограмів речовини є кілограм-еквівалентом цієї речовини.
Дослідним шляхом Фарадей встановив, що для виділення на електроді одного хімічного еквівалента будь-якої речовини необхідно через розчин електроліту пропустити певний заряд (F).
Стала Фарадея F дорівнює заряду на кожний моль виділеної на електроді речовини при проходженні струму через електроліт.
F = 9,65 · 104 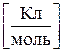 .
.
Таким чином, стала Фарадея дорівнює величині заряду, при проходженні якого через електроліт на електроді виділяється 1 кілограм-еквівалент речовини.
Рівняння (4) можемо записати так:
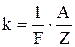 ,
, 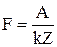 . (5)
. (5)
Підставивши значення k в рівняння (1), одержимо:
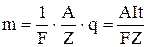 . (6)
. (6)
Оскільки в 1 кілограм-еквіваленті речовини знаходиться NA = 6,02×1023 атомів (число Авогадро), які й переносять електричний заряд, то при одержанні 1 кілограм-еквівалента речовини нейтралізується кількість іонів, що дорівнює числу Авогадро.
Якщо при електролізі виділяється одновалентна речовина, то її хімічний еквівалент дорівнює кілограм-еквіваленту цієї речовини. Тому заряд одновалентного іона визначається за формулою:
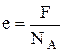 . (7)
. (7)
На рисунку зображена установка для виконання роботи. В її склад входять: електролітична ванна, амперметр, вимикач, реостат, блок живлення.
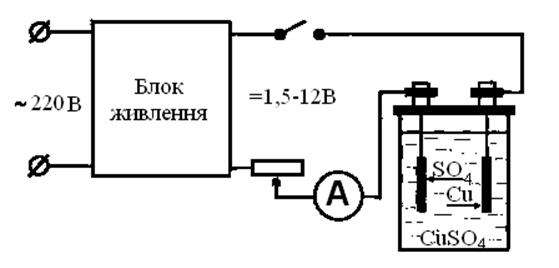
Рис. 10.3.
Порядок виконання роботи
1. Ознайомитися з електричною схемою (рис. 10.3).
2. Перед початком роботи показати схему викладачу або лаборанту.
3. Повзунком реостата виставити найбільше значення опору, почистити катод наждачним папером та визначити його масу m1 на терезах.
4. Помістити у електролітичну ванну катод паралельно аноду, замкнути коло вимикачем К і включити секундомір. Величину сили струму вказує викладач.
5. Через 20–30 хвилин виключити струм, дістати катод, промити його проточною водою, висушити за допомогою фена і знову зважити. Визначити масу катода m2. Різниця мас (m2 - m1) – це кількість міді, що виділилася при електролізі.
6. Одержані дані записати в таблицю.
7. За формулою (3) визначити електрохімічний еквівалент.
8. За формулою (7) знайти величину елементарного заряду.
9. Визначити абсолютні похибки Δk та Δе, використовуючи табличні значення е і k (е = 1,6·10-19 Кл, k = 0,399·10-6 кг/Кл), а також відносні похибки за формулами:
Δk = 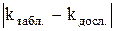
Δе = 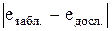
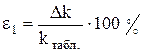
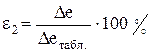
Для міді прийняти А = 63,55; Z = 2.
Таблиця
| m1, кг | m2, кг | t, c | I, A | k, кг/Кл | F, Кл/кг-екв | е, Кл | Δk, кг/Кл | Δе, Кл |
Контрольні питання
1. Які речовини називаються електролітами?
2. Що таке електролітична дисоціація?
3. Що називається хімічним та електрохімічним еквівалентом?
4. Дати визначення першого та другого закону Фарадея.
5. В чому полягає фізичний зміст сталої Фарадея? Зв’язок сталої Фарадея з хімічним еквівалентом.
