Обратимые и необратимые процессы
Термодинамический процесс называетсяобратимым,если он может проходить как в прямом, так и в обратном направлении; при этом после возвращения системы в исходное состояние в окружающей среде и в самой системе не происходит никаких изменений.
Равновесный (квазистатический) процесс представляет собой непрерывную последовательность равновесных состояний. Любая точка такого процесса – состояние равновесия, из которого система может идти как в прямом, так и в обратном направлении. Отсюда следует, что любой равновесный процесс обратим.
Только термодинамически равновесные процессы можно изображать графически, потому что для неравновесной системы значение параметров, например, температуры или концентрации, объёму неодинаково, а для всей системы является неопределённой величиной. Процессы, происходящие в таких системах, могут быть изображены графически только приближённо, по усреднённым значениям параметров.
Можно привести пример обратимого процесса из механики – абсолютно упругое соударение. Если заменить переменную времени t на –t, то при абсолютно упругом ударе начальные и конечные скорости тел просто поменяются ролями. Законы Ньютона обратимы.
Обратимые процессы – идеализация. Все реальные процессы в той или иной степени необратимы из-за трения, диффузии, теплопроводности. Все явления переноса – необратимые процессы. Теплота сама собой может переходить только от горячего к холодному, но никогда наоборот. Ещё пример необратимого процесса: абсолютно неупругое соударение, при котором механическая энергия превращается частично или полностью в теплоту.
Обратимые процессы наиболее экономичны, система при таких процессах совершает максимальную работу, а КПД оказывается максимальным.
9) Цикл Карно. Теорема Карно.
Попробуем создать тепловую машину, при работе которой используются только обратимые процессы.
Обратимым может быть адиабатный процесс – теплопередачи там нет вообще; работа внешних сил идёт на приращение внутренней энергии или наоборот, работа системы совершается за счёт убыли внутренней энергии системы, и эти процессы обратимы.
 ;
; 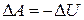 .
.
Но теплопередачу от нагревателя как-то надо осуществить, иначе за счёт какой тепловой энергии мы получим полезную работу? Обратимый процесс теплопередачи между двумя телами можно осуществить в изотермическом процессе, если температура обоих тел равна. Тогда безразлично, в какую сторону течёт поток теплоты. Но такой процесс будет и бесконечно медленным.
В цикле Карно (рис.8.10 и 8.11) идеальный газ проходит цикл, состоящий из двух адиабат (2-3 и 4-1) и двух изотерм (1-2 и 3-4).
1-2 – изотермическое расширение от объёма V1 до V2; при этом газ находится в контакте с нагревателем при температуре T1;
2-3 – адиабатическое расширение от объёма V2 до V3; конечная температура газа равна температуре охладителя T2;

3-4 – изотермическое сжатие от объёма V3 до V4; при этом газ находится в контакте с охладителем при температуре T2;
4-1 – адиабатическое сжатие от объёма V4 до V1; конечная температура газа равна температуре нагревателя T1.
Для изотермических процессов:


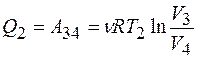
Для адиабатических процессов:
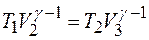 ;
;
 .
.
Тогда из последних двух равенств:

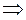

Тогда КПД цикла Карно равен:
 .
.
Доказана первая часть теоремы Карно:
1) КПД цикла Карно не зависит от природы рабочего тела и определяется только температурами нагревателя и охладителя:
 . (8.38)
. (8.38)
Сформулируем две другие части теоремы Карно, а докажем их позже.
2)КПД любого обратимого цикла не больше КПД цикла Карно с теми же температурами нагревателя и охладителя:
 . (8.39)
. (8.39)
3)КПД любого необратимого цикла меньше КПД цикла Карно с теми же температурами нагревателя и охладителя:
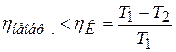 . (8.40)
. (8.40)
Энтропия.
Определение энтропии
 |
Понятие энтропии было введено Клаузиусом. Энтропия – это одна из функций состояния термодинамической системы. Функция состояния – это такая величина, значения которой однозначно определяются состоянием системы, а изменение функции состояния при переходе системы из одного состояния в другое определяется только начальным и конечным состояниями системы и не зависят от пути перехода.
Внутренняя энергия U – функция состояния. Внутренняя энергия идеального газа равна  , и её изменение определяется только начальной и конечной температурами:
, и её изменение определяется только начальной и конечной температурами:  . Величина
. Величина  – это молярная теплоёмкость идеального газа при постоянном объёме.
– это молярная теплоёмкость идеального газа при постоянном объёме.
Количество теплоты Q и работа A не являются функциями состояния: они зависят от пути перехода системы из начального состояния в конечное. Например, пусть идеальный газ переходит из состояния 1 в состояние 2, совершив последовательно сначала изобарный процесс, затем – изохорный (рис.8.12, а). Тогда совершённая за весь процесс работа равна 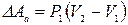 . Пусть теперь из 1 в 2 идеальный газ переходит, сначала совершив изохорный процесс, а затем изобарный (рис.8.12, b). Работа при таком переходе равна
. Пусть теперь из 1 в 2 идеальный газ переходит, сначала совершив изохорный процесс, а затем изобарный (рис.8.12, b). Работа при таком переходе равна  . Очевидно,
. Очевидно,  . Величина работы оказалась разная, хотя начальное и конечное состояние одинаковы. Поскольку по первому закону термодинамики количество теплоты, сообщённое системе, идёт на приращение внутренней энергии и на работу системы против внешних сил:
. Величина работы оказалась разная, хотя начальное и конечное состояние одинаковы. Поскольку по первому закону термодинамики количество теплоты, сообщённое системе, идёт на приращение внутренней энергии и на работу системы против внешних сил:  , то теплота, полученная системой в процессах a и b, тоже будет разной, то есть теплота также не является функцией состояния.
, то теплота, полученная системой в процессах a и b, тоже будет разной, то есть теплота также не является функцией состояния.
С точки зрения математики, малые приращения величин, не являющихся функциями состояния, не будут полными дифференциалами, и для них нужно использовать обозначения:  и
и 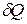 . Оказывается, что для теплоты интегрирующим множителем является обратная температура:
. Оказывается, что для теплоты интегрирующим множителем является обратная температура:  , и величина, равная отношению полученной системой теплоты к абсолютной температуре, является полным дифференциалом – это приведённая теплота:
, и величина, равная отношению полученной системой теплоты к абсолютной температуре, является полным дифференциалом – это приведённая теплота:  . По определению Клаузиуса, функция состояния системы, дифференциал которой в обратимом процессе равен приведённой теплоте, является энтропией:
. По определению Клаузиуса, функция состояния системы, дифференциал которой в обратимом процессе равен приведённой теплоте, является энтропией:
 . (8.41)
. (8.41)
Свойства энтропии
1) Энтропия – функция состояния системы, то есть в замкнутой системе в обратимом процессе, когда система возвращается в исходное состояние, полное изменения энтропии равно нулю:
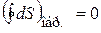 . (8.42)
. (8.42)
2) Энтропия аддитивна, то есть энтропия системы равна сумме энтропий всех её частей.
3) Энтропия замкнутой системы не убывает:
 , (8.43)
, (8.43)
причём 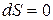 для обратимых процессов и
для обратимых процессов и 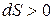 для необратимых.
для необратимых.
Соотношение (8.43) называется неравенством Клаузиуса и представляет собой одну из формулировок второго начала термодинамики: энтропия замкнутой системы остаётся постоянной, если в ней происходят только обратимые процессы, и возрастает в случае необратимых процессов.
Рассмотрим замкнутую систему, состоящую из двух тел с температурами  и
и  . Пусть
. Пусть  – количество теплоты, полученное вторым телом от первого
– количество теплоты, полученное вторым телом от первого  . Тогда количество теплоты, полученное первым телом, отрицательно и равно
. Тогда количество теплоты, полученное первым телом, отрицательно и равно 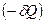 . Полное приращение энтропии системы двух тел в процессе теплопередачи равно сумме изменений энтропий двух тел:
. Полное приращение энтропии системы двух тел в процессе теплопередачи равно сумме изменений энтропий двух тел:
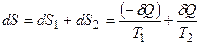 . (8.44)
. (8.44)
Процесс теплопередачи может быть обратим лишь в случае, если температуры тел равны: 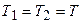 . При неравенстве температур обратный процесс невозможен: теплота сама собой от холодного к нагретому идти не может – это одна из формулировок второго начала термодинамики. Тогда из (8.44) получим:
. При неравенстве температур обратный процесс невозможен: теплота сама собой от холодного к нагретому идти не может – это одна из формулировок второго начала термодинамики. Тогда из (8.44) получим:
 . (8.45)
. (8.45)
Процесс передачи теплоты от первого тела ко второму будет необратимым, если  . Тогда
. Тогда 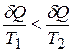 , и из (8.44)
, и из (8.44)
 . (8.46)
. (8.46)
