Тема 3. Другий закон термодинаміки
Самочинні та не самочинні процеси. Формулювання другого закону термодинаміки і його аналітичний вираз. Розрахунок зміни ентропії у різних процесах. Статистичний характер другого закону термодинаміки. Термодинамічна вірогідність. Ентропія як міра вірогідності. Формула Больцмана. Абсолютні значення ентропії. Постулат Планка. Третій закон термодинаміки. Залежність ентропії від температури. Функції Гіббса і Гельмгольца як критерій напряму процесу
Перший принцип термодинаміки стверджує еквівалентність різних форм енергії і дає кількісні співвідношення, справедливі при будь-яких переходах. Але він не дає ніяких відомостей про напрям, в якому відбувається перехід насправді.
Наприклад, якщо система цинк — сірчана кислота, що знаходиться у певному стані, будь-яким шляхом переходить у новий певний стан сульфат цинку — водень, то згідно з першим законом загальна кількість теплоти і роботи залишається незмінною. Крім того, при зворотному переході загальний енергетичний баланс буде тим же, але з протилежним знаком. Однак з досвіду відомо, що цинк самочинно реагує із сірчаною кислотою, у той час як зворотний перехід вимагає втручання ззовні, витрати роботи.
Таким чином, всі процеси можуть бути поділені на дві групи: процеси самочинні, або спонтанні (позитивні), які проходять самі по собі, і процеси не самочинні (негативні), які вимагають для свого проходження витрати роботи.
Самочинні процеси проходять у напрямі наближення системи до рівноважного стану. Ідеальним граничним випадком процесів, які лежать між самочинними і не самочинними, є рівноважні процеси, при яких відбувається перехід системи у прямому або зворотному напрямі через послідовність рівноважних станів.
Другий закон термодинаміки дає можливість передбачити напрям перебігу процесу в заданих умовах, а також характеризувати рівноважний стан системи.
Другий закон (принцип) термодинаміки, як і перший, є постулатом, який неможливо довести на основі інших положень. Неможливий самочиннийперехід теплоти від менш нагрітого тіла до більш нагрітого. Отже, неможливо сконструювати машину, яка б у круговому процесі тільки переносила тепло від більш холодного тіла до більш нагрітого.
Інше формулювання запропоноване В. Томсоном (лордом Кельвіном, 1851):
Неможливо побудувати періодично діючу машину, яка б тільки одержувала тепло від теплового резервуару і повністю перетворювала його в еквівалентну кількість роботи (принцип неможливості вічного двигуна другого роду).
З другого закону термодинаміки випливає, що люба форма енергії – механічна, електрична, хімічна – може повністю переходити в тепло, однак зворотній повний перехід не можливий, тому що частина теплової енергії розсіюється. Для характеристики незворотності енергетичних переходів при різних фізичних і хімічних процесах застосовується особа величина – ентропія S, як та частина енергії, яка не перетворюється у корисну роботу. Зміна ентропії при оборотному процесі визначається рівнянням(оскільки 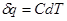 ):
):
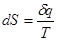 =
= 
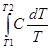 .
.
В цьому рівнянні С – теплоємкість при постійному тиску Ср, або постійному об’ємі Сv.
Для не оборотних процесів 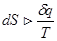 . Таким чином, зміни ентропії в ізольованій системі вказують на можливість самочинних переходів у системі(збільшення ентропії), або на стан рівноваги(сталість ентропії).
. Таким чином, зміни ентропії в ізольованій системі вказують на можливість самочинних переходів у системі(збільшення ентропії), або на стан рівноваги(сталість ентропії).
Можна сказати що ентропія є мірою невпорядкованості стану системи. Системи прагнуть перейти з більш впорядкованого стану до менш впорядкованого стану, який характеризується збільшенням ентропії.
Виходячи із рівняння 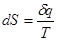 можна розрахувати зміну ентропії у різних процесах:
можна розрахувати зміну ентропії у різних процесах:
1.для ізотермічного процесу(при переході речовини з одного агрегатного стану у інше):
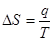 .
.
Для процесу плавлення q – теплота плавлення і т.д.
2.Змішання двох ідеальних газів при сталих температурі і тиску:
.
3.Нагрівання при сталому об’єму або тиску:
 .
.
Стан системи можна характеризувати мікро станами часток, які її складають – їх миттєвими координатами і швидкостями різних видів руху у різних напрямках. Число мікро станів системи зветься термодинамічною вірогідністю системи W. Оскільки число часток у системі значне, імовірність виражається значними числами. Тому користуються логарифмом термодинамічної вірогідності, який зв’язане з ентропією формулою Больцмана: S = кlnW і є ентропією системи. Множник к дорівнює сталій Больцмана. Статистичний характер другого закону термодинаміки вказує на те, що збільшення ентропії відображає найбільш вірогідний шлях змін.
Розглянуті вище співвідношення дають можливість розрахувати тільки зміни ентропії, але не дозволяють знайти її абсолютне значення. Ентропію можна обчислити на основі постулату Планка (1912), згідно з яким ентропія ідеального кристала індивідуальної речовини дорівнює нулю при абсолютному нулі температури S0 = 0. Цей постулат називають також третім законом термодинаміки.
Зі збільшенням температури зростає швидкість різних видів руху часток, а відповідно і число їх мікро станів і термодинамічна імовірність і ентропія. При переході речовини з твердого стану у рідкий значно збільшується невпорядкованість і ентропія речовини. Особливо різко збільшується ентропія при переході з рідкого у газоподібний стан. Збільшення числа атомів у молекулі і ускладнення молекули призводять до збільшення ентропії. Можна розрахувати зміну ентропії хімічної реакції яка дорівнює різниці(з урахуванням стехіометричних коефіцієнтів) між сумою ентропій продуктів реакції і сумою ентропій вихідних речовин.
У довідкових таблицях термодинамічних властивостей речовин звичайно наводяться величини S — стандартні ентропії при 298 К і р = 1,013 105 Па. Для знаходження абсолютних ентропій в інших умовах необхідно до цих значень додати зміни, пов'язані з переходом із стандартного стану в новий.
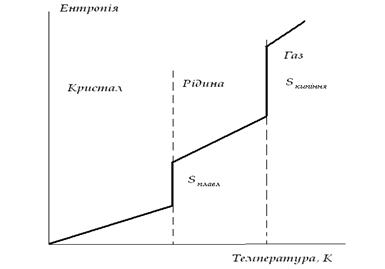
Рисунок. Зміна ентропії речовини зі збільшенням температури.
Таким чином для систем, які не обмінюються з зовнішнім середовищем ні енергією ні речовиною другий закон термодинаміки можна сформулювати наступним чином: в ізольованих системах самочинно йдуть тільки такі процеси, які супроводжуються зростанням ентропії.
Однак, системи, в яких перебігають хімічні реакції не ізольовані, тому що вони супроводжуються зміною внутрішньої енергії(тепловим ефектом реакції), обмінюються енергією з зовнішнім середовищем і таким чином зазвичай супроводжуються як зміною ентропії, так і зміною ентальпії. В хімічних процесах проявляються дві протилежні тенденції: а) прагнення до утворення міцних зв’язків між частками, виникнення більш складних речовин, що супроводжується зменшенням енергії системи(ентальпійний фактор -  ); б) прагнення до роз’єднанню часток, до безладдя, що характеризується збільшенням ентропії(ентропійний фактор -Т
); б) прагнення до роз’єднанню часток, до безладдя, що характеризується збільшенням ентропії(ентропійний фактор -Т 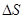 ). Кожний з зих факторів окремо не може бути критерієм самочинності хімічної реакції. Для ізобаро-ізотермічного процесу їх об’єднує термодинамічна функція, яка зветься енергією Гіббса(
). Кожний з зих факторів окремо не може бути критерієм самочинності хімічної реакції. Для ізобаро-ізотермічного процесу їх об’єднує термодинамічна функція, яка зветься енергією Гіббса( 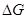 ):
):
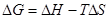 .
.
Це рівняння можна записати у вигляді:
 .
.
Ентальпія хімічної реакції складається з двох частин. Перша ( 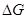 ) дорівнює максимальній роботі Аmax, яку може виконати система, або частина енергетичного ефекту хімічної реакції, яку можна перетворити в роботу:
) дорівнює максимальній роботі Аmax, яку може виконати система, або частина енергетичного ефекту хімічної реакції, яку можна перетворити в роботу: 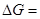 Аmax, або її ще називають вільною енергією. Друга частина(ентропійний фактор) – це частина енергетичного ефекту, яку не можливо перетворити на роботу, вона розсіюється у зовнішнє середовище у вигляді теплоти і ентропійний фактор
Аmax, або її ще називають вільною енергією. Друга частина(ентропійний фактор) – це частина енергетичного ефекту, яку не можливо перетворити на роботу, вона розсіюється у зовнішнє середовище у вигляді теплоти і ентропійний фактор  зветься зв’язаною енергією. Енергія Гіббса є критерій самочинності перебігання хімічної реакції при ізобаро-ізотермічних процесах. Хімічна реакція принципово можлива коли
зветься зв’язаною енергією. Енергія Гіббса є критерій самочинності перебігання хімічної реакції при ізобаро-ізотермічних процесах. Хімічна реакція принципово можлива коли  . Якщо
. Якщо 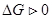 , хімічна реакція не може перебігати самочинно. Якщо
, хімічна реакція не може перебігати самочинно. Якщо 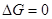 , реакція зворотна і може перебігати як у прямому, так і у зворотному напрямках.
, реакція зворотна і може перебігати як у прямому, так і у зворотному напрямках.
Напрямок реакції залежить від її характеру. Якщо реакція екзотермічна( 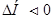 ) і в результаті реакції збільшується число моль газоподібних речовин(
) і в результаті реакції збільшується число моль газоподібних речовин( 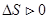 ), то вона перебігає у прямому напрямку при любих температурах. Навпаки, якщо
), то вона перебігає у прямому напрямку при любих температурах. Навпаки, якщо  і зменшується число моль газоподібних речовин
і зменшується число моль газоподібних речовин 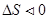 , реакція не може перебігати самочинно у прямому напрямку при любій температурі.
, реакція не може перебігати самочинно у прямому напрямку при любій температурі.
Якщо 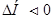 , і
, і 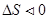 самочинно може перебігати пряма реакція при низьких температурах Т
самочинно може перебігати пряма реакція при низьких температурах Т 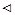 Тр=
Тр= 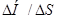 і зворотна при високих.
і зворотна при високих.
Якщо  , і
, і 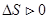 самочинно може перебігати пряма реакція при високих температурах Т
самочинно може перебігати пряма реакція при високих температурах Т 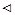 Тр=
Тр= 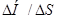 і зворотна при низьких.
і зворотна при низьких.
В довідниках наведені стандартні значення зміни енергії Гіббса при утворенні 1 моль речовини з простих речовин, стійких при 298 К(енергі Гіббса утворення речовини -  ). Енергію Гіббса хімічної реакції можна розрахувати як різницю між сумою енергій Гіббса утворення продуктів реакції і сумою енергій Гіббса утворення вихідних речовин з урахуванням стехіометричних коефіцієнтів. Отримане значення
). Енергію Гіббса хімічної реакції можна розрахувати як різницю між сумою енергій Гіббса утворення продуктів реакції і сумою енергій Гіббса утворення вихідних речовин з урахуванням стехіометричних коефіцієнтів. Отримане значення  зветься стандартною енергією Гіббса хімічної реакції і є критерієм самочинного перебігання реакції при стандартних станах вихідних речовин і продуктів реакції.
зветься стандартною енергією Гіббса хімічної реакції і є критерієм самочинного перебігання реакції при стандартних станах вихідних речовин і продуктів реакції.
Для ізохоро-ізотермічних умов максимальна робота системи при рівноважному проведенню процесу дорівнює зміні енергії Гельмгольца 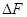 :
:
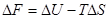 .
.
Енергія Гельмгольца характеризує напрямок самочинного перебігання хімічної реакції при ізохоро-ізотермічних умовах, що можливо, коли 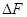
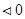 .
.
Зв’язок розглянутих термодинамічних функцій між собою наведено на рисунку.
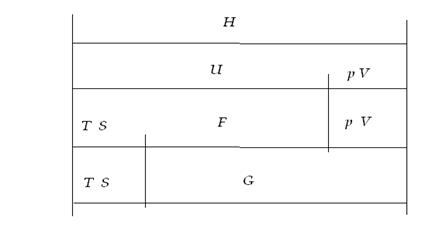
Рисунок. Зв’язок термодинамічних функцій між собою.
Тема 4. Хімічна рівновага. Хімічна спорідненість.
Закон діючих мас для оборотної реакції. Константа рівноваги хімічної реакції і способи її виразу. Ізотерма хімічної реакції Вант-Гоффа. Хімічна спорідненість. Вплив зовнішніх умов на положення рівноваги. Принцип рухомої рівноваги.
Розглянемо реакцію:
aА + вВ  сС + dD.
сС + dD.
Якщо при деякій температурі ентальпійний і ентропіяний фактори урівнюються, то 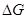 = 0 і виконується умова хімічної рівноваги. При цьому концентрації або парціальні тиски не змінюються у часі і звуться рівноважними. Якщо застосувати закон діючих мас для рівноважного стану то отримаємо:
= 0 і виконується умова хімічної рівноваги. При цьому концентрації або парціальні тиски не змінюються у часі і звуться рівноважними. Якщо застосувати закон діючих мас для рівноважного стану то отримаємо:
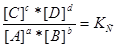 .
.
При хімічній рівновазі при постійних температурі і тиску відношення добутку рівноважних концентрацій продуктів реакції к добутку рівноважних концентрацій вихідних речовин є величина стала яка зветься константою рівноваги реакції КС. При цьому рівноважні концентрації беруться у ступенях, що відповідають стехіометричним коефіцієнтам.
Як видно з рівняння для константи рівноваги, її чисельне значення характеризує напрямок і повноту перебігання реакції. Якщо КС > 1 реакція пряма; КС <1 реакція зворотна. Чим більше константа рівноваги, тим більш повно перетворюються вихідні речовини. Для реакцій з участю тільки газоподібних речовин замість концентрації можна використовувати парціальні тиски компонентів. Тоді:
 .
.
Константа рівноваги, яка виражена через рівноважні концентрації - КС, пов’язана з константою рівноваги - КР співвідношенням: КР = КС(  , де
, де 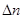 - зміна числа моль газу в результаті реакції:
- зміна числа моль газу в результаті реакції:  .
.
З термодинамічної точки зору можна визначити умови для можливості перебігання хімічної реакції за величиною зміни енергії Гіббса, яка являє собою за фізичним змістом максимальну корисну роботу 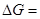 Аmax. Для ізобаро-ізотермічних умов зміна енергії Гіббса розраховується за рівняннями:
Аmax. Для ізобаро-ізотермічних умов зміна енергії Гіббса розраховується за рівняннями:
 ,
,
 ,
,
де: 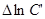 - різниця між натуральними логарифмами початкових концентрацій продуктів реакції і вихідних речовин з урахуванням стехіометричних коефіцієнтів;
- різниця між натуральними логарифмами початкових концентрацій продуктів реакції і вихідних речовин з урахуванням стехіометричних коефіцієнтів;
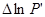 - різниця між натуральними логарифмами початкових парціальних тисків продуктів реакції і вихідних речовин з урахуванням стехіометричних коефіцієнтів. C’ і P’ не рівноважні концентрації і парціальні тиски.
- різниця між натуральними логарифмами початкових парціальних тисків продуктів реакції і вихідних речовин з урахуванням стехіометричних коефіцієнтів. C’ і P’ не рівноважні концентрації і парціальні тиски.
Ці рівняння звуться рівняннями ізотерми хімічної реакції. Величина  є кількісною мірою хімічної спорідненості реагуючих речовин, тобто здатності речовин вступати в хімічну взаємодію одна з одною. Чим більш негативною стає
є кількісною мірою хімічної спорідненості реагуючих речовин, тобто здатності речовин вступати в хімічну взаємодію одна з одною. Чим більш негативною стає  тим більшою стає К, тобто рівновага зміщується у бік утворення продуктів реакції.
тим більшою стає К, тобто рівновага зміщується у бік утворення продуктів реакції.
Зрівняння хімічної спорідненості різних реакцій здійснюють для умов, коли всі речовини, які приймають участь у реакції знаходяться у стандартному стані(початкові концентрації і тиски дорівнюють 1). Тоді:
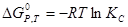
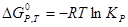
Розрахував величину  можливо визначити константу рівноваги хімічної реакції і, користуючись законом діючих мас, розрахувати рівноважні концентрації або парціальні тиски речовин, що взаємодіють.
можливо визначити константу рівноваги хімічної реакції і, користуючись законом діючих мас, розрахувати рівноважні концентрації або парціальні тиски речовин, що взаємодіють.
Зміна зовнішніх умов (зміна температури, тиску, введення в систему додаткової кількості одного з компонентів або його виведення з реакційної суміші, введення інертних речовин тощо) призводить до порушення сталої рівноваги і переходу системи до нового стану рівноваги. Якісно вплив зовнішніх умов на положення рівноваги оцінюється за допомогою принципу рухомої рівноваги (принципу Ле- Шательє):
При зовнішньому впливі на систему, яка знаходиться в стані рівноваги, в системі відбуваються зміни, спрямовані проти цих зовнішніх впливів.
Наприклад, при підвищенні зовнішнього тиску у системі відбуваються зміни, які повинні призводити до зменшення тиску, що можливо за рахунок зменшення об'єму системи. Таким чином, підвищення зовнішнього тиску зміщує рівновагу у бік зменшення числа молів реагуючих речовин. Наприклад, реакцію :
N2 + 3H2 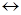 2NH3
2NH3
доцільно проводити при підвищеному тиску(у промисловості при 32 Мпа).
Додавання якої не будь речовини, яка приймає участь у реакції, призводить до зміщення рівноваги у бік тієї реакції, за якою ця речовина витрачається(це витікає з рівняння для константи рівноваги).
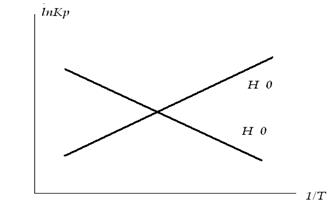
Величина константи рівноваги залежить від температури. У невеликому температурному інтервалі, якщо вважати зміну ентальпії сталою, ця залежність має вигляд:
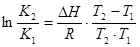
Для ендотермічних реакцій ( 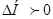 ) константа рівноваги при підвищені температури зростає, а для екзотермічної реакції зменшується, що узгоджується з принципом рухомої рівноваги. Цю залежність наведено на рисунку.
) константа рівноваги при підвищені температури зростає, а для екзотермічної реакції зменшується, що узгоджується з принципом рухомої рівноваги. Цю залежність наведено на рисунку.
Тема 5. Хімічна кінетика
Предмет хімічної кінетики. Швидкість хімічної реакції. Закон діючих мас. Молекулярність і порядок реакції. Односторонні реакції першого, другого і третього порядку. Період напіврозпаду. Вплив температури на швидкість хімічних реакцій. Правило Вант-Гоффа. Рівняння Ареніуса.
Хімічна кінетика вивчає швидкість і механізми хімічних реакцій, а також залежність швидкості реакції від різноманітних факторів.
Розрізняють середню( 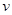 ) і істину(
) і істину( 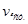 ) швидкість реакції. Середня швидкість – зміна концентрації реагуючих речовин у заданому інтервалі часу
) швидкість реакції. Середня швидкість – зміна концентрації реагуючих речовин у заданому інтервалі часу  :
:

С2 і С1 –відповідно концентрації речовин в моменти  і
і 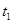 .
.
Істина швидкість – швидкість в даний момент часу як перша похідна концентрації С у часі:
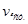 =
=  .
.
Знак + відноситься до речовини що утворюється, а знак – до вихідної речовини.
Залежність швидкості хімічної реакції від концентрації реагуючих речовин виражається законом діючих мас: швидкість реакції прямо пропорційна добутку молярних концентрацій реагуючих речовин, які взяті у ступенях їх стехіометричних коефіцієнтів. Для реакції аА+вВ+сС:
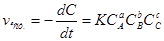 .
.
Коефіцієнт пропорційності К зветься константою швидкості реакції. Її фізичний сенс - це швидкість реакції при концентраціях реагуючих речовин 1 моль/л. Константа швидкості залежить від природи реагуючих речовин і температури.
Показники ступенів а,b,с звуться порядком реакції за речовинами (частковий порядок), а їх сумарне значення  зветься загальним порядком реакції. Порядок реакції може бути нульовим, цілочисельним і дробовим.
зветься загальним порядком реакції. Порядок реакції може бути нульовим, цілочисельним і дробовим.
Молекулярність реакції – число молекул, що беруть участь в елементарному акті хімічної взаємодії. Відповідно розрізняють одно-, бі- і тримолекулярні реакції.
Якщо реакція одночасно перебігає у прямому і зворотному напрямках вона зветься оборотною. У принципі усі реакції є оборотними, але у деяких реакціях рівновага сильно зміщена у бік утворення продуктів і вони за певних умов перебігають до практично повного зникнення вихідних речовин. Такі реакції звуть необоротними, або односторонніми.
Односторонніми реакціями першого порядку є в основному реакції розкладання, наприклад:
CaCO3 = CaO +CO2.
 Константа швидкості реакції першого порядку:
Константа швидкості реакції першого порядку:
 ,
,  ,
,
С0 - початкова концентрація речовини, моль/л;
Сx - кількість речовини, що прореагувала до моменту часу t від початку, моль/л.
Константа швидкості реакції другого порядку, типу H2 + I2 = 2HI:
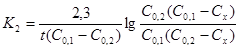 ,
, 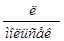 ?
?
якщо початкові концентрації речовин однакові:
 .
.
Для реакції третього порядку, наприклад 2NO + O2 = N2O4, якщо концентрації усіх речовин однакові:
 ,
, 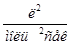 .
.
Іноді швидкість реакції оцінюють за періодом напіврозпаду 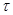 – часом, за який прореагує половина вихідної речовини. Для періоду напіврозпаду С=С0/2, тоді для реакцій першого, другого і третього порядку маємо кінетичні рівняння:
– часом, за який прореагує половина вихідної речовини. Для періоду напіврозпаду С=С0/2, тоді для реакцій першого, другого і третього порядку маємо кінетичні рівняння:
; ; .
Швидкість хімічної реакції в значній мірі залежить від температури. Для приблизного оцінювання впливу температури на швидкість хімічної реакції у незначному температурному інтервалі і при порівняно низьких температурах можна використовувати правило Вант-Гоффа: при збільшені температури на 10К швидкість реакції збільшується у 2-4 рази:
 .
.
KT1 і КT2 - швидкості реакції при температурах Т1 і Т2;
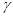 =2-4 - температурний коефіцієнт швидкості реакції.
=2-4 - температурний коефіцієнт швидкості реакції.
Більш точно залежність константи швидкості реакції від температури передається рівнянням Арреніуса:
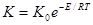 .
.
У цьому рівнянні:
К - константа швидкості;
К0 - предекспоненційний множник;
Е - енергія активації – кількість енергії, яка необхідна щоб перевести один моль молекул, що знаходяться у нормальному стані, в особливо активну, реакційно здатну форму, Дж/моль.
Якщо відомі константи швидкості реакції KT1 і КT2 при двох температурах Т1 і Т2 , енергію активації можна обчислити за рівнянням:
 .
.
