Раздел ii. молекулярная физика. термодинамика
ОСНОВНЫЕ ФОРМУЛЫ
1. Количество вещества однородного газа (в молях):
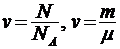 ,
,
где N - число молекул газа, NА - число Авогадро, m -масса газа, µ - молярная масса газа. Если система представляет смесь из нескольких газов, то количество вещества системы
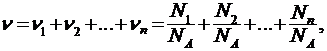
или
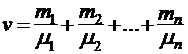 ,
,
где 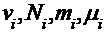 - соответственно количество вещества, число молекул, масса, молярная масса i -ой компоненты смеси.
- соответственно количество вещества, число молекул, масса, молярная масса i -ой компоненты смеси.
2. Уравнение Менделеева - Клапейрона (уравнение состояния идеального газа):
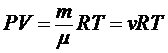 ,
,
где m - масса газа, µ - молярная масса газа, R - универсальная газовая постоянная, v - количество вещества, Т - термодинамическая температура Кельвина.
3. Опытные газовые законы, являющиеся частными случаями уравнения Менделеева - Клайперона для изопроцессов:
а) закон Бойля-Мариотта (изотермический процесс: Т = сonst, m = сonst):
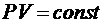 ,
,
или для двух состояний газа:
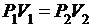 ,
,
где P1 и V1 - давление и объем газа в начальном состоянии, Р2 и V2 - те же величины в конечном состоянии.
б) закон Гей-Люссака (изобарический процесс Р = сonst, m = сonst )
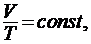
или для двух состояний:
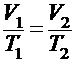 ,
,
где T1 и V1 температура и обьем газа в начальном состоянии, Т2 и V2 - те же величины в конечном состоянии.
в) закон Шарля (изохорический процесс V = сonst, m = сonst)
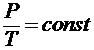 ,
,
или для двух состояний
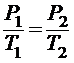 ,
,
где P1 и T1 - давление и температура газа в начальном состоянии, Р2 и Т2 - те же величины в конечном состоянии.
г) объединенный газовый закон (m = сonst)
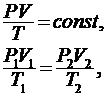
где 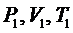 - давление, объем и температура газа в начальном состоянии Р2, V2, T2 - те же величины в конечном состоянии.
- давление, объем и температура газа в начальном состоянии Р2, V2, T2 - те же величины в конечном состоянии.
4. Закон Дальтона, определяющий давление смеси газов:
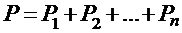 ,
,
где Pi - парциальное давление компонента смеси, n - число компонентов смеси.
5. Молярная масса смеси газов
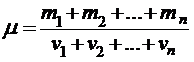 ,
,
где mi - масса i-го компонента смеси, 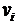 - количество вещества i-го компонента смеси, n - число компонентов смеси.
- количество вещества i-го компонента смеси, n - число компонентов смеси.
6. Массовая доля i-го компонента смеси газов (в долях единицы или в процентах):
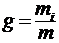 ,
,
где m - масса смеси.
7. Концентрация молекул (число молекул в единице объема)
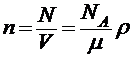 ,
,
где N - число молекул, содержащихся в данной системе, ρ - плотность вещества.
Формула справедлива не только для газов, но и для любого состояния вещества.
8. Основное уравнение кинетической теории газов:
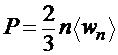 ,
,
где <wn> - средняя кинетическая энергия поступательного движения молекулы.
9. Средняя кинетическая энергия поступательного движения молекулы
 ,
,
где k - постоянная Больцмана.
10. Средняя полная кинетическая энергия молекулы:
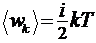 ,
,
где i - число степеней свободы молекулы.
11. Зависимость давления газа от концентрации молекул и от температуры:
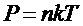 .
.
12. Скорости молекул:
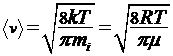 - средняя арифметическая,
- средняя арифметическая,
 - средняя квадратичная,
- средняя квадратичная,
 - наиболее вероятная,
- наиболее вероятная,
где 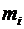 - масса одной молекулы.
- масса одной молекулы.
13. Относительная скорость молекулы:
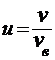 ,
,
где 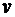 - скорость данной молекулы.
- скорость данной молекулы.
14. Удельные теплоемкости газов при постоянном объеме cV и при постоянном давлении сP:
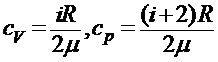 .
.
15. Связь между удельной (с) и молярной (С) теплоемкостями:
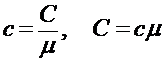 .
.
16. Уравнение Роберта Майера:
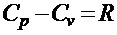 .
.
17. Внутренняя энергия идеального газа
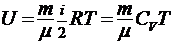 .
.
18. Первое начало термодинамики:
Q = ∆U + A,
где Q - теплота, сообщенная системе (газу), ΔU - изменение внутренней энергии системы. А - работа, совершенная системой против внешних сил.
19. Работа расширения газа:
в общем случае 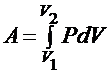 ,
,
при изобарическом процессе 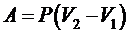 ,
,
при изотермическом процессе 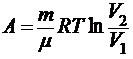 ,
,
при адиабатическом процессе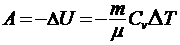
или
 ,
,
где 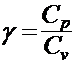 - показатель адиабаты.
- показатель адиабаты.
20. Уравнения Пуассона, связывающие параметры идеального газа при адиабатическом процессе:
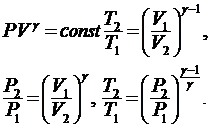
21. Термический КПД цикла:
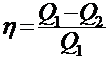 ,
,
где 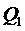 - теплота, полученная рабочим телом от нагревателя, Q2 - теплота, переданная рабочим телом охладителю.
- теплота, полученная рабочим телом от нагревателя, Q2 - теплота, переданная рабочим телом охладителю.
22. Термический КПД цикла Карно:
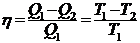 ,
,
где T1 и Т2 - термодинамические температуры нагревателя и температуры охладителя.
23. Коэффициент поверхностного натяжении:
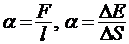 ,
,
где F - сила поверхностного натяжения, действующая на контур длиной 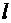 , ограничивающий поверхность жидкости, ∆Е - изменение свободной энергии поверхностной пленки жидкости, связанное с изменением площади ∆S поверхности этой пленки.
, ограничивающий поверхность жидкости, ∆Е - изменение свободной энергии поверхностной пленки жидкости, связанное с изменением площади ∆S поверхности этой пленки.
24. Формула Лапласа, выражающая давление Р, создаваемое сферической поверхностью жидкости:
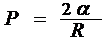 ,
,
где R - радиус сферической поверхности.
25. Высота подъема жидкости в капиллярной трубке:
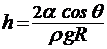 ,
,
где θ - краевой угол (θ = 0 при полном смачивании стенки трубки жидкостью, θ = π при полном несмачивании), R = радиус канала трубки,  - плотность жидкости, g - ускорение свободного падения.
- плотность жидкости, g - ускорение свободного падения.
27. Высота подъема жидкости между двумя близкими и параллельными друг другу плоскостями:
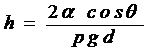 ,
,
где d - расстояние между плоскостями.
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
Пример 1. Определить число N молекул, содержащихся в объеме V = 1 мм3 воды, массу 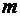 молекулы воды. Считая условно, что молекулы воды имеют вид шариков, соприкасающихся друг с другом, найти диаметр d молекул.
молекулы воды. Считая условно, что молекулы воды имеют вид шариков, соприкасающихся друг с другом, найти диаметр d молекул.
Решение: Число N молекул, содержащихся в некоторой массе равно произведению числа Авогадро 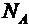 на количество вещества
на количество вещества 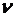 :
:
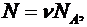
так как количество вещества:

μ - молярная масса, то
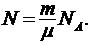
Выразив в этой формуле массу, как произведение плотности 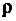 на объем V, получим
на объем V, получим
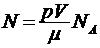 . (1)
. (1)
Подставим в формулу (1) следующие значения величин:  = 103 кг/м3,
= 103 кг/м3,
V = 1 мм3 = 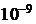 м
м 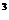 , μ =
, μ =  кг/моль,
кг/моль, 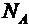 =
= 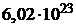 моль
моль  и произведем вычисления:
и произведем вычисления:
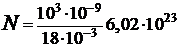 молекул = 3,34 1019молекул.
молекул = 3,34 1019молекул.
Массу  , одной молекулы можно найти делением молярной массы на число Авогадро:
, одной молекулы можно найти делением молярной массы на число Авогадро: 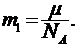
Подставим сюда числовые значения μ и 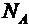 и найдем массу молекулы воды:
и найдем массу молекулы воды:
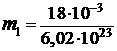 кг =
кг = 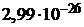 кг.
кг.
Если молекулы воды плотно прилегают друг к другу, то можно считать, что на каждую молекулу приходится объем (кубическая ячейка) 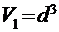 , где d - диаметр молекулы воды. Отсюда
, где d - диаметр молекулы воды. Отсюда
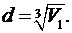 (2)
(2)
Объем 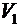 найдем, разделив молярный объем
найдем, разделив молярный объем 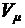 на число молекул в моле, т.е. на число Авогадро
на число молекул в моле, т.е. на число Авогадро 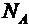 :
:
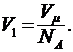
Подставим полученное выражение 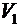 в формулу (2):
в формулу (2):
Входящий в эту формулу молярный объем определяется выражением 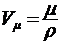 , тогда искомый диаметр молекулы:
, тогда искомый диаметр молекулы:
 (3)
(3)
Проверим, дает ли правая часть выражения (3) единицу длины:

Теперь подставим числовые значения физических величин в формулу (3) и произведем вычисления:
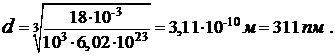
Пример 2. В баллоне объемом V = 10 л находится гелий под давлением Р 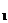 = 1 МПа и при температуре Т
= 1 МПа и при температуре Т 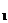 = 300 К. После того, как из баллона было взято m = 10 г гелия, температура в баллоне понизилась до Т
= 300 К. После того, как из баллона было взято m = 10 г гелия, температура в баллоне понизилась до Т 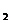 = 290 К. Определить давление Р
= 290 К. Определить давление Р 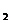 гелия, оставшегося в баллоне.
гелия, оставшегося в баллоне.
Решение: Для решения задачи воспользуемся уравнением Менделеева-Клапейрона, применив его к конечному состоянию газа:
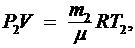 (1)
(1)
где 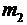 - масса гелия в баллоне в конечном состоянии, μ - молярная масса гелия, R - универсальная газовая постоянная. Из уравнения (1) выразим искомое давление Р
- масса гелия в баллоне в конечном состоянии, μ - молярная масса гелия, R - универсальная газовая постоянная. Из уравнения (1) выразим искомое давление Р 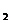 .
.
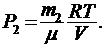 (2)
(2)
Массу гелия m2 выразим через массу m1, соответствующую начальному состоянию и массу m гелия, взятого из баллона:
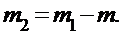 (3)
(3)
Массу гелия m найдем также из уравнения Менделеева-Клапейрона, применив его к начальному состоянию
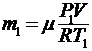 (4)
(4)
Подставляя в выражение (3) массу из формулы (4), а затем полученное выражение в формулу (2), найдем:
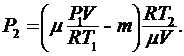
После преобразования и сокращения находим:
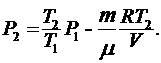 (5)
(5)
Левая часть расчётной формулы (5) выражает давление, имеет размерность 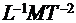 . Проверим размерность правой части. Размерность первого слагаемого не вызывает сомнения, т.к. отношение температур – величина безразмерная. Размерность второго слагаемого:
. Проверим размерность правой части. Размерность первого слагаемого не вызывает сомнения, т.к. отношение температур – величина безразмерная. Размерность второго слагаемого:
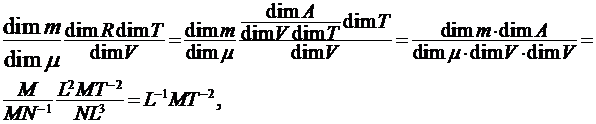
что совпадает с размерностью давления.
Убедившись в том, что размерность правой и левой частей формулы (5) одинаковы, выразим величины,входящие в эту формулу, в единицах СИ и произведем вычисления:
P1 = 1 МПа =106 Па, 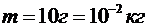 ,
, 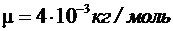 ,
,
R = 8,31 Дж/(мольК), T1 = 300 К, T2 = 290 К,
V = 10 л = 10-2 м3,
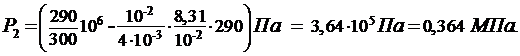
Пример 3.Баллон содержит  = 80 г кислорода и
= 80 г кислорода и 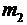 = 320 г аргона. Давление смеси Р = 1 МПа, температура Т = 300 К. Принимая данные газа за идеальные, определить объем V баллона.
= 320 г аргона. Давление смеси Р = 1 МПа, температура Т = 300 К. Принимая данные газа за идеальные, определить объем V баллона.
Решение. По закону Дальтона давление смеси равно сумме парциальных давлений газов, входящих всостав смеси. Парциальным давлением газа называется давление, которое производил бы этот газ, если бы только он один находился в сосуде, занятым смесью. По уравнению Менделеева-Клапейрона, парциальные давления кислорода 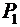 и аргона
и аргона 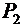 выражается формулами:
выражается формулами:
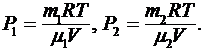
Следовательно, по закону Дальтона давление смеси газов

откуда объем баллона:
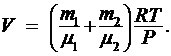
Выразим в единицах СИ числовые значения величин, входящих в эту формулу m1 = 80 г = 0,8 кг, 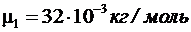 , m2 = 330 г = 0,33 кг,
, m2 = 330 г = 0,33 кг, 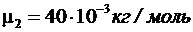 , m2 = 40 10-3 кг/моль, P1 = 1 МПа = 106 Па, R = 8,31 Дж/(мольК), подставим числовые значения в формулу и произведем вычисления:
, m2 = 40 10-3 кг/моль, P1 = 1 МПа = 106 Па, R = 8,31 Дж/(мольК), подставим числовые значения в формулу и произведем вычисления:
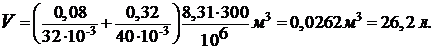
Пример 4. Найти среднюю кинетическую энергию 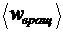 вращательного движения одной молекулы кислорода при температуре Т = 350 К, а также кинетическую энергию
вращательного движения одной молекулы кислорода при температуре Т = 350 К, а также кинетическую энергию 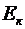 вращательного движения всех молекул кислорода массой m = 4 г.
вращательного движения всех молекул кислорода массой m = 4 г.
Решение: Известно, что на каждую степень свободы молекулы газа приходится одинаковая средняя энергия 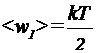 , где
, где 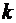 - постоянная Больцмана, Т - абсолютная температура газа. Так как вращательному движению двухатомной молекулы (молекула кислорода двухатомная) соответствует две степени свободы, то средняя энергия вращательного движения молекулы кислорода выразится формулой:
- постоянная Больцмана, Т - абсолютная температура газа. Так как вращательному движению двухатомной молекулы (молекула кислорода двухатомная) соответствует две степени свободы, то средняя энергия вращательного движения молекулы кислорода выразится формулой:
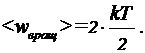 (1)
(1)
Подставив в формулу (1) значение 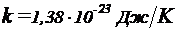 и T = 350 К получим
и T = 350 К получим 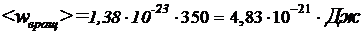 . Кинетическая энергия вращательного движения всех молекул газа определяется равенством:
. Кинетическая энергия вращательного движения всех молекул газа определяется равенством:
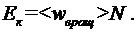 (2)
(2)
Число всех молекул газа можно вычислить по формуле:
 (3)
(3)
где  число Авогадро,
число Авогадро, 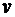 - количество вещества. Если учесть, что количество вещества
- количество вещества. Если учесть, что количество вещества 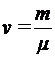 , где
, где 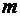 - масса газа, μ - молярная масса газа, то формула (3) примет вид:
- масса газа, μ - молярная масса газа, то формула (3) примет вид:

Подставив это выражение в формулу (2) получим:
 (4)
(4)
Выразим величины, входящие в эту формулу, в единицах СИ:
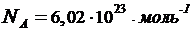 ,
, 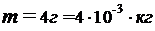 ,
, 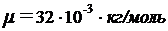 ,
, 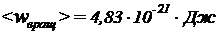 . Подставив эти значения в формулу (4), найдем:
. Подставив эти значения в формулу (4), найдем: 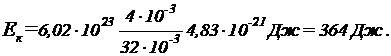
Пример 5. Вычислить удельные теплоемкости при постоянном объеме 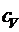 и при постоянном давлении
и при постоянном давлении 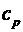 неона и водорода, принимая эти газы за идеальные.
неона и водорода, принимая эти газы за идеальные.
Решение: Удельные теплоемкости идеальных газов выражаются формулами
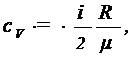 (1)
(1)
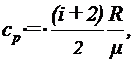 (2)
(2)
где 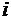 - число степеней свободы молекул газа,
- число степеней свободы молекул газа,  - молярная масса. Для неона (одноатомный газ)
- молярная масса. Для неона (одноатомный газ) 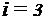 ,
, 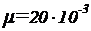 кг/моль (см. справочную таблицу). Вычисляя по формулам (1) и (2), получим:
кг/моль (см. справочную таблицу). Вычисляя по формулам (1) и (2), получим: 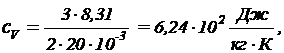

Для водорода (двухатомный газ) 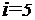 ,
, 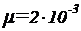 кг/моль. Вычисляя по тем же формулам, получим:
кг/моль. Вычисляя по тем же формулам, получим:
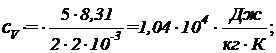
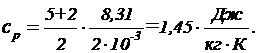
Пример 6. Вычислить удельные теплоемкости 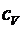 и
и 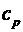 смеси неона и водорода, если массовая доля неона
смеси неона и водорода, если массовая доля неона 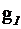 = 80%, массовая доля водорода
= 80%, массовая доля водорода 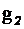 = 20%. Значение удельных теплоемкостей газов взять из предыдущего примера.
= 20%. Значение удельных теплоемкостей газов взять из предыдущего примера.
Решение: Удельную теплоемкость смеси при постоянном объеме 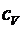 найдем следующим образом. Теплоту, необходимую для нагревания смеси на
найдем следующим образом. Теплоту, необходимую для нагревания смеси на 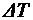 , выразим двумя способами.
, выразим двумя способами.

 (1)
(1)
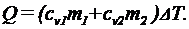 (2)
(2)
где 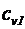 - удельная теплоемкость неона,
- удельная теплоемкость неона, 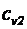 - удельная теплоемкость водорода. Приравняв правые части (1) и (2) и разделив обе части полученного равенства на
- удельная теплоемкость водорода. Приравняв правые части (1) и (2) и разделив обе части полученного равенства на 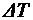 . получим:
. получим:
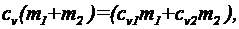
отсюда
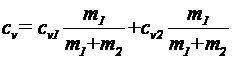 (3)
(3)
или
 (4)
(4)
где 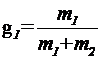 и
и 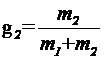 - массовые доли неона и водорода в смеси. Подставив в формулу (4) числовые значения величин, найдем:
- массовые доли неона и водорода в смеси. Подставив в формулу (4) числовые значения величин, найдем:
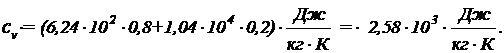
Рассуждая таким же образом, получим формулу для вычисления удельной теплоемкости смеси при постоянном давлении:
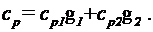 (5)
(5)
Подставим в формулу (5) числовые значения величин:
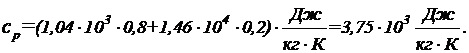
Пример 7. Кислород массой m = 2 кг занимает объем равный V = 1 м3 и находится под давлением P 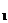 = 0,2 МПа. Газ был нагрет сначала при постоянном давлении до объема V2= 3 м3, а затем при постоянном объеме до давления Р
= 0,2 МПа. Газ был нагрет сначала при постоянном давлении до объема V2= 3 м3, а затем при постоянном объеме до давления Р 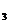 = 0,5 МПа. Найти изменение внутренней энергии газа, совершенную им работу А и теплоту Q , переданную газу. Построить график процесса.
= 0,5 МПа. Найти изменение внутренней энергии газа, совершенную им работу А и теплоту Q , переданную газу. Построить график процесса.
Решение: Изменение внутренней энергии газа выражается формулой:
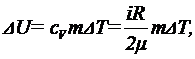 (1)
(1)
где i - число степеней свободы молекул газа (для двухатомных молекул кислорода i = 5), μ - молярная масса. Начальную и конечную температуру газа найдем из уравнения Клапейрона-Менделеева:
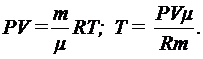 (2)
(2)
Выпишем заданные величины в единицах системы СИ:  ,
, 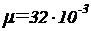 кг/моль,
кг/моль, 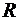 = 8,31 Дж/моль К, V
= 8,31 Дж/моль К, V 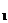 = 1 м
= 1 м 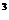 , V2 = V3 = 3 м 3, P
, V2 = V3 = 3 м 3, P 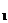 = P2 = 0,2 МПа = 2
= P2 = 0,2 МПа = 2 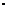 105 Па, Р
105 Па, Р 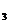 = 0,5 МПа = 5
= 0,5 МПа = 5 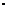 105 Па. Подставляя эти значения в выражение (2) и выполняя арифметические действия, получим:
105 Па. Подставляя эти значения в выражение (2) и выполняя арифметические действия, получим:
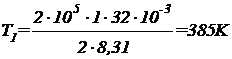 ;
;
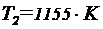 ;
; 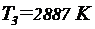 .
.
Подставляя в выражение (1) числовые значения величин, входящих в него и выполняя арифметические действия, находим:
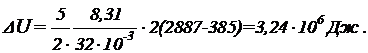
Работа расширения газа при постоянном давлении выражается формулой:
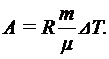
Подставим числовые значения величин, получим:
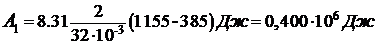 .
.
Работа газа, нагреваемого при постоянном объеме, равна нулю, т.е. 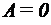 . Следовательно, полная работа, совершенная газом, равна
. Следовательно, полная работа, совершенная газом, равна
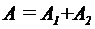 =
= 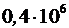 Дж.
Дж.
Согласнопервому началу термодинамики теплота Q, переданная газу, равна сумме изменения внутренней энергии и работы A: 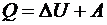 , следовательно
, следовательно  .
.
Пример 8. Тепловая машина работает по обратному циклу Карно. Температура нагревателя T 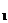 = 500 К. Определить термический КПД цикла и температуру Т2 охладителя тепловой машины, если за счет каждого килоджоуля теплоты, полученной от нагревателя, машина совершает работу А = 350 Дж.
= 500 К. Определить термический КПД цикла и температуру Т2 охладителя тепловой машины, если за счет каждого килоджоуля теплоты, полученной от нагревателя, машина совершает работу А = 350 Дж.
Решение: Термический КПД тепловой машины, называемый также коэффициентом использованной теплоты, показывает, какая доля теплоты, полученной от нагревателя, превращается в механическую работу. Термический КПД выражается формулой:
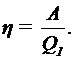
где Q 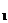 - теплота, полученная от нагревателя, А - работа, совершаемая рабочим телом тепловой машины. Подставив числовые значения в эту формулу, получим
- теплота, полученная от нагревателя, А - работа, совершаемая рабочим телом тепловой машины. Подставив числовые значения в эту формулу, получим

Зная КПД цикла, можно по формуле 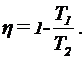 определить температуру охладителя Т2:
определить температуру охладителя Т2:

Подставив в эту формулу полученное значение КПД и температуры T 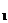 нагревателя, получим:
нагревателя, получим:
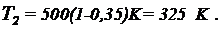
Пример 9. Найти добавочное давление внутри мыльного пузыря диаметром d = 10 см. Какую работу нужно совершить, чтобы выдуть этот пузырь?
Решение: Пленка мыльного пузыря имеет две сферические поверхности - внешнюю и внутреннюю. Обе поверхности оказывают давление на воздух, заключенный внутри пузыря. Так как толщина пленки чрезвычайно мала, то диаметры обеих поверхностей практически одинаковы. Поэтому добавочное давление, где 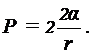 - . где
- . где 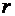 радиус пузыря. Так как
радиус пузыря. Так как 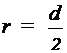 , то
, то 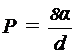 . Коэффициент поверхностного натяжения мыльной воды 40 мН/м (см. справочную табл.) диаметр пузыря = 10 см = 0,1 м.
. Коэффициент поверхностного натяжения мыльной воды 40 мН/м (см. справочную табл.) диаметр пузыря = 10 см = 0,1 м.
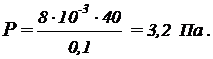
Работа, которую нужно совершить, чтобы, растягивая пленку, увеличить её поверхность на 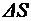 , выражается формулой
, выражается формулой
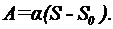
В данном случае  - общая площадь двух сферических поверхностей пленки, затягивающей отверстие трубки до выдувания пузыря, пренебрегая
- общая площадь двух сферических поверхностей пленки, затягивающей отверстие трубки до выдувания пузыря, пренебрегая  , получим
, получим
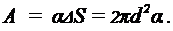
Подставив числовые значения величин, получим:
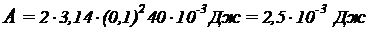 .
.
ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
200. Определить количество вещества v и число N молекул кислорода массой m = 0,5 кг.
201. Сколько атомов содержится в ртути 1) количеством вещества  = 0.2 моль, 2) массой m = 1 г.
= 0.2 моль, 2) массой m = 1 г.
202. Вода при температуре  занимает объем
занимает объем 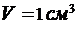 . Определить количество вещества
. Определить количество вещества 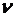 и число N молекул воды.
и число N молекул воды.
203. Найти молярную массу 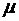 и массу одной молекулы поваренной соли.
и массу одной молекулы поваренной соли.
204. Определить массу m одной молекулы поваренной соли.
205. Определить концентрацию n молекул кислорода, находящего в сосуде объемом V = 2 л. Количество v вещества кислорода равно 0,2 моль.
206. Определить количество вещества водорода, заполняющего сосуд объемом V = 3 л, если концентрация молекул газа в сосуде 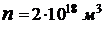 .
.
207. Газ в колбе емкостью  , находящейся при температуре
, находящейся при температуре  , разрежен до давления 550 мм. рт. ст. Определить, сколько молекул содержится в колбе и число молей газа.
, разрежен до давления 550 мм. рт. ст. Определить, сколько молекул содержится в колбе и число молей газа.
208. Из сосуда испарилось за 10 суток 100 г воды. Сколько в среднем молекул вылетало из сосуда за одну секунду?
209. Сколько молей и какое количество молекул газа находится в баллоне объемом 2 литра, если температура газа 47°C, а давление 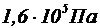 ?
?
210. В сосуде объемом 0,7 м3 находится смесь 8 кг водорода и 4 кг кислорода при температуре 7°C. Определить давление и молярную массу смеси газа.
211. В сосуде объемом 200 литров содержится азот при температуре 2°C. Часть азота израсходовали и давление снизилось на  Па. Сколько израсходовано газа?
Па. Сколько израсходовано газа?
212. Азот находится под давлением  Па и занимает объем 2,8 л. Масса азота 56 г. На сколько изменится температура газа, если его объем уменьшится в два раза, а давление увеличится до
Па и занимает объем 2,8 л. Масса азота 56 г. На сколько изменится температура газа, если его объем уменьшится в два раза, а давление увеличится до 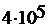 Па?
Па?
213. Каково будет давление воздуха, если 5 л его сжаты до объема 1,5 л при неизменной температуре? Начальное давление воздуха 690 мм. рт. ст. Постройте по точкам график процесса в координатах P, V.
214. В баллоне при давлении  Па содержится газ при температуре 47°C. Когда 1/3 массы газа была выпущена из баллона, температура снизилась на 20°C. Как изменилось давление?
Па содержится газ при температуре 47°C. Когда 1/3 массы газа была выпущена из баллона, температура снизилась на 20°C. Как изменилось давление?
215. В сосуде объемом V = 40 л находится кислород при температуре T = 300 K. Когда часть кислорода израсходовали, давление в баллоне понизилось на 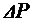 = 100 кПа. Определить массу израсходованного кислорода, если его температура не изменилась.
= 100 кПа. Определить массу израсходованного кислорода, если его температура не изменилась.
216. Два сосуда одинакового объема содержат кислород. В одном сосуде давление 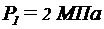 и температура
и температура  , в другом
, в другом 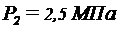 ,
, 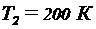 . Сосуды соединили трубой и охладили находящийся в них кислород до
. Сосуды соединили трубой и охладили находящийся в них кислород до 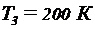 . Определить установившееся в сосудах давление.
. Определить установившееся в сосудах давление.
217. Смесь кислорода и азота находится в сосуде под давлением P = 1,2 МПа. Определить парциальное давление 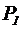 и
и  газов, если массовая доля кислорода в смеси составляет 20%.
газов, если массовая доля кислорода в смеси составляет 20%.
218. Смесь водорода и азота общей массой m = 290 г при температуре T = 600 К и давлении P = 2,46 МПа занимает объем V = 30 л. Определить массу водорода и массу азота.
219. Смесь азота с массовой долей 87,5% и водорода с массовой долей 12,5% находится в сосуде объемом V = 20 л при температуре T = 560 К. Определить давление P смеси, если масса смеси равна 8 г.
220. Определить суммарную кинетическую энергию 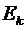 поступательного движения всех молекул газа, находящегося в сосуде объемом V = 3 л под давлением P = 540 кПа.
поступательного движения всех молекул газа, находящегося в сосуде объемом V = 3 л под давлением P = 540 кПа.
221. Количество вещества гелия v = 1,5 моль, температура T = 120 К. Определить суммарную кинетическую энергию 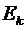 поступательного движения всех молекул этого газа.
поступательного движения всех молекул этого газа.
222. Определить среднюю кинетическую энергию <w> одной молекулы водяного пара при температуре T = 500 К.
223. Определить среднюю квадратную скорость < 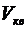 > молекул газа, заключенного в сосуде объемом V = 2 л под давлением P = 200 кПа. Масса газа m = 0,3 г.
> молекул газа, заключенного в сосуде объемом V = 2 л под давлением P = 200 кПа. Масса газа m = 0,3 г.
224. В азоте взвешены мельчайшие пылинки, которые движутся так, как если бы они были очень крупными молекулами. Масса m каждой пылинки равна 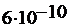 г. Газ находится при температуре T = 400 К. Определить средние квадратичные скорости <
г. Газ находится при температуре T = 400 К. Определить средние квадратичные скорости < 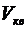 >, а так же средние кинетические энергии поступательного движения молекул азота и пылинки.
>, а так же средние кинетические энергии поступательного движения молекул азота и пылинки.
225. Вычислить кинетические энергии поступательного, вращательного движений и полную кинетическую энергию молекул аргона, кислорода и паров воды при температуре 27°C, а также средние квадратичные скорости молекул.
226. Определить полную энергию молекул азота, который находится в баллоне объемом V = 100 л при давлении 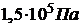 .
.
227. При температуре 37°C движется взвешенные в воздухе мельчайшие пылинки массой 10-12 кг каждая. Определить среднюю квадратичную, среднюю арифметическую и наиболее вероятную скорости пылинок.
228. Кислород находится под давлением 1,2 атм, молекулы имеют среднюю квадратичную скорость 500 м/с. Определить среднюю длину свободного пробега молекул.
229. Найти среднее число столкновений <z> в единицу времени и длину свободного пробега <l> молекулы гелия, если газ находится под давлением P = 2 кПа при температуре T = 200 К.
230. Определить показатель адиабаты 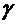 азота, который при температуре T = 350 К и давлении P = 0,4 МПа занимает объем V = 300 л и имеет теплоемкость C = 857 Дж/К.
азота, который при температуре T = 350 К и давлении P = 0,4 МПа занимает объем V = 300 л и имеет теплоемкость C = 857 Дж/К.
231. В сосуде объемом V = 6 л находится при нормальных условиях двухатомный газ. Определить теплоемкость 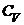 этого газа при постоянном объеме.
этого газа при постоянном объеме.
232. Определить молярные теплоемкости газа, если его удельные теплоемкости cV = 10,4 кДж/кгК и cp = 14,6 кДж/кгК.
233. Найти удельные 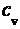 ,
,  и молярные
и молярные 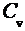 и
и 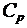 теплоемкости азота и гелия.
теплоемкости азота и гелия.
234. Вычислить удельные теплоемкости газа, зная, что его молярная масса 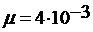 кг/моль и отношение теплоемкостей
кг/моль и отношение теплоемкостей 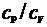 =1,67.
=1,67.
235. Трехатомный газ под давлением P = 240 кПа и температуре t = 20°C занимает объем V = 10 л. Определить теплоемкость 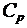 этого газа при постоянном давлении.
этого газа при постоянном давлении.
236. Удельная теплоемкость газа 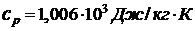 . Отношение
. Отношение 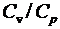 = 1,4. Определить молярную массу газа.
= 1,4. Определить молярную массу газа.
237. Определить относительную молекулярную массу 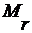 и молярную массу
и молярную массу 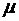 газа, если его разность удельных теплоемкостей показатель
газа, если его разность удельных теплоемкостей показатель 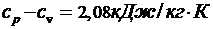 .
.
238. Смесь двух газов состоит из гелия массой m1 = 5 г и водорода массой m2 = 2 г. Найти отношение теплоемкостей 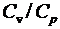 этой смеси.
этой смеси.
239. Относительная молярная масса Mr = 30, показатель адиабаты g = 1,40. Вычислить удельные теплоемкости  и
и 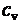 этого газа.
этого газа.
240. Определить изменение внутренней энергии 10 кг водорода при изобарическом расширении, если в процессе нагревания температура повысилась на 100°С.
241. В баллоне емкостью 10 дм3 содержится кислород при температуре 30°C и под давлением 107 Па. При нагревании кислород получил  Дж теплоты. Определить температуру и давление кислорода после нагревания.
Дж теплоты. Определить температуру и давление кислорода после нагревания.
242. Водород занимает объем V = 1 м3 при давлении 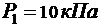 . Газ нагрели при постоянном давлении
. Газ нагрели при постоянном давлении  . Определить изменение внутренней энергии газа и теплоту, сообщенную газу.
. Определить изменение внутренней энергии газа и теплоту, сообщенную газу.
243. Кислород при неизменном давлении P = 100 кПа нагревается. Его объем увеличивается от V1 = 1 м3 до V2 = 2 м3. Определить изменение внутренней энергии кислорода.
244. В цилиндре под поршнем находится азот, имеющий массу m = 5 кг и занимающий объем V1 = 8 м3 при температуре 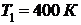 . После нагревания объем газа V2 = 27 м3, температура осталась неизменной. Найти работу расширения газа.
. После нагревания объем газа V2 = 27 м3, температура осталась неизменной. Найти работу расширения газа.
245. Один моль гелия изобарически расширяется от объема 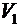 = 5 л до объема
= 5 л до объема 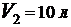 при давлении
при давлении 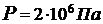 . Определить изменение внутренней энергии тела в этом процессе.
. Определить изменение внутренней энергии тела в этом процессе.
246. Один грамм кислорода ( 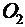 ) нагревается от
) нагревается от 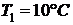 до
до  при P = const. Определить изменение внутренней энергии.
при P = const. Определить изменение внутренней энергии.
247. Два грамма азота нагреваются от  до
до 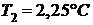 при V = const. Определить изменение внутренней энергии.
при V = const. Определить изменение внутренней энергии.
248. Один грамм кислорода нагревается от 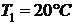 до
до 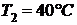 при
при 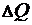 = 0. Определить изменение внутренней энергии.
= 0. Определить изменение внутренней энергии.
249. Азот занимает объем  и находится под давлением P1 = 105 Па. Газ нагревают при постоянном объеме до давления P2 = 5∙105 Па. Масса азота m = 3 кг. Определить из<
и находится под давлением P1 = 105 Па. Газ нагревают при постоянном объеме до давления P2 = 5∙105 Па. Масса азота m = 3 кг. Определить из<
