Барометрическая формула. Распределение Больцмана.
Таким образом, зависимость атмосферного давления от высоты выражается формулой:
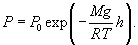
Исходя из основного уравнения молекулярно-кинетической теории: P = nkT, заменим P и P0 в барометрической формуле (2.4.1) на n и n0 и получим распределение Больцмана для молярной массы газа:
 | (2.5.1) |
где n0 и n - число молекул в единичном объёме на высоте h = 0 и h.
Так как 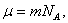 а
а  , то (2.5.1) можно представить в виде
, то (2.5.1) можно представить в виде
 |
14 внутренняя энергия, работа, теплота. Первое начало термодинамики и его применение к изопроцессам. Первый закон термодинамики гласит, (4 разные формулировки) что :
- Энергия не может быть создана или уничтожена (закон сохранения энергии), она лишь переходит из одного вида в другой в различных физических процессах. Отсюда следует, что внутренняя энергия изолированной системы остается неизменной.
- Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы против внешних сил.
- Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданной системе и не зависит от способа, которым осуществляется этот переход.
- Изменение внутренней энергии неизолированной термодинамической системы равно разности между количеством теплоты, переданной системе, и работой, совершенной системой над внешними силами.
- Внутренняя энергия ( Internal Energy) - Внутренняя энергия определяется как энергия случайных, находящихся в неупорядченном движении молекул. Энергия молекул находится в диапазоне от высокой, необходимой для движения, до заметной лишь с помощью микроскопа энергии на молекулярном или атомном уровне. Например, у стакана с водой комнатной температы, стоящего на столе нет, на первый взгляд, никакой энергии: ни кинетической, ни потенциальной относительно стола. Но, с помощью микроскопа становится заметна "бурлящая" масса быстро двигающихся молекул. Если выплеснуть воду из стакана, эта микроскопическая энергия не обязательно заметно изменится, когда мы усредним добавленную кинетическую энергию на все молекулы воды.
- Тепло - Тепло может быть определено, как энергия, передаваемая от объекта с более высокой температурой к объекту с менее высокой температурой. Сам по себе объект не обладает "теплом"; соответствующий термин для микроскопической энергии объекта - внутренняя энергия. Внутренняя энергия может увеличиваться путем переноса энергии к объекту от объекта, имеющего температуру выше - этот процесс называется нагревом.
- Работа - Когда работа совершается термодинамической системой (чаще всего это газ, который совершает работу), то работа совершенная газом при постоянном давлении определяется как :W = p dV, где W - работа, p - давление, а dV -изменение объема.
В случаях когда давление не является постоянным, работа может быть представлена интегральным образом, как площадь поверхности под кривой в координатах давление, объем, которые представляют происходящий процесс.
15 энтропия, ее статистическое толкование и связь с термодинамической вероятностью.Понятие энтропии впервые введено в 1865 г. Р. Клаузиусом. Для определения физического содержания этого понятия берут отношение теплоты Q, которое получило тело в изотермическом процессе, к температуре Т теплоотдающего тела, называемое приведенным количеством теплоты.
Приведенное количество теплоты, которое сообщается телу на малом участке процесса, равно δQ/T. Строгий формальный анализ показывает, что приведенное количество теплоты, которое сообщается телу в любом обратимом круговом процессе, равно нулю:
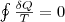 (1)
(1)
Из равенства нулю интеграла (1), взятого по замкнутому контуру, следует, что подынтегральное выражение δQ/T есть полный дифференциал некоторой функции, которая определяется только состоянием системы и не зависит от пути, которым система пришла в это состояние. Таким образом,
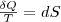 (2)
(2)
Функция состояния, у которой дифференциал равен δQ/T, называется энтропией и обозначается S.
Из формулы (1) следует, что для обратимых процессов изменение энтропии
 (3)
(3)
В термодинамике доказывается, что энтропия системы, совершающей необратимый цикл, возрастает:
 (4)
(4)
Выражения (3) и (4) применяются только к замкнутым системам, если же система обменивается теплотой с внешней средой, то ее энтропия может вести себя произвольным образом. Соотношения (3) и (4) можно представить в виде неравенства Клаузиуса
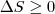 (5)
(5)
т. е. энтропия замкнутой системы может либо возрастать (в случае необратимых процессов), либо оставаться постоянной (в случае обратимых процессов).
Если система совершает равновесный переход из состояния 1 в состояние 2, то, согласно (2), изменение энтропии
 (6)
(6)
где подынтегральное выражение и пределы интегрирования определяются через величины, которые характеризуют рассматриваемый процесс. Формула (6) определяет энтропию лишь с точностью до аддитивной постоянной (слагаемого). Физический смысл имеет не сама энтропия, а разность энтропий.
Используя выражение (6), найдем изменение энтропии в процессах идеального газа. Taк как dU=(m/M)CVdT, δA=pdV=(m/M)RT(dV/V) , то
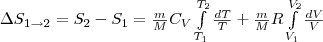
или
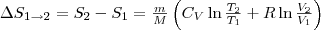 (7)
(7)
т. е. изменение энтропии ΔS1→2 идеального газа при переходе его из cоcтояния 1 в cоcтояние 2 не завиcит от вида процеccа перехода 1→2.
Так как для адиабатического процесса δQ = 0, то ΔS = 0 и, следовательно, S=const, т. е. адиабатический обратимый процесс протекает при постоянной энтропии. Поэтому его часто называют изоэнтропийным процессом. Из формулы (7) следует, что при изотермическом процессе (T1= T2)
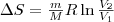
при изохорном процессе (V1 = V2)

Энтропия обладает свойством аддитивности: энтропия системы равна сумме энтропий тел, которые входят в систему. Свойством аддитивности обладают также внутренняя энергия, масса, объем (но таким свойством не обладают температура и давление).
Более глубокий смысл энтропии показывается в статистической физике: энтропия связывается с термодинамической вероятностью состояния системы. Термодинамическая вероятность W состояния системы — это число способов, с помощью которых может быть реализовано данное состояние макроскопической системы, или число микросостояний, которые осуществляют данное макросостояние (по определению, W≥1, т. е. термодинамическая вероятность не есть вероятность в математическом смысле (последняя ≥1 !!!)).
Cогласно Больцману, энтропия cиcтемы и термодинамическая вероятность связаны между собой следующим образом:
 (8)
(8)
где k — постоянная Больцмана. Таким образом, энтропия определяется логарифмом числа микросостояний, с помощью которых может быть осуществлено данное макросостояние.
16 второе начало термодинамики.Второе начало термодинамики может быть сформулировано несколькими способами. В наиболее очевидной формулировке второе начало гласит, что невозможен самопроизвольный переход тепла от тела, менее нагретого, к телу, более нагретому. Более строго, невозможны такие процессы, единственным конечным результатом которых был бы переход тепла от тела, менее нагретого, к телу, более нагретому.
Второе начало термодинамики может быть также сформулировано следующим образом: невозможны такие процессы, единственным конечным результатом которых явилось бы отнятие от некоторого тела определенного количества тепла и превращения этого тепла полностью в работу.
На первый взгляд может показаться, что второй формулировке противоречит, например, процесс изотермического расширения идеального газа. Действительно, все полученное идеальным газом от какого-то тела тепло превращается полностью в работу. Однако получение и превращение его в работу не единственный конечный результат процесса, кроме того, в результате происходит изменение объема газа.
Легко убедиться, что утверждение, содержащееся во второй формулировке, логически вытекает из утверждения, заключенного в первой формулировке. В самом деле, работа может быть полностью превращена в тепло, например, при трении. Поэтому, превратив с помощью процесса, запрещенного второй формулировкой, тепло, отнятое от какого-либо тела, полностью в работу, а затем превратив эту работу при посредстве трения в тепло, сообщаемое другому телу с более высокой температурой, мы осуществим процесс, невозможный согласно первой формулировке.
17 замкнутые процессы. Цикл карно. Кпд.Процессы, в которых термодинамические состояния рабочего тела в начале и в конце совпадают, называются замкнутыми процессами или циклами. Цикл Карно является обратимым циклическим процессом с двумя источниками теплоты, имеющими разные, но постоянные температуры. Так как температуры источников тепла постоянные, а процессы получения и отдачи рабочим веществом тепла должны быть обратимыми, то эти процессы могут быть только изотермическими. При этом температура рабочего вещества в цикле должна, очевидно, меняться без теплообмена с окружающей средой, т.е. в адиабатных условиях. Поэтому цикл Карно состоит из двух обратимых изотермических и двух обратимых адиабатных процессов, чередующихся между собой.
