Основное уравнение массопередачи при абсорбции.
Абсорбция (десорбция) — диффузионный пр-с, в к-ом участвуют две фазы: газовая и жидкая. Движущей силой пр-са абсорбции (десорбции) является разность парциальных давлений поглощаемого компонента в газовой и жидкой фазах, который стремится перейти в ту фазу, где его концентрация меньше, чем это требуется по условию равновесия.
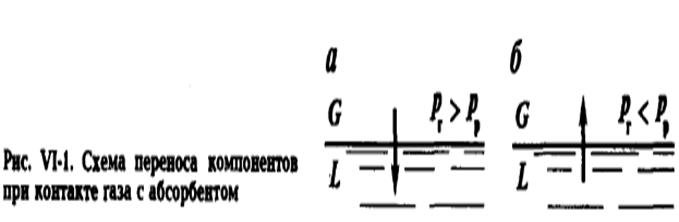
Обозначим парциальное давление поглощаемого компонента в газовой фазе через рг, а парциальное давление того же компонента в газовой фазе, находящейся в равновесии с абсорбентом, через рр. Если рг > рр, то компонент газа переходит в жидкость, т.е. протекает процесс абсорбции . Если рг < рр, то поглощенные компоненты газа переходят из абсорбента в газовую фазу, т.е. осуществляется процесс десорбции .
Чем больше величина рг — рр, тем интенсивнее осуществляется переход компонента из газовой фазы в жидкую. При приближении системы к состоянию равновесия движущая сила уменьшается и скорость перехода компонента из газовой фазы в жидкую замедляется. Поскольку парциальное давление компонента пропорционально его концентрации, то движущая сила процесса абсорбции или десорбции может быть выражена также через разность концентраций компонента в газовой 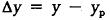 или жидкой фазе
или жидкой фазе 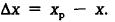 .
.
Количество вещества М, поглощаемого в единицу времени при абсорбции или выделяемого при десорбции, прямо пропорционально поверхности контакта газовой и жидкой фаз F, движущей силе процесса и коэффициенту пропорциональности К, зависящему от гидродинамического режима процесса и физико-химических свойств системы.
Уравнение массопередачи при абсорбции можно записать в виде
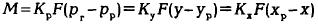
или
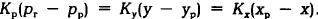
Коэффициент К называется коэффициентом массопередачи при абсорбции и характеризует массу вещества, переданную в единицу времени через единицу поверхности контакта фаз при движущей силе, равной единице.
Единица измерения величины К зависит от единиц измерения составляющих, входящих в уравнение (1). Так, например, если измерять массу поглощенного компонента в кг/ч, поверхность контакта фаз в м , а движущую силу процесса абсорбции в МПа, то из уравнения ( 1) получим единицу измерения К в 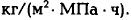
Материальный баланс абсорбера.
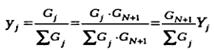
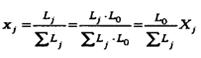
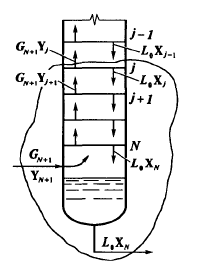 взаимосвязь обычных концентраций с приведенными:
взаимосвязь обычных концентраций с приведенными:
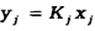 Если потоки газа и жидкости мало меняются по высоте аппарата, т.е.
Если потоки газа и жидкости мало меняются по высоте аппарата, т.е. 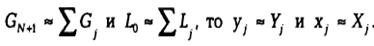
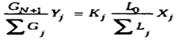 уравнение равновесия:
уравнение равновесия:
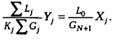 заменим концентрации на приведенные
заменим концентрации на приведенные
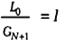
|
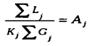
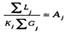 поменяем члены местами
поменяем члены местами 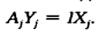 учитывая, что
учитывая, что
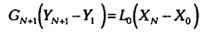 уравнение равновесия запишется
уравнение равновесия запишется
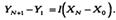 запишем баланс для выбранного сечения
запишем баланс для выбранного сечения
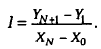 затем
затем
отсюда удельный расход абсорбента
Тепловой баланс абсорбера.
Поглощение комп-ов газовой смеси при абсорбции сопровождается выделением тепла, величина к-го пропорциональна массе и теплоте растворения qA поглощаемых комп-ов, к-ая в первом приближении может быть принята равной теплоте конденсации соответствующего комп-та. Если считать, что все выделившееся при абсорбции тепло пошло на увеличение темп-ры абсорбента, т.е. не учитывать некоторое повышение температуры газа и тепловые потери в окр. среду, то такое допущение дает некоторый запас в расчетах. Общее количество тепла, выделяющееся при абсорбции, равно
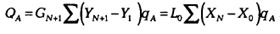
Выделяющееся в процессе абсорбции тепло QAповышает температуру абсорбента, что приводит к ухудшению поглощения компонентов газовой смеси.
Если выделенное при абсорбции тепло не отводить, то темп-ра абсорбента на выходе из аппарата без учета нагревания газа и теплопотерь в окр. среду будет равна 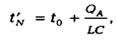
где С — средняя теплоемкость абсорбента в интервале температур от ( t0 до
tN’; L — средний расход абсорбента в абсорбере.
Средняя температура в абсорбере 
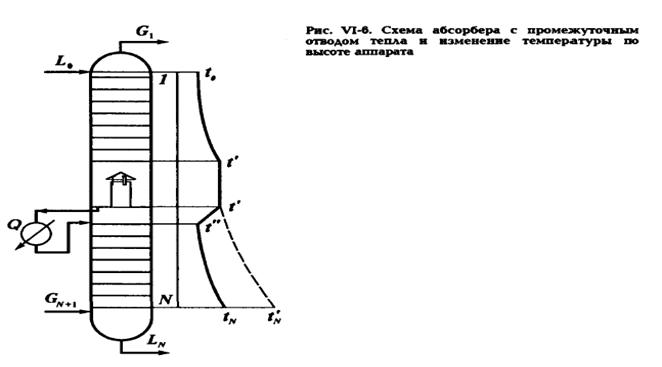
При абсорбции жирных газов, когда поглощается значительная масса газа, тепло, выделенное при абсорбции, окажется большим и приведет к недопустимому повышению темп-ры, что потребует увеличения расхода абсорбента или числа тарелок в абсорбере. Чтобы избежать этого, в одном-двух сечениях аппарата проводят промежуточный отвод тепла Q, обеспечивая тем самым на выходе из абсорбера необходимую температуру tN. При промежуточном отводе тепла темп-ра абсорбента на выходе из абсорбера будет равна 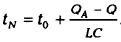
Применение промежуточного охлаждения обеспечивает более равномерное распределение температур по высоте аппарата и более благоприятные условия протекания процесса абсорбции
. 
Абсорбция тощих газов.
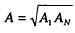 В случае абсорбции так называемых "сухих" газов кол-во извлекаемых комп-ов невелико, что позволяет в расчетах пользоваться усредненным абсорбционным фактором А, к-ый рассчитывают как среднее геометрическое между абсорбционными факторами для низа и верха абсорбера:
В случае абсорбции так называемых "сухих" газов кол-во извлекаемых комп-ов невелико, что позволяет в расчетах пользоваться усредненным абсорбционным фактором А, к-ый рассчитывают как среднее геометрическое между абсорбционными факторами для низа и верха абсорбера:

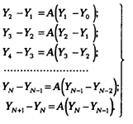 В этом случае уравнение
В этом случае уравнение  запишется в виде
запишется в виде
Варьируя номером тарелки j от 1 до N, получим с-му равенств:
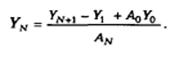 После соответствующих подстановок и преобразований получим выражение изменение концентрации на нижней тарелке.
После соответствующих подстановок и преобразований получим выражение изменение концентрации на нижней тарелке.

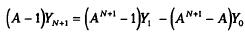 Исключим YN из этого уравнения, использовав уравнение
Исключим YN из этого уравнения, использовав уравнение
 Получим
Получим
 Это уравнение можно привести к виду уравнения
Это уравнение можно привести к виду уравнения
 если в левой части последнего прибавить и отнять
если в левой части последнего прибавить и отнять
После преобразований получим уравнение Кремсера.
При заданных эффективности извлечения е и абсорбционном факторе А из этого уравнения можно определить N — число теоретических тарелок в абсорбере.
При идеальном отделении абсорбента от извлеченных компонентов, когда Y0=0. получим уравнение для расчета коэффициента извлечения через фактор абсорбции.
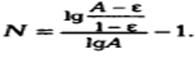 Из этого уравнения может быть получено следующее уравнение для расчета числа теоретических тарелок в абсорбере:
Из этого уравнения может быть получено следующее уравнение для расчета числа теоретических тарелок в абсорбере:
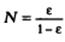 Для компонента, у которого абсорбционный фактор А = 1, из последнего уравнения после раскрытия неопределенности получим
Для компонента, у которого абсорбционный фактор А = 1, из последнего уравнения после раскрытия неопределенности получим
Зависимость между эффективностью абсорбции, абсорбционным фактором и числом теоретических тарелок, определяемая уравнением Кремсера, представлена графически на рис. Этот же график может быть использован и для расчета процесса десорбции.
 |
