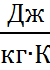Уравнение состояния идеального газа.
Уравнение состояния идеального газа, полученное Клапейроном, имеет вид Р∙v = RT, где Р— абсолютное давление газа, Па; v— удельный объем, м3/кг; R— газовая постоянная, отнесенная к массе газа, равной 1 кг, и имеющая для каждого газа свое значение Дж/(кг∙К).; Т — термодинамическая температура, К. Уравнение явл. ур-ием состояния для 1 кг газа. Умножая обе части на Gи учитывая, что Gv = V, получим уравнение состояния для любого количества газа: РV = GRT., а если в уравнении Vзаменить объемом, занимаемым 1 кмолем (VМ), G— молекулярной массой µ, то получим уравнение состояния для 1 кмоля газа: РVM =µRT. Из этого уравнения определяется универсальная газовая постоянная, отнесенная к 1 кмолю (килограмм-моль) газа: µR = РVM/T.
Из физики известно, что при температуре Т=273,16 К и при давлении Р= 101,325 кПа (760 мм рт. ст.), т. е. при нормальных физических условиях, объем 1 кмоля любого идеального газа равен 22,4146 м3 (закон Авогадро). Подставляя числовые значения объема, давления, температуры в уравнение µR = РVM/T, получаем универсальную газовую постоянную: µR =8314,9 Дж/(кмоль∙К). Газовая постоянная, отнесенная к 1 кг любого газа, будет равна R = 8314,9/µ [ Дж/(кгК)].
Физич. смысл газовой постоянной. Рассмотрим числитель левой части уравн. Р∙v/Т=R: Рv =Н∙м3/(м2∙кг)= (Н∙м)/кг = Дж/кг. Как видно из равенства, произведение давления на удельный объем Рvможно рассматривать как удельную механическую работу, измеряемую в джоулях, полученную в результате расширения 1 кг газа. Если же газ произвел эту работу при нагревании его на один кельвин, то удельная газовая постоянная будет измеряться в джоулях на килограмм-кельвин Дж/(кг∙К). Следовательно, удельная газовая постоянная R есть удельная работа расширения 1 кг газа при нагревании его на 1 кельвин.
Известно, что плотность ρ является обратной величиной удельного объема ρ = 1/v, поэтому удельная газовая постоянная, выраженная через плотность, имеет вид R= Р/(ρТ).
 3.Внутренняя энергия идеального газа.
3.Внутренняя энергия идеального газа.
Непрерывное изменение состояния рабочего тела в результате взаимодействия его с окружающей средой называется термодинамическим процессом. Различают равновесные и неравновесные термодинамические процессы.
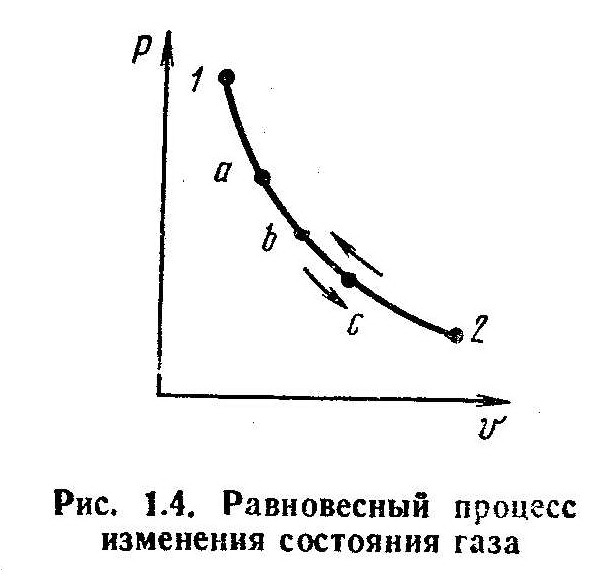
На рис. изображен некоторый равновесный процесс изменения состояния газа. Равновесный процесс, проходящий в направлении от состояния 1 к состоянию 2 через промежуточные точки а, Ь, с и т.д. и связанный с расширением рабочего тела, называется прямым процессом.Равновесный процесс, проходящий в направлении от состояния 2к состоянию 1 через те же точки, что и в прямом процессе, но связанный со сжатием рабочего тела, — обратным процессом.
Процессы, протекающие в прямом и обратном направлениях через одни и те же промежуточные точки, называются обратимыми.
Внутр. Энергия газа –сумма кинетических энергий поступательного, вращательного, внутрималекулярных колебаний атомов и энергии межмалек. Взаимодействий. Последняя составляющая = 0. Каждая сост-ая явл. функцией энергии.
Внутр. Энергия газа явл. парам-м состояния газа и не зависит от хода (пути) термодинамич. процесса.
U=f(T), где U- внутр. энергия 1кг массы газа.
Изменение внутренней энергии рабочего тела не зависит от его промежуточных состояний и определяется полностью величиной его начальных и конечных параметров:
ΔU=U2-U1, где U1— значение внутренней энергии в начальном состоянии, Дж/кг; U2— значение внутренней энергии в конечном состоянии, Дж/кг.
Во всех термодинамических процессах, если v= const, т. е. рабочее тело не расширяется и не совершает работы, сообщаемая ему теплота q = Сv(T2—T1) идет только на увеличение его внутренней энергии, т. е. U2-U1= Сv(T2—T1), Сv- теплоемкость Дж/кгК.
Работа идеального газа.
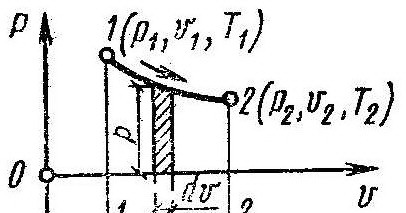 На рис. в системе координат р—v. представлен процесс 1-2. Выделим участок процесса, в котором происходит бесконечно малое изменение dvудельного объема рабочего тела (газа). Давление на этом уча стке равно текущей ординате р.
На рис. в системе координат р—v. представлен процесс 1-2. Выделим участок процесса, в котором происходит бесконечно малое изменение dvудельного объема рабочего тела (газа). Давление на этом уча стке равно текущей ординате р.
Работа расширения l, Дж/кг, рабочего тела в процессе 1-2: dl=P∙dVили V2.l=∫pdv. V1
Работа расширения считается положительной, а работа сжатия отрицательной - это служит признаком того, что работа совершается внешней средой над газом. В отличие от внутренней энергии работа зависит от характера протекания процесса и не является параметром состояния.
Теплоемкость газа
Теплоемкость (ТЕ) – это величина количества тепловой энергии, которая требуется для изменения температуры рабочего тела на 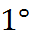 .
.
Удельная теплоемкость – количество тепловой энергии, необходимое для изменения температуры некоторого количества рабочего тела на 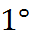 . ТЕ не является хар-кой состояния, она характеризует сам процесс, т.е. является параметром процесса. В зависимости от выбранной единицы количества вещества теплоемкость делится на:
. ТЕ не является хар-кой состояния, она характеризует сам процесс, т.е. является параметром процесса. В зависимости от выбранной единицы количества вещества теплоемкость делится на:
1) Массовую С, 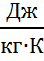 ; 2) Объемную С’,
; 2) Объемную С’, 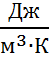 ; 3) Мольную μС,
; 3) Мольную μС, 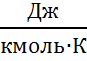
ТЕ может быть истинной и средней.
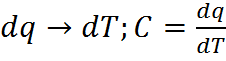 – истинная ТЕ.
– истинная ТЕ.
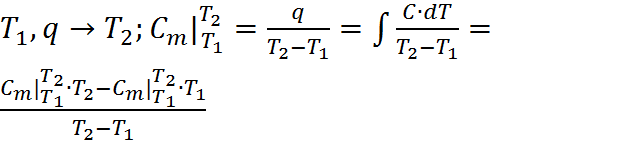 – средняя ТЕ.
– средняя ТЕ.
 В зависимости от вида термодинамического процесса различают ТЕ:
В зависимости от вида термодинамического процесса различают ТЕ:
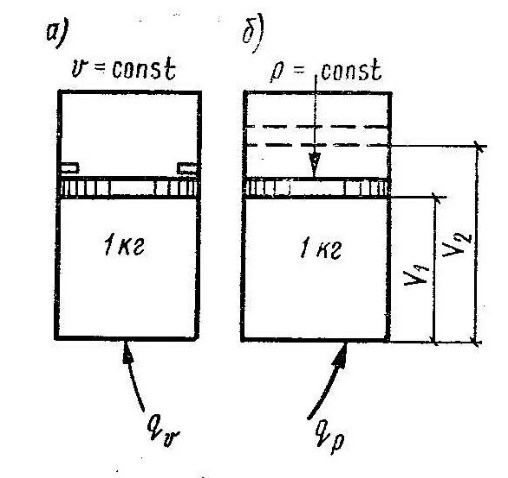
а) Изохорную Сv (V=const)
б) Изобарную Cp (P=const)
Связь между этими ТЕ уст-ся ур-нием Майера:
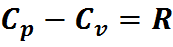
где R – универсальная газовая постоянная, 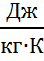
При нагревании 1 кг газа на 1 °С при V=const сообщаемая газу теплота (ТЕ Cv) расходуется только на увеличение внутр. энергии газа, т.к. внешняя работа не совершается. При нагревании 1 кг газа на 1 °С при P=const объем газа возрастает и сообщаемая газу теплота (ТЕ Cр) расходуется не только на увеличение внутренней энергии газа, но и на совершение работы расширения. Поэтому теплоемкость Ср всегда больше, чем теплоемкость Сv на величину работы, совершаемой 1 кг газа при нагревании его на 1 °С при постоянном давлении.
Газовые смеси
Идеальная газовая смесь – механическая смесь отдельных газовых компонентов, между которыми отсутствуют химические реакции. Каждый из компонентов занимает объем смеси, имеет одинаковую с ней 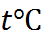 , и оказывает свое парциальное давление.
, и оказывает свое парциальное давление.
Парциальное давление – давление, оказываемое отдельным компонентом смеси на стенки сосуда при определенных 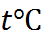 и V (объёме) газовой смеси.
и V (объёме) газовой смеси.
Газовые смеси могут быть заданы массовыми или объемными долями.
А) 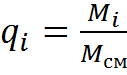 Б)
Б) 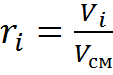
Массовая доля Объемная доля
Для газовых смесей характерен закон Дальтона: 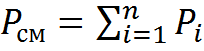
Для воздуха (влажного): 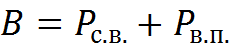
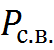 - давление сухого воздуха;
- давление сухого воздуха; 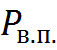 – давление водяных паров.
– давление водяных паров.
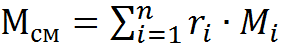 – кажущаяся молекулярная масса;
– кажущаяся молекулярная масса;
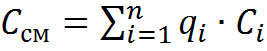 ;
; 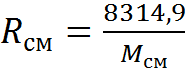 ,
,