Третий закон термодинамики. Тепловая теорема Нернста. Следствия.
Протекание химических реакций связано с изменением состояния атомов в молекулах реагирующих веществ. При этом происходит изменение внутренней энергии, которое может проявляться в виде выделяющейся теплоты реакции и различных работ:
ΔU = Q – L – A,
где Q - теплота реакции; L = V1∫V2 р dV - работа изменения объема (против внешних сил); А - сумма работ против электрических, световых, магнитных, звуковых и других сил, проявляющихся в ходе химической реакции и сопутствующих воздействий.
Уравнение первого закона термодинамики, выраженное через энтальпию, можно представить в виде
ΔI = Q + p1∫p2Vdp – A
Рассмотрим процессы, когда фиксированными являются два параметра: (v, Т) = const или (р, Т) = const.
Для процесса при (v, Т) = const уравнение запишется в виде
ΔUv,T = Qv,T – Av,T или Av,T = Qv,T – ΔUv,T (*)
Для процесса при (р, Т) = const уравнение будет иметь вид
ΔIp,T = Qp,T – Ap,T или Ap,T = Qp,T – ΔIp,T (**)
В приведенных уравнениях изменения внутренней энергии и энтальпии происходят за счёт отвода теплоты реакции и совершения работы против внешних сил.
Выражая теплоту через изменение энтропии в виде Q = T(S2 – S1) и учитывая, что
F = U – TS, – изохорно-изотермический потенциал или свободная энергия Гельмгольца (мера работоспособности системы)
G = I – TS, – изобарно-изотермический потенциал или свободная энергия Гиббса (определяет наличие обратимых и/или необратимых процессов в системе) уравнения (*) и (**) перепишутся в виде:
Av,T = (F1 – F2)v,T Ap,T = (G1 – G2)p,T
Дифференцируя F = U – TS, получаем
dF = dU – TdS – SdT.
Учитывая, что в обратимых процессах
TdS = dU + pdV или dU – TdS = – pdV,
 получаем dF = –SdT – pdV.
получаем dF = –SdT – pdV.
Продифференцируем это уравнение по Т при V = const.

Уравнение превращается в частную производную и принимает вид:
 , откуда
, откуда 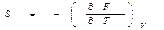
Следовательно:

При переходе термодинамической системы из одного состояния в другое в обратимом химическом процессе при (v, Т) = const совершается максимальная работа
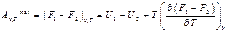 При записи теплового эффекта (максимальной выделяемой или поглощаемой теплоты) химической реакции в виде QV = (U2 – U1)v,T , получаем
При записи теплового эффекта (максимальной выделяемой или поглощаемой теплоты) химической реакции в виде QV = (U2 – U1)v,T , получаем

Аналогично, если рассмотреть химическую реакцию в условиях термодинамической обратимости, протекающую в изобарно-изотермической термодинамической системе при (р, Т) = const, получим


Уравнения для  и
и 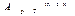 называются уравнениями максимальной работы Гиббса-Гельмгольца, в которых часто индекс «mах» не пишут, т.к. знак равенства уже означает термодинамическую обратимость и, следовательно, – максимальную работу реакции.
называются уравнениями максимальной работы Гиббса-Гельмгольца, в которых часто индекс «mах» не пишут, т.к. знак равенства уже означает термодинамическую обратимость и, следовательно, – максимальную работу реакции.
В экспериментах было обнаружено, что чем ниже температура, тем меньше разность ( 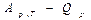 ).
).
Однако равенство  соблюдается не только при температуре, равной нулю, но и вблизи нуля температур по шкале Кельвина, т.е.
соблюдается не только при температуре, равной нулю, но и вблизи нуля температур по шкале Кельвина, т.е.
 Этот постулат получил название тепловой теоремы Нернста.
Этот постулат получил название тепловой теоремы Нернста.
По правилу Лопиталя (предел отношения функций равен пределу отношения их производных):

Раскрытие неопределённости типа 0/0 даёт:
 Ранее было установлено
Ранее было установлено
Ap,T = (G1–G2)p,T
Записав дополнительно


следует, что изменение энтропии вблизи нуля температурной шкалы Кельвина также равно нулю, т.е.  (постулат Планка или третий закон термодинамики), т.е. энтропия перестаёт быть функцией состояния.
(постулат Планка или третий закон термодинамики), т.е. энтропия перестаёт быть функцией состояния.
Фактически Планк предположил, что при температуре Т = 0 К не только алгебраическая сумма энтропии твердых тел, но и энтропия каждого тела в отдельности также равняется нулю 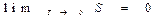 .
.
Формулировка третьего закона термодинамики по Планку:
в любом изотермическом процессе, который происходит при температуре, близкой к абсолютному нулю, изменение энтропии системы равно нулю.
Из положения теоремы Нернста о том, что энтропия системы вблизи Т = 0 К не изменяется, следует, что в этой области не происходит теплообмена системы с окружающей средой (изотермический процесс является также и адиабатным).
Таким образом, система, еще не достигнув температуры Т = 0 К, приходит в такое состояние, что достижение абсолютного нуля практически становится невозможным (как путем адиабатного расширения, так и путем изотермического процесса).
Нернст сделал вывод, являющийся формулировкой третьего закона термодинамики: никаким конечным процессом нельзя охладить тело до абсолютного нуля, или абсолютный нуль температур недостижим.
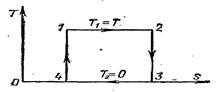
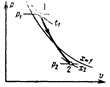
Рассмотрим цикл Карно с температурой теплоотдатчика Т1=Т и температурой теплоприемника Т2 = 0.
По второму закону термодинамики, для кругового процесса §dQ/T = 0 или Δs12 + Δs23 + Δs34 + Δs41 = 0, где Δs12 = Q/T, Δs23 = 0 (адиабатный процесс); Δs34 = 0 (по постулату Планка), Δs41 = 0 (адиабатный процесс).
Следовательно, в результате проведения такого цикла, который дает возможность получать непрерывную работу за счет охлаждения одного теплоотдатчика, можно создать вечный двигатель второго рода, что, согласно второму закону термодинамики, невозможно.
Или: невозможно создать машину, которая в качестве низшего источника теплоты имела бы тело с Т = 0 К, или вечный двигатель третьего рода неосуществим.
Поскольку 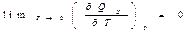 , то
, то 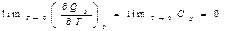
т.е. теплоемкость не изменяется вблизи абсолютного нуля и стремится к нулю.
А т.к. теплоёмкость равна нулю, то и изменения внутренней энергии вблизи абсолютного нуля не происходит, а соответственно аналитическому выражению первого закона термодинамики, и работа не совершается.
12. Водяной пар. Основные понятия и определения.
Газообразные тела (с примесью одноименной жидкости в виде взвешенных мелкодисперсных частиц или без нее) принято называть парами.
Все пары являются реальными газами и подчиняются всем присущим этим газам закономерностям, в частности закономерностям фазовых переходов.
Образование пара из одноименной жидкости происходит посредством ее испарения или кипения. Между этими двумя процессами существует принципиальное различие.
Испарение жидкости может происходить лишь с открытой поверхности и при любой температуре.
С повышением температуры жидкости процесс испарения ускоряется, т.к. средняя скорость движения молекул возрастает.
Кипение жидкости может происходить и при отсутствии открытой поверхности. Сущность его состоит в том, что образование пара происходит в основном в объеме самой жидкости.
В сосуде одновременно происходят противоположные процессы испарения жидкости и конденсации пара.
 Пока концентрация молекул пара в паровоздушной смеси мала, первый процесс превалирует над вторым. Вместе с этим увеличивается и парциальное давление пара Рп в паровоздушной смеси; парциальное же давление воздуха Рв уменьшается, ибо избыток его удаляется в окружающую среду через обратный клапан, но суммарное давление паровоздушной смеси остается неизменным.
Пока концентрация молекул пара в паровоздушной смеси мала, первый процесс превалирует над вторым. Вместе с этим увеличивается и парциальное давление пара Рп в паровоздушной смеси; парциальное же давление воздуха Рв уменьшается, ибо избыток его удаляется в окружающую среду через обратный клапан, но суммарное давление паровоздушной смеси остается неизменным.
С повышением парциального давления пара скорость испарения жидкости уменьшается, а скорость обратной конденсации пара возрастает и в конечном итоге наступает момент, когда скорости обоих процессов становятся одинаковыми, а Рп устанавливается одинаковым.
Пар какого-либо вещества, находящийся в динамическом равновесии с одноименной жидкостью, называется насыщенным.
Температура и давление насыщенного пара взаимосвязаны и каждой температуре соответствует вполне определенное давление насыщения.
По мере роста температуры паровоздушной смеси содержание воздуха в ней уменьшается за счет вытеснения его паром через обратный клапан. Поэтому наступает момент, когда из сосуда удаляются последние остатки воздуха и в верхней его части остается один лишь насыщенный пар.
Этот момент отмечается тем, что давление насыщенного пара становится равным давлению окружающей среды, под которым все время находилась жидкость, а потому становится возможным кипение жидкости.
Температура, при которой давление насыщения становится равным внешнему давлению на жидкость, называется температурой кипения; она является функцией внешнего давления и с увеличением его возрастает.
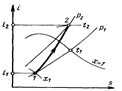
 После начала кипения в рассматриваемом сосуде продолжение подвода тепла сопровождается дальнейшим парообразованием, причем давление в нём сохраняется неизменным, т.к. излишки пара вытесняются через обратный клапан. Неизменной остается и температура, как пара, так и самой жидкости. Такой процесс продолжается до полного выкипания жидкости, и, наступает момент, когда весь сосуд оказывается заполненным лишь насыщенным паром, температура которого еще равна температуре кипения.
После начала кипения в рассматриваемом сосуде продолжение подвода тепла сопровождается дальнейшим парообразованием, причем давление в нём сохраняется неизменным, т.к. излишки пара вытесняются через обратный клапан. Неизменной остается и температура, как пара, так и самой жидкости. Такой процесс продолжается до полного выкипания жидкости, и, наступает момент, когда весь сосуд оказывается заполненным лишь насыщенным паром, температура которого еще равна температуре кипения.
Пар какого-либо вещества, не содержащий в себе одноименной жидкости и имеющий температуру кипения при данном давлении, называется сухим насыщенным.
Пар какого-либо вещества, температура, которого превышает температуру кипения при данном давлении, называется перегретым.
Состояние перегретого пара определяется значениями двух независимых параметров, в качестве которых наиболее часто используются давление и температура.
С повышением перегрева пар по своим свойствам приближается к идеальному газу.
При изобарном отводе теплоты от сухого насыщенного пара температура его не изменяется, а вместо этого начинается конденсация пара, и по всему его объему образуются мельчайшие капельки жидкости.
Насыщенный пар какого-либо вещества, содержащий в себе одноименную жидкость в виде взвешенных мелкодисперсных частиц, называется влажным насыщенным паром.
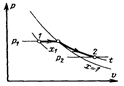
Представив себе влажный пар как механическую смесь сухого насыщенного пара и равномерно распределенной в нем жидкости, можно определить степень сухости х влажного пара как массовую долю содержащегося в нем сухого насыщенного пара.
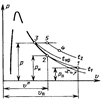 Очевидно, величина х может изменяться от единицы (что соответствует сухому насыщенному пару) до нуля (что соответствует кипящей воде).
Очевидно, величина х может изменяться от единицы (что соответствует сухому насыщенному пару) до нуля (что соответствует кипящей воде).
Таким образом, состояние влажного пара определяется значениями двух независимых параметров, – давления (или температуры) и степени сухости.
Влажный пар и его параметры
Объем влажного пара можно представить как сумму объемов двух компонентов.
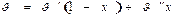
где х – степень сухости пара.
Первое слагаемое представляет собой объем жидкости, содержащейся в 1 кг влажного пара, а второе – объем содержащегося в нем сухого насыщенного пара.
Для превращения 1 кг кипящей воды в сухой насыщенный пар при постоянном давленииему необходимо сообщить количество теплоты, называемое теплотой парообразования:
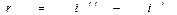

 Часть теплоты парообразования расходуется на увеличение внутренней энергии, связанное с совершением работы против сил взаимного притяжения молекул (внутренняя теплота парообразования). Остальная часть теплоты парообразования расходуется на работу расширения, не связанную с наличием сил молекулярного взаимодействия (внешняя теплота парообразования).
Часть теплоты парообразования расходуется на увеличение внутренней энергии, связанное с совершением работы против сил взаимного притяжения молекул (внутренняя теплота парообразования). Остальная часть теплоты парообразования расходуется на работу расширения, не связанную с наличием сил молекулярного взаимодействия (внешняя теплота парообразования).
С помощью теплоты парообразования r энтальпия влажного пара определяется следующим образом.
В процессе парообразования при Р=const
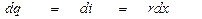
где х – степень сухости влажного пара.
Интегрируя, получаем:
ix 
Энтропия влажного пара:
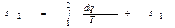
а для данного случая
sx 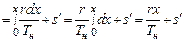 (*)
(*)
где Тн – температура кипения при заданном постоянном давлении.
Для сухого насыщенного пара х=1, поэтому
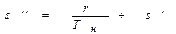
откуда получаем

Формула (*) может быть записана так:
sx  .
.
