Кафедра фармацевтической химии
Кафедра фармацевтической химии
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
К ПРОИЗВОДСТВЕННОЙ ПРАКТИКЕ
по фармацевтическому анализу
для студентов 5 курса фармацевтического факультета
Томск 2013
Блинникова А.А. Методические рекомендациик производственной практике, зачёту по фармацевтическому анализу. – Томск: СибГМУ, 2010. – 28 с.
Методические рекомендации к производственной практике, зачёту по фармацевтическому анализу подготовлены в соответствии с учебной программой дисциплины и квалификационной характеристикой специалиста.
Утверждено решением методической комиссии фармацевтического факультета Сибирского государственного медицинского университета (протокол № __ от «__» _______2010 г.).
©А.А. Блинникова
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ К ПРОВЕДЕНИЮ ПРОИЗВОДСТВЕННОЙ ПРАКТИКИ, ЗАЧЁТА ПО ФАРМАНАЛИЗУ
Цели практики: закрепление полученных в учебном процессе теоретических знаний, практических навыков и умений для решения конкретных задач практической деятельности провизора-аналитика в условиях аптек, контрольно-аналитических лабораторий, аптечных складов и лабораторий НИИ.
Производственная практика по фармацевтическому анализу( контролю качества лекарственных средств) базируется на знаниях и умениях, полученных при изучении дисциплины «Фармацевтическая химия» в течение 5-9 семестров.
До начала производственной практики студент должен знать:
- законы и законодательные акты о здравоохранении, стандартизации и контроле качества лекарственных средств, порядке их хранения, охране окружающей среды, санитарном режиме и технике безопасности, об административной и уголовной ответственности за их нарушение;
- принципы фармацевтической этики и деонтологии;
- систему государственного контроля качества лекарственных средств;
- контрольно-разрешительную систему обеспечения качества лекарственных средств, организацию контроля качества лекарственных средств в испытательных лабораториях и в аптеках;
- общие методы анализа согласно действующему изданию Государственной фармакопеи: физические, химические и физико-химические;
- статистическую обработку результатов химического эксперимента и результатов микробиологических испытаний;
- контроль качества лекарственных средств мелкосерийного производства, виды и методы внутриаптечного контроля;
- экологический контроль фармацевтических производств (вода, почва, воздух) и фармацевтических препаратов;
- развитие исследований по созданию новых и совершенствованию действующих методов оценки качества лекарственных средств, относительность требований и методов оценки качества, их комплексность и взаимосвязь, оценка пригодности (валидация) методов и способов оценки качества.
После прохождения производственной практики студент должен
знать:
- общие методы оценки качества ЛС, возможность использования каждого метода в зависимости от способа получения ЛС, исходного сырья, структуры ЛВ, физико-химических процессов, которые могут происходить во время хранения и обращения ЛС;
- факторы, влияющие на качество ЛС на всех этапах обращения. Определение главных факторов в зависимости от свойств ЛВ (окислительно-восстановительных, способности к гидролизу, полимеризации и.т.д.). Возможность предотвращения влияния внешних факторов на доброкачественность ЛС;
- химические методы, положенные в основу качественного анализа ЛС. Основные структурные фрагменты ЛВ, по которым проводится идентификация неорганических и органических ЛВ. Общие и специфические реакции на отдельные катионы, анионы и функциональные группы;
- химические методы, положенные в основу количественного анализа ЛС. Уравнения химических реакций, проходящих при кислотно-основном, окислительно-восстановительном, осадительном, комплексонометрическом титровании;
- принципы, положенные в основу физико-химических методов анализа ЛС;
- оборудование и реактивы для проведения химического анализа ЛС. Требования к реактивам для проведения испытаний на чистоту, подлинность и количественного определения;
- оборудование и реактивы для проведения физико-химического анализа ЛВ. Принципиальную схему рефрактометра, фотоколориметра, спектрофотометра, ГЖХ, ВЭЖХ;
- структуру НД, регламентирующей качество ЛС. Особенности структуры ФС и ФСП;
- способы определения физико-химических констант ЛВ: температуры плавления, угла вращения, удельного показателя поглощения, температуры кипения;
- понятие валидации. Валидационные характеристики методик качественного и количественного анализа.
Уметь:
- пользоваться нормативной документацией и проводить фармакопейный анализ лекарственных средств;
- взвешивать на аптечных и аналитических весах;
- измерять объемы жидкости с помощью мерных цилиндров, бюреток, пипеток;
- выпаривать жидкости на водяной и песчаной бане;
- титровать с помощью пипетки и бюретки;
- измерять показатель преломления с помощью рефрактометра;
- измерять величину светопоглощения с помощью фотоколориметра и спектрофотометра;
- измерять угол вращения с помощью поляриметра;
- наносить пробы на хроматографическую пластинку или бумагу, готовить подвижную фазу, проводить хроматографирование и проявление;
- рассчитывать содержание вещества по результатам титриметрического или физико-химического анализа;
- выбирать реакции для проведения качественного анализа лекарственных веществ в соответствии с наличием в них определенных структурных фрагментов;
- интерпретировать результаты анализа лекарственных средств для оценки их качества.
Владеть:
- навыками оценки качества лекарственных средств по критерию «описание»;
- методами определения общих показателей качества фармацевтических субстанций: растворимость, температура плавления, плотность, кислотность и щелочность, прозрачность, цветность, зола, потеря в массе при высушивании;
- методиками проведения реакций для установления подлинности лекарственных средств по их структурным фрагментам;
- навыками интерпретации результатов УФ- и ИК-спектрометрии, хроматограмм ВЭЖХ и ГЖХ анализа для подтверждения идентичности лекарственных средств;
- методикой проведения тонкослойной и бумажной хроматографии лекарственных средств и интерпретации ее результатов;
- навыками проведения испытаний на чистоту лекарственных средств и установления пределов содержания примесей химическими и физическими методами;
- навыками приготовления реактивов, эталонных, титрованных и исследуемых растворов.
- навыками проведения количественного определения лекарственных средств в субстанции и лекарственных препаратах титриметрическими методами;
- навыками проведения количественного определения лекарственных средств в субстанции и лекарственных препаратах физико-химическими методами;
- навыками выполнения анализа и контроля качества лекарственных средств аптечного изготовления;
- навыками проведения следующих видов контроля качества продукции аптечного производства: опросного, письменного, органолептического, физического, химического;
- навыками заполнения документации по контролю качества лекарственных средств.
Задачипроизводственной практикипо контролю качества лекарственных средств:
-изучение обязанностей провизора-аналитика на рабочем месте;
-ознакомление с организацией и технической оснащенностью рабочего места провизора-аналитика;
-проведение контроля качества лекарственных средств под руководством провизора-аналитика и оформление соответствующей документации.
СОДЕРЖАНИЕ ПРАКТИКИ
Общие требования к содержанию практики.
Общая трудоемкость производственной практики составляет: 252 часа
Теоретическое обучение: 29 часов;
Производственная практика: – 223 часа.
Таблица 1
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
Во время производственной практики знания студентов контролируются при периодической проверке дневника руководителем от кафедры, при сдаче зачёта на рабочем месте и зачёта по фармацевтическому анализу на кафедре.
ОСНОВНЫЕ ЭТАПЫ АТТЕСТАЦИИ СТУДЕНТОВ
Аттестация студентов 5 курса по производственной практике по фармацевтическому анализу предусматривает следующие этапы:
1.1. Выполнение студентом графика прохождения производственной практики
Во время работы в аптеке студент обязан безоговорочно выполнять правила внутреннего трудового распорядка данного учреждения и все указания руководителя практики. Время работы студента в аптеке и вид выполняемой работы фиксируется в отдельном табеле (Приложение 3), который представляется в дневнике. Табель должен быть заверен подписью руководителя практики и печатью учреждения.
Рабочий день студента устанавливается в соответствии с рабочим днем руководителя производственной практики от учреждения.
Пропущенные по любой причине рабочие дни должны быть отработаны в соответствии с распорядком, принятым в учреждении, в противном случае студент не допускается к сдаче зачёта.
Студенту целесообразно распределять свое рабочее время в соответствии с приведенным планом-графиком (табл.1,2), однако последовательность отдельных видов работ может меняться в связи с производственной необходимостью аптеки или другого учреждения.
1.2. Оформление студентом дневника и отчёта по производственной практике
В период прохождения производственной практики по фармацевтическому анализу студент должен закрепить практические навыки, указанные в Приложении 1. Освоение того или иного практического навыка, выполнение анализов, другая выполняемая работа фиксируется студентом в дневнике.
Дневник начинают с титульного листа (Приложение 2), далее ежедневно по форме заполняется табель рабочего времени студента-практиканта
(Приложение 3). Затем идет описание лаборатории или контрольно-аналитического кабинета, стола с приложением плана, указания рабочих мест, оснащения, литературы. Желательно приложить план-схему помещений и паспорт аптеки (Приложение 6) или другого учреждения прохождения практики.
Студент ежедневно ведет дневник, в котором фиксирует выполненную работу. Дневник является основным документом, отражающим характер и качество производственной практики. В дневнике должна быть отмечена вся работа, проводимая студентами во время прохождения производственной практики. Необходимо отражать наиболее сложные вопросы и анализы, избегая дублирования, при этом должны быть применены доступные на месте прохождения практики методы физико-химического и химического анализа.
Для оформления дневника студенту-практиканту ежедневно отводится 1 час рабочего времени.
Объем дневника не регламентируется, вместе с тем он должен отражать информацию по вопросам, предусмотренным программой. Дневник должен быть оформлен на листах формата А4 (210х297 мм) в рукописном варианте со стандартными полями (левое – 3 см, правое – 1-1,5 см, верхнее – 2 см, нижнее – 2,5 см).
При анализе фармацевтических препаратов основываются на требовании ГФ или заменяющих ее документов - ФСП, ФС и др. и оформляют результаты анализов в виде протоколов (Приложение 4).
Помимо анализов, проведенных в лаборатории, необходимо описать те анализы, которые выполнены в аптеке при ее посещении. Кроме того, следует приложить акт обследования аптеки и заполненную форму на препараты, анализируемые в аптеке экспресс-методом.
Дневник ежедневно контролируется и подписывается руководителем производственной практики от аптечного учреждения, а по окончании практики заверяется печатью и подписью руководителя аптечного учреждения.
Материалы к составлению отчетасобираются постепенно с первого дня практики. Отчет о прохождении производственной практики по фармацевтическому анализу (титульный лист см.Приложение 5) оформляется в произвольной форме в рукописном виде и подписывается студентом, при этом он показывает способность критического анализа работы учреждения и достаточную квалификацию по контролю качества лекарственных средств
При написании отчета необходимо отметить следующие моменты:
1. Титульный лист (см. приложение 5);
2. причина изменения срока практики (в случае болезни к отчету прилагается врачебная справка);
3. общая характеристика условий и обстановки, в которой осуществлялась работа студента. Необходимо дать характеристику рабочего места студента, его оборудование, инвентарь и принадлежности, применяемые в работе и др.;
4. организация контроля качества лекарств в аптеках;
5. порядок прохождения практики, ее содержание, выполнение программы;
6. указать противоречия между теорией и практикой, выявляющиеся во время практики, их причины, значение; собственная точка зрения студента на возможность устранения их;
7. указать недостатки производственного процесса, их причины, значение и возможность устранения;
8. указать, что нового внес студент в практическую работу контрольно-аналитической лаборатории или аптеки. Какие вопросы интересуют или вызывают затруднения у работников контрольно-аналитической службы – практические, теоретические (указать конкретно);
9. производственная экскурсия и ее содержание, если была;
10. рационализаторские мероприятия, их сущность, целесообразность, эффект;
11. общественная жизнь коллектива и участие в ней практиканта;
12. оклады и сообщения, сделанные студентами во время практики (копии приложить), участие в рационализаторской работе и работе научно-фармацевтического общества;
13. оценка практики, положительные и отрицательные стороны и предложения по улучшению.
1.3. Зачёт на рабочем месте
На последней неделе прохождения производственной практики студент сдаёт зачёт на рабочем месте.
Для этого он получает индивидуальное задание по анализу конкретного лекарственного средства и, выполняя его, показывает способность определять подлинность, чистоту и количественное содержание анализируемого ЛС, используя закреплённые практические навыки.
1.4. Зачёт по фармацевтическому анализу
В соответствии с учебным планом в 10 семестре обучения после окончания производственной практики студент сдаёт зачёт по фармацевтическому анализу. Для подготовки к зачёту студенту заранее даётся перечень вопросов и его знакомят с формой проведения зачёта.
После окончания производственной практики по фармацевтическому анализу документы должны поступить на кафедру в течение 7 дней, иногородние студенты сдают их по приезду в г.Томск. Для этого студент должен сдать куратору кафедры оформленные дневник, отчёт, протокол сдачи зачёта на рабочем месте, характеристику для проверки.
2. ПРИЁМ ЗАЧЁТА НА РАБОЧЕМ МЕСТЕ
К сдаче зачёта на рабочем месте допускаются студенты, посетившие и отработавшие все дни согласно графика прохождения производственной практики по фарманализу.
По завершении производственной практики студенты должны овладеть практическими навыками, указанными в Приложении 1, которые они демонстрируют при выполнении выданного задания.
Результаты анализа предложенного лекарственного средства студент оформляет в виде протокола (Приложение 4), который подписывает руководитель производственной практики от учреждения, выставляя при этом соответствующую оценку по пятибальной системе.
3. ПРИЁМ ЗАЧЁТА ПО ФАРМАНАЛИЗУ
К итоговому зачёту по производственной практике допускаются студенты, сдавшие на кафедру дневник, отчёт, протокол сдачи зачёта на рабочем месте, характеристику. После проверки куратором указанных документов, студенту назначается время сдачи зачёта.
Зачет проводится в форме собеседования по вопросам, касающимся оформления дневника, отчёта по производственной практике и вопросам, указанным в Приложении 7. Студент получает три вопроса из разных разделов этого приложения и в зависимости от предложенного задания моделирует анализ лекарственного вещества по соответствующей фармакопейной статье, анализ лекарственной формы, приготовление титрованного раствора и установление его поправочного коэффициента по ГФ.
Оценка знаний на зачёте учитывает оценку зачёта на рабочем месте, оценку за оформление дневника и отчёта, оценку при собеседовании.
Учебно-методическое обеспечение самостоятельной работы студентов на производственной практике
Для самостоятельной работы студентов разрабатываются банки тестовых заданий по каждому виду контроля качества лекарственных средств, а также темы для самостоятельного изучения студентами методов анализа лекарственных средств. Вопросы для контроля прохождения производственной практики должны формулироваться в зависимости от места прохождения практики.
Контрольные вопросы:
1. Роль испытательных лабораторий в системе добровольной сертификации лекарственных средств. Декларирование соответствия лекарственных средств
2. Источники и классификация некачественной и контрафактной продукции
3. Структура, особенности и область применения нормативной документации (ФС, ОФС, ФСП, НД фирмы- изготовителя)
4.Основные критерии качества фармацевтической субстанции. Общие фармакопейные методы анализа.
5.Понятие технологической и специфической примеси, принципы нормирования их содержания.
6.Классификация методов количественного определения лекарственных средств. Обоснования выбора метода. Возможности химических и физико-химических методов анализа.
7.Требования ОФС к таблетированным лекарственным препаратам.
8.Требования ОФС к парентеральным лекарственным препаратам.
9.Требования ОФС к глазным каплям, жидким лекарственным формам (растворы, суспензии, сиропы)
10.Виды контроля лекарственных средств, изготавливаемых в условиях аптек.
11. Организация хранения в аптечных учреждениях различных групп лекарственных средств и изделий медицинского назначения
12.Критерии оценки качества лекарственных средств, изготавливаемых в аптеках.
13.Привести ход анализа фармацевтической субстанции, пояснить используемые методы, написать схемы химических реакций (в соответствии с протоколом анализа, приведенном в дневнике студента)
14. Привести ход анализа лекарственного средства заводского изготовления (таблетки, растворы и т.д.), пояснить используемые методы, написать схемы химических реакций (в соответствии с протоколом анализа, приведенном в дневнике студента)
15. Привести ход анализа, лекарственного средства, изготовленного в аптеке, пояснить используемые методы, написать схемы химических реакций (в соответствии с протоколом анализа, приведенном в дневнике студента,
Учебно-методическое и информационное обеспечение производственной практики
а) основная литература
1. Беликов, В.Г. Фармацевтическая химия. В 2 ч..: Учебн. пособие / В.Г. Беликов – 4-е изд., перераб. и доп. – М.:МЕДпресс-информ, 2007. – 624с.
2. Фармацевтическая химия: Учеб. пособие / Под ред. А.П. Арзамасцева. – 2-е изд., испр. – М.: ГЭОТАР-Медиа, 2005.-640с.
3. Лабораторные работы по фармацевтической химии: Учебное пособие //В.Г. Беликов, Е.Н. Вергейчик, Е.В. Компанцева и др./Под ред. Е.Н. Вергейчика и Е.В. Компанцевой. – 2-е изд., перераб. и доп. - Пятигорск, 2003. – 342с.
4. Государственная фармакопея СССР 11-е изд. Вып. 1 - М. Медицина, 1987. -334 с.
5. Государственная фармакопея СССР 11-е изд. Вып.2-М.: Медицина 1989.- 400 с.
6. Государственная фармакопея РФ 12-е изд.- «Издательство «Научный центр экспертизы средств медицинского применения», 2008. -704 с.
б) дополнительная литература:
1. Кулешова М.И., Гусева Л.Н., Сивицкая О. К. Анализ лекарственных форм, изготовляемых в аптеках. -М.: Медицина, 1989.-270 с.
2. Приказ министерства здравоохранения и социального развития от 30октября 2006 года № 734 «Об утверждении административного регламента федеральной службы по надзору в сфере здравоохранения и социального развития по исполнению государственной функции по организации проведения экспертизы качества, эффективности и безопасности лекарственных средств »
3. Письмо федеральной службы по надзору в сфере здравоохранения и социального развития от 20.12.2006 № 01И-971/06 «О декларировании соответствия лекарственных средств»
4. Методические рекомендации по принятию и регистрации декларации о соответствии лекарственных средств, утверждены приказом Минпромэнерго России от « 26 » декабря 2006 г. № 425
5. Постановление Правительства РФ от 13 августа 1997 г. N 1013 "Об утверждении перечня товаров, подлежащих обязательной сертификации, и перечня работ и услуг, подлежащих обязательной сертификации" (с изменениями от 24 мая 2000 г., 3 января, 29 апреля 2002 г., 10 февраля 2004 г., 28 апреля 2005 г.
6. Письмо федеральной службы по надзору в сфере здравоохранения и социального развития от 31.01.2007 № 01И-90/07 «О подтверждении соответствия лекарственных средств»
7. Стандарт отрасли «правила организации производства и контроля качества лекарственных средств (GMP) ОСТ 42-510-98 (Введен в действие совместным приказом Минздрава РФ и Минэкономики РФ от 3 декабря 1999 г. N 432/512)
8. Приказ МЗ РФ №305 от 16.10.97 "О нормах отклонений, допустимых при изготовлении лекарственных средств и фасовке промышленной продукции в аптеках"
9. Приказ МЗ РФ №214 от 16.07.97. "О контроле качества лекарственных средств, изготовляемых аптеках".
10. Приказ МЗ РФ №376 от 04.07.97 г "Единые правила оформления лекарств, приготовляемых в аптеках". Требования ГФ XI к инъекционным растворам. Технология приготовления лекарственных форм, содержащих стабилизаторы и особенности количественного анализа таких лекарственных форм.
11. Приказ МЗ РФ №308 от 21.10.97 "Об утверждении инструкции по приготовлению в аптеках жидких лекарственных форм".
12. Приказ МЗ РФ №318 "Об утверждении инструкции но организации хранения в аптечных учреждениях различных групп лекарственных средств и изделий медицинского назначения".
13. Приказ МЗ РФ №309 "Об утверждении инструкции но санитарному режиму аптек".
14. Приказ МЗ РФ №328 от 21.10.99 г "О рациональном назначении лекарственных средств, правилах выписывания рецептов на них и порядка их отпуска аптечным учреждениям."
15. Федеральный закон. О лекарственных средствах. (в ред. Федеральных законов от 02.01.2000 №5-ФЗ, от 30.12.2001 №196-ФЗ, от 10.01.2003 №15-ФЗ, от 30.06.2003 №86-ФЗ).
16. ФС. ФСП. НД на лекарственные средства.
Приложение 2
Государственное образовательное учреждение высшего профессионального образования «Сибирский государственный медицинский университет Министерства здравоохранения и социального развития России»
(ГБОУ ВПО СибГМУ Минздравсоцразвития России)
ФАРМАЦЕВТИЧЕСКИЙ ФАКУЛЬТЕТ
ДНЕВНИК
Приложение 3
ТАБЕЛЬ РАБОЧЕГО ВРЕМЕНИ СТУДЕНТА-ПРАКТИКАНТА
| Дата | Начало и окончание рабочего дня | Выполняемая работа | Затраты времени | Подписи | |
| студента | руководителя | ||||
| Пример: 09.02.11 | 9.00-15.00 | 1.Анализ воды дистиллированной 2.Анализ дефектуры 3.Качественный и количественный анализ раствора Рингера 4.Оформление дневника | 1 час 1 час 3 часа 1 час |
Приложение 4
В протоколе указывается:
1. латинское название препарата, его русский перевод и всевозможные синонимы;
2. для органических препаратов необходимо указать структурную формулу и молекулярную массу;
3. описание внешнего вида;
4. отметить растворимость веществ в различных растворителях;
5. описание подлинности необходимо сопроводить уравнениями химических реакций, если это возможно;
6. при описании чистоты препарата необходимо четко излагать условия проведения и полученные при этом результаты, иллюстрируя уравнениями химических реакций, за исключением испытания на содержание общих примесей хлоридов, сульфатов, солей тяжелых металлов;
7. при количественном определении препарата необходимо дать теоретическое обоснование используемого метода, условия проведения анализа, сопровождая уравнениями химических реакций, лежащих в основе описанного метода, расчетом молярной массы эквивалента, титра, расчетной формулой и полученными данными;
8. вывод или заключение.
При анализе готовых лекарственных средств необходимо написать рецепт на латинском языке с указанием входящих в него ингредиентов и их дозировки. Анализ начинают с внешнего осмотра. Проверяют общую массу, объем, среднюю массу, органолептический контроль.
При описании реакций установления подлинности и определения количественного содержания ингредиентов следует руководствоваться вышеописанными требованиями. Кроме того, необходимо провести расчет отклонений от прописи как в общей массе или объеме, так и на каждый ингредиент в отдельности.
В конце анализа следует сделать заключение о том, что данная лекарственная форма приготовлена удовлетворительно или неудовлетворительно.
Приложение 5
Государственное образовательное учреждение высшего профессионального образования «Сибирский государственный медицинский университет Министерства здравоохранения и социального развития России»
(ГБОУ ВПО СибГМУ Минздравсоцразвития России)
ФАРМАЦЕВТИЧЕСКИЙ ФАКУЛЬТЕТ
Задание 5
Проведите испытание на подлинность (первая реакция) и количественное определение прокаина (новокаина) гидрохлорида.
Задание 6
Проведите испытание на подлинность (вторая реакция) и количественное определение теобромина (точную массу теобромина уменьшить в 5 раз и использовать 5 мл раствора 0,1 моль/л серебра нитрата).
Задание 7
Проведите испытание на подлинность (с 0,1 М раствором йода), рН (потенциометрически) и количественное определение кислоты аскорбиновой.
Задание 8
Проведите определение удельного вращения и количественного содержания кислоты глютаминовой.
Задание 9
Проведите испытания подлинности (с 0.1 М раствором калия йодата), прозрачности раствора и количественное определениеметамизола натрия (анальгина).
Задание 10
Проведите испытание подлинности, обнаружение примеси солей кальция и количественное определение декстрозы (глюкозы)йодометрическим методом по методике: Около 0,1г препарата (точная масса) растворяют в мерной колбе вместимостью 100 мл, доводят водой до метки
( раствор А). 5 мл раствора А переносят в колбу коническую вместимостью 250 мл, прибавляют 5 мл 0,1 моль/л раствора йода, 10 мл 0,1 моль/л раствора натра едкого и оставляют на 20 мин, после чего добавляют 5 мл разведенной кислоты серной и выделившийся йод титруют 0,1 моль/л раствором натрия тиосульфата (индикатор – раствор крахмала).
Параллельно проводят контрольный опыт.
1 мл 0,1 моль/л раствора йода соответствует 0,009985 г глюкозы.
Задание 11
Проведите определение примесей сульфатов, хлоридов, кальция, аммиака в воде очищенной.
Задание 12
Проведите определение подлинности и количественного содержания магния сульфата .
Задание 13
Проведите определение подлинности ксантинола никотината методом тонкослой хроматографии.
Задание 14
Проведите определение примеси теофиллина в ксантиноле никотинатеметодом тонкослойной хроматографии.
Задание 15
Проведите испытание на примеси сульфатов и солей аммония, количественное определение натрия хлорида.
Задание 16
Проведите испытание натрия хлорида на прозрачность, цветность и примеси кальция, магния.
Задание 17
Проведите определение рН (потенциометрически) и количественное содержание кальция глюконата.
Анализ порошков
Задание 33
Проведите анализ бензокаина(анестезина)в лекарственной форме:
Папаверина гидрохлорида 0,02
Бензокаина 0,2
Задание 34
Установите подлинность и количественное содержание кислоты ацетилсалициловой в лекарственной форме:
Кислоты ацетилсалициловой 0,3
Кофеин-бензоата натрия 0,1

Задание № 35
Проведите количественное определение нитрофурала (фурацилина) фотоэлектроколориметрическим методом в лекарственной форме:
Раствора нитрофурала 1:5000 500 мл
Методика количественного определения. 0,5 мл анализируемого раствора помещают в коническую колбу вместимостью 50 мл, прибавляют пипеткой 7,5 мл воды очищенной, 2 мл 0,1 моль/л натрия гидроксида перемешивают, и оставляют на 20 мин. Затем измеряют оптическую плотность (D1) с помощью фотоэлектроколориметра при длине волны около 450 нм в кювете толщиной слоя 10 мм. В качестве контрольного раствора используют воду. Параллельно проводят определение с 0,5 мл 0,02% стандартного раствора нитрофурала и измеряют оптическую плотность (D2). Содержание нитрофурала в 5000 мл лекарственной формы в граммах (Х) вычисляют по формуле:

Х= 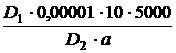
 ,
, 


где а – объем анализируемого раствора, взятый для анализа, мл;
0,00001 – концентрация стандартного раствора, г/мл;
10 – разведение, мл;
5000 – объём, приготовленной лекарственной формы, мл.
Кафедра фармацевтической химии
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
К ПРОИЗВОДСТВЕННОЙ ПРАКТИКЕ
по фармацевтическому анализу
для студентов 5 курса фармацевтического факультета
Томск 2013
Блинникова А.А. Методические рекомендациик производственной практике, зачёту по фармацевтическому анализу. – Томск: СибГМУ, 2010. – 28 с.
Методические рекомендации к производственной практике, зачёту по фармацевтическому анализу подготовлены в соответствии с учебной программой дисциплины и квалификационной характеристикой специалиста.
Утверждено решением методической комиссии фармацевтического факультета Сибирского государственного медицинского университета (протокол № __ от «__» _______2010 г.).
©А.А. Блинникова
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ К ПРОВЕДЕНИЮ ПРОИЗВОДСТВЕННОЙ ПРАКТИКИ, ЗАЧЁТА ПО ФАРМАНАЛИЗУ
Цели практики: закрепление полученных в учебном процессе теоретических знаний, практических навыков и умений для решения конкретных задач практической деятельности провизора-аналитика в условиях аптек, контрольно-аналитических лабораторий, аптечных складов и лабораторий НИИ.
Производственная практика по фармацевтическому анализу( контролю качества лекарственных средств) базируется на знаниях и умениях, полученных при изучении дисциплины «Фармацевтическая химия» в течение 5-9 семестров.
До начала производственной практики студент должен знать:
- законы и законодательные акты о здравоохранении, стандартизации и контроле качества лекарственных средств, порядке их хранения, охране окружающей среды, санитарном режиме и технике безопасности, об административной и уголовной ответственности за их нарушение;
- принципы фармацевтической этики и деонтологии;
- систему государственного контроля качества лекарственных средств;
- контрольно-разрешительную систему обеспечения качества лекарственных средств, организацию контроля качества лекарственных средств в испытательных лабораториях и в аптеках;
- общие методы анализа согласно действующему изданию Государственной фармакопеи: физические, химические и физико-химические;
- статистическую обработку результатов химического эксперимента и результатов микробиологических испытаний;
- контроль качества лекарственных средств мелкосерийного производства, виды и методы внутриаптечного контроля;
- экологический контроль фармацевтических производств (вода, почва, воздух) и фармацевтических препаратов;
- развитие исследований по созданию новых и совершенствованию действующих методов оценки качества лекарственных средств, относительность требований и методов оценки качества, их комплексность и взаимосвязь, оценка пригодности (валидация) методов и способов оценки качества.
После прохождения производственной практики студент должен
знать:
- общие методы оценки качества ЛС, возможность использования каждого метода в зависимости от способа получения ЛС, исходного сырья, структуры ЛВ, физико-химических процессов, которые могут происходить во время хранения и обращения ЛС;
- факторы, влияющие на качество ЛС на всех этапах обращения. Определение главных факторов в зависимости от свойств ЛВ (окислительно-восстановительных, способности к гидролизу, полимеризации и.т.д.). Возможность предотвращения влияния внешних факторов на доброкачественность ЛС;
- химические методы, положенные в основу качественного анализа ЛС. Основные структурные фрагменты ЛВ, по которым проводится идентификация неорганических и органических ЛВ. Общие и специфические реакции на отдельные катионы, анионы и функциональные группы;
- химические методы, положенные в основу количественного анализа ЛС. Уравнения химических реакций, проходящих при кислотно-основном, окислительно-восстановительном, осадительном, комплексонометрическом титровании;
- принципы, положенные в основу физико-химических методов анализа ЛС;
- оборудование и реактивы для проведения химического анализа ЛС. Требования к реактивам для проведения испытаний на чистоту, подлинность и количественного определения;
- оборудование и реактивы для проведения физико-химического анализа ЛВ. Принципиальную схему рефрактометра, фотоколориметра, спектрофотометра, ГЖХ, ВЭЖХ;
- структуру НД, регламентирующей качество ЛС. Особенности структуры ФС и ФСП;
- способы определения физико-химических констант ЛВ: температуры плавления, угла вращения, удельного показателя поглощения, температуры кипения;
- понятие валидации. Валидационные характеристики методик качественного и количественного анализа.
Уметь:
- пользоваться нормативной документацией и проводить фармакопейный анализ лекарственных средств;
- взвешивать на аптечных и аналитических весах;
- измерять объемы жидкости с помощью мерных цилиндров, бюреток, пипеток;
- выпаривать жидкости на водяной и песчаной бане;
- титровать с помощью пипетки и бюретки;
- измерять показатель преломления с помощью рефрактометра;
- измерять величину светопоглощения с помощью фотоколориметра и спектрофотометра;
- измерять угол вращения с помощью поляриметра;
- наносить пробы на хроматографическую пластинку или бумагу, готовить подвижную фазу, проводить хроматографирование и проявление;
- рассчитывать содержание вещества по результатам титриметрического или физико-химического анализа;
- выбирать реакции для проведения качественного анализа лекарственных веществ в соответствии с наличием в
