Деполяризующие миорелаксанты
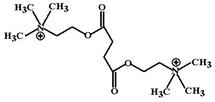 Все деполяризующие миорелаксанты имеют гибкую линейную структуру с четко сформированными двумя фрагментами ацетилхолина. Расстояние между их катионными головками составляет 1,0±0,1 нм. Bovet назвал эти средства лептокураре (от греч. leptos – тонкий, нежный).
Все деполяризующие миорелаксанты имеют гибкую линейную структуру с четко сформированными двумя фрагментами ацетилхолина. Расстояние между их катионными головками составляет 1,0±0,1 нм. Bovet назвал эти средства лептокураре (от греч. leptos – тонкий, нежный).
Сукцинилхолин (Succinylcholine, Dythylin, Listenon, Suxamethonii iodide) МД: При введении в организм сукцинилхолин быстро захватывается мышечными волокнами в количествах в 20 раз больших, чем антидеполяризующие миорелаксанты. Он связывается с активным центром НМ-холинорецептора и вызывает его длительную активацию. Под влиянием активированных холинорецепторов открываются Na+-каналы мышечного волокна, развивается деполяризация его мембраны и происходит начальное сокращение мышцы.
Сукцинилхолин не способен, однако, быстро диссоциировать от рецепторов и они остаются в состоянии длительной активации, сохраняя деполяризацию мембраны. Деполяризация вызывает постепенное закрытие инактивационных ворот Na+-каналов и они переходят в нерабочее состояние. Мышца расслабляется и перестает отвечать на нервные импульсы. Возникает вялый паралич.
В мышцах человека, а также в быстрых скелетных мышцах кошек обычно наблюдается только деполяризующее действие сукцинилхолина, которое получило название I фазы деполяризационного блока. Однако, в медленных скелетных мышцах кошек и у человека при совместном назначении с галогенированными наркотическими газами можно вызвать т.н. II фазу деполяризующего блока[11].
Развитие этой фазы связывают со следующим механизмом. Постепенно, за счет открытия K+-каналов и выхода из клетки ионов калия ее мембрана реполяризуется и чувствительность натриевых каналов восстанавливается. Однако, ацетилхолин, которые выделяется при прохождении нервного импульса, по-прежнему не способен вызвать активации рецепторов, поскольку они остаются связанными с сукцинилхолином, который экранирует их активный центр. Т.о. в этой фазе сукцинилхолин ведет себя как типичный антидеполяризующий миорелаксант и поддерживает состояние вялого паралича мышц.
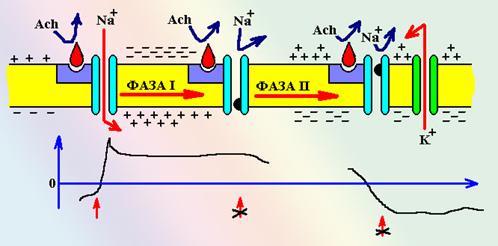
Схема 8. Фазный характер действия сукцинилхолина. Вначале сукцинилхолин вызывает длительную активацию рецептора, что вызывает открытие каналов и ток ионов натрия через мембрану с генерацией потенциала действия. Мембрана деполяризуется и становится невозбудимой (ФАЗА I). Постепенно закрываются инактивационные ворота натриевых каналов и, за счет выхода калия из мышечного волокна, возникает гиперполяризация мембраны. В этом состоянии возбуждение было бы возможно, но сукцинилхолин продолжает занимать активный центр рецептора и не позволяет ацетилхолину обеспечить генерацию потенциала (ФАЗА II).
Окончание действия сукцинилхолина связано с его гидролизом под влиянием холинэстеразы (основную роль в гидролизе играет псевдохолинэстераза).
ФК: Молекула сукцинилхолина содержит 2 четвертичных атома азота, поэтому он крайне плохо проникает через гистогематические барьеры, не поступает в ЦНС и для создания миорелаксации используется только в виде внутривенной инфузии или инъекции.
Метаболизм сукцинилхолина протекает в плазме крови за счет гидролиза псевдохолинэстеразой на 2 молекулы холина, ацетата и сукцинат. Скорость гидролиза не зависит от функции печени и почек, поэтому сукцинилхолин может применяться у пациентов с хроническими заболеваниями печени и почек.
ФЭ: Миопаралитическое действие сукцинилхолина развивается уже через 30-60 секунд после введения и сохраняется всего лишь 10-15 мин. Сразу после введенения может наблюдаться кратковременное подергивание (фасцикуляции) мышц, которые сменяются параличом. Но, при этом, характер развития паралича отличается от такового при введении антидеполяризующих миорелаксантов. Первыми выключаются мышцы шеи и конечностей, затем паралич захватывает мышцы лица, жевательные и глазодвигательные мышцы (однако, эти группы мышц никогда не парализуются полностью), мышцы глотки. В последнюю очередь выключается мускулатура туловища.
Респираторные мышцы чрезвычайно устойчивы к действию сукцинилхолина (его широта миопаралитического действия составляет »1:1.000) и блокируются только при использовании токсических доз лекарства.
Таблица 7. Сравнительная характеристика деполяризующего и антидеполяризущего блоков.
| Параметр | Антидеполяризующий блок (тубокурарин) | Деполяризующий блок (сукцинилхолин) |
| Вид паралича | Вялый | Фасцикуляции, переходящие в вялый паралич |
| Видовая чувствительность | Крысы > кролики > кошки | Кошки > кролики > крысы |
| Влияние на мембрану мышечного волокна | Повышение порога деполяризации | Деполяризация |
| Влияние на изолированную скелетную мышцу | Отсутствует | Контрактура мышцы |
| Введение неостигмина | Устраняет блок | Не влияет на блок |
| Снижение температуры | Уменьшает блок | Усиливает блок |
| Действие катодного тока на мышцу | Уменьшает блок | Усиливает блок |
| Порядок развития паралича | Пальцы, глаза → конечности → шея, лицо → туловище → дыхательные мышцы | Шея, конечности → лицо, челюсти, глаза, глотка → туловище → → → дыхательные мышцы |
Особенности применения. Сукцинилхолин наиболее часто применяют для проведения интубации трахеи, вправления вывиха бедра или плеча (т.к. в этих областях большая мышечная масса препятствует тракции кости). Однако, следует помнить, сто сукцинилхолин не подходит для выполнения репозиции при оскольчатых переломах, т.к. в этом случае, начальное подергивание мышц может вызвать смещение отломков и травму сосудисто-нервных пучков.
Обычно сукцинилхолин вводят в дозе 1,5-2,0 мг/кг.
НЭ: Сукцинилхолин является либератором гистамина и его введение может спровоцировать выброс гистамина, приводящий к бронхоспазму. Данный эффект можно предупредить, если предварительно выполнить инъекцию Н1-блокатора (антигистаминного средства) – дифенгидрамина (димедрола).
Фасцикуляции мышц, которые вызывает сукцинилхолин, приводят к микротравмам скелетных волокон, что после окончания действия лекарства сопровождается тянущими болями в мышцах, возникающими через 10-12 часов. Данный эффект удается предупредить предварительным введением 5-10 мг диазепама, который понижает мышечный тонус.
Длительная деполяризация скелетных мышц приводит к открытию калиевых каналов и выходу ионов калия из мышечного волокна в попытке его реполяризации. Потеря калия столь значительна, что может вызвать клинически значимую гиперкалиемию с мышечной слабостью, нарушением сердечного ритма по типу блокады (особенно у людей, которые принимают сердечные гликозиды).
Сукцинилхолин способен стимулировать вегетативные ганглии. Это может привести к повышению артериального давления. Кроме того, он повышает тонус наружных мышц глаза и несколько сдавливает глазное яблоко, поэтому его не применяют в офтальмологии, а также у пациентов с травматическими повреждениями глазного яблока.
Иногда при использовании сукцинилхолина развивается идиосинкразия, которая может проявляться в виде двух состояний:
· Аномальное удлинение миопаралитического действия сукцинилхолина до 3-5 часов. Данный эффект связан с наследственным дефицитом псевдохолинэстеразы (встречается с частотой 1:8.000-9.000). Для устранения эффекта сукцинилхолина таким пациентам следует ввести псевдохолинэстеразу или перелить »500 мл крови донора (она также содержит псевдохолинэстеразу).
· Злокачественная гипертермия. Встречается с частотой 1:15.000 у детей и 1:100.000 у взрослых. Вероятность развития повышается при совместном применении сукцинилхолина с галогенированными анестезирующими газами. Полагают, что развитие этого синдрома связано с наследственным дефектом строения Т-трубочек мышечных волокон. Под влиянием сукцинилхолина происходит массивный выброс ионов кальция из Т-трубочек саркоплазматического ретикулума и это приводит к стимуляции биоэнергетических процессов в мышцах, усилению сократительного термогенеза. Симптоматика злокачественной гиперетермии характеризуется:
] Гипертермией (температура повышается на 0,5°С за каждые 15 мин);
] Ригидностью скелетных мышц вместо ожидаемой релаксации;
] Тахикардией свыше 140 ударов в минуту с переходом в аритмию и острую сердечную недостаточность;
] Метаболическим и дыхательным ацидозом (усиливается образование лактата и СО2);
] Гиперкалиемией;
] ДВС-синдромом.
Помощь при развитии злокачественной гипертермии заключается во внутривенном введении дантролена (лекарства, которое препятствует освобождению кальция из саркоплазматического ретикулума), ингаляции 100% кислорода, устранении гипертермии (пациента обкладывают льдом, проводят лаваж желудка и мочевого пузыря ледяным физиологическим раствором, внутривенно вливают физиологический раствор, охлажденный до 4°С в объеме 500-1000 мл). Мероприятия продолжают до тех пор, пока температура тела не опустится ниже 38°С. Для устранения гиперкалиемии вводят внутривенно 20-40 ЕД инсулина в 40-60 мл 40% глюкозы.
 ФВ: порошок в ампулах по 100, 250 и 500 мг, раствор 2% в ампулах по 5 и 10 мл.
ФВ: порошок в ампулах по 100, 250 и 500 мг, раствор 2% в ампулах по 5 и 10 мл.
Мелликтин (Mellictinum) Представляет собой гидройодид метилликанонитина – алкалоида живокости сетчатоплодной и полубородатой (Delphinium dictiocarpum et semibarbatum). Способен блокировать как НН, так и НМ-типы холинорецепторов, сочетая миорелаксирующее и ганглиоблокирующее действия.
Молекулы мелликтина содержат третичный азот, поэтому он хорошо всасывается при пероральном приеме.
Миорелаксирующий эффект мелликтина напоминает действие антидеполяризующих миорелаксантов. Его применяли для уменьшения спастических состояний мышц при паркинсонизме, арахноэнцефалите, болезни Литтля, центральных параличах после инсультов.
Мелликтин назначали внутрь по 20 мг 1 раз в день, постепенно повышая частоту приема до 5 раз в день. Курсы лечения 1-2 месяца повторяли 3-4 раза в год.
ФВ: таблетки по 20 мг.
Антагонисты миорелаксантов
1. При передозировке антидеполяризующих миорелаксантов или необходимости срочно прекратить их миопаралитическое действие используют антихолинэстеразные средства. Они блокируют холинэстеразу, в результате чего гидролиз ацетилхолина прекращается и его концентрация в синапсе повышается. Избыток ацетилхолина способен вытеснить миорелаксант из связи с рецептором и восстановить проводимость. Обычно прибегают к внутривенному введению 0,5-2,0 мл 0,05% раствора неостигмина. Поскольку неостигмин повышает уровень ацетилхолина как в нейро-мышечных синапсах, так и в М-холинергических синапсах внутренних органов, то, чтобы избежать нежелательного М-холиномиметического эффекта неостигмина перед его использованием пациенту вводят 0,5-1,0 мг атропина.
2. При передозировке деполяризующих миорелаксантов их эффект не требует специального медикаментозного устранения, ввиду быстрого гидролиза псевдохолинэстеразой. У пациентов с дефицитом псевдохолинэстеразы его действие можно прекратить путем внутривенного введения 500 мл донорской крови, которая содержит этот фермент.
