Поступление через кожу
Морфология, биохимия кожи препятствуют резорбции большинства токсикантов. Для водорастворимых веществ кожа представляет непреодолимый барьер. Некоторой проницаемостью кожные покровы обладают для веществ, хорошо растворимых в липидах (например, для зомана, фосфорилтиохолинов, иприта, люизита, тетраэтилсвинца и т.д.). Возможны два способа прохождения токсиканта через кожу: трансэпидермальный (через клетки эпидермиса) и трансфолликулярный (через волосяные фолликулы).
Помимо способности растворяться в липидах, на скорость резорбции веществ через кожу влияет: агрегатное состояние, дисперсность (размер частиц аэрозолей), площадь и область кожных покровов, на которую нанесен токсикант, интенсивность кровотока в кожных покровах.
Механические повреждения, мацерация кожи, раздражение, сопровождающиеся усилением кровотока, усиливают процесс резорбции токсикантов. Некоторые органические растворители, разрушающие липидный слой кожи, могут усиливать кожную резорбцию.
Поступление через желудочно-кишечный тракт
Энтеральная резорбция предполагает хотя бы минимальную растворимость токсиканта в содержимом ЖКТ. Слизистая желудочно-кишечного тракта в силу особенностей строения приспособлена для быстрой резорбции веществ. Поскольку сосудистая сеть желудочно-кишечного тракта развита хорошо, резорбция здесь не лимитирована фактором кровоснабжения. Закономерности резорбции аналогичны во всех отделах желудочно-кишечного тракта.
Имеющиеся особенности всасывания в различных отделах ЖКТ определяются:
- различиями рН содержимого отделов. Содержимое желудка имеет кислую реакцию. Слабые кислоты (например, производные барбитуровой кислоты и др.), в основном, здесь находятся в недиссоциированном состоянии, и потому относительно легко всасываются. Слабые основания (алкалоиды), напротив, в желудочном соке находятся в форме ионов, и потому - не всасываются. В кишечнике рН - щелочная и поэтому здесь преобладает ионизированная форма кислот и неионизированная форма слабых оснований.
- неодинаковой площадью всасывающей поверхности (см. табл. 1).
Количество и качество пищи, принятой вместе (до, после) с токсикантом могут существенно повлиять на скорость его резорбции.
Распределение
Транспорт веществ кровью
Всосавшееся вещество попадает в кровь и с током крови разносится по организму. Кровь может осуществлять транспорт веществ в свободной и связанной форме.
Способностью связывать ксенобиотики обладают альбумины, гликопротеиды и липопротеиды плазмы крови. В основе связывания ксенобиотиков белками лежит образование между ними слабых гидрофобных, водородных и ионных связей. Связанные соединения приобретают характеристики распределения, свойственные белкам. Сильные связи белок-ксенобиотик затрудняют отток вещества в ткани.
Положительно заряженные ксенобиотики могут адсорбироваться на отрицательно заряженной мембране эритроцитов. Липофильные вещества проникают через эритроцитарную мембрану и взаимодействуют с гемоглобином. Связавшаяся с гемоглобином фракция ксенобиотика порой не в состоянии диффундировать из клетки и длительно циркулирует в таком состоянии в крови.
Поступление в ткани
Характер распределения токсикантов в организме определяется общими закономерностями (см. выше). Дополнительными факторами, влияющими на процесс, являются интенсивность кровоснабжения органов (рис. 6) а также суммарная площадь их капиллярного русла (табл. 7).
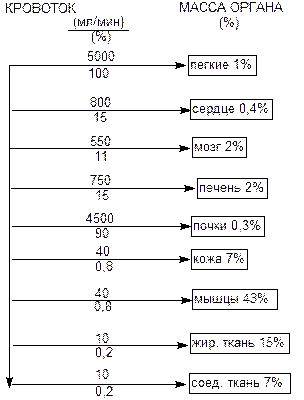
Рисунок 6. Особенности кровоснабжения различных органов и тканей
Таблица 7.
Площадь капиллярного русла различных органов собаки, см2/г ткани
| Мозг | Почки | Печень | Легкие | Мышцы |
Так, например, захвату ксенобиотиков печенью способствуют хорошее кровоснабжение органа, высокая степень порозности эндотелия капиллярного русла. Клеточные мембраны гепатоцитов также содержат большое количество пор, что облегчает поступление веществ в клетки. Помимо указанного, накоплению ксенобиотиков в органе способствуют механизмы их активного захвата из плазмы крови (активный транспорт кислот, щелочей, пиноцитоз макромолекул).
Напротив, проникновение из крови в ЦНС многих (прежде всего водорастворимых) ксенобиотиков существенно затруднено наличием так называемого гематоэнцефалического барьера.
Гематоэнцефалический барьер формируется при участии ряда анатомических структур головного мозга.
Во-первых, эндотелий капиллярного русла головного мозга отличается от эндотелия других органов чрезвычайно тесным контактом клеток друг с другом. Эффективный радиус пор капилляров мозга значительно меньше, чем в других тканях и составляет, например, у кролика 0,7 - 0,9 нм. Крупные молекулы не в состоянии проникать через эндотелиальный барьер. Водорастворимые и заряженные молекулы могут проходить непосредственно через биомембраны и цитоплазму эндотелиальных клеток только в том случае, если имеют малые размеры (CN-). В норме эндотелиальные клетки мозга лишены способности к пиноцитозу. Лишь при некоторых патологических состояниях (гипоксия мозга) в эндотелии сосудов образуются пиноцитарные вакуоли, при этом возрастает проницаемость гематоэнцефалического барьера, увеличивается уязвимость мозга для действия токсикантов.
Во-вторых, капилляры мозга плотно окутаны отростками астроцитарной глии. Астроцитарная оболочка препятствует проникновению гидрофильных ксенобиотиков из крови в ткань мозга и их взаимодействию с другими клеточными элементами. В некоторых областях мозга, таких как срединное возвышение гипоталямуса, медиальная преоптичесая область, область четвертого желудочка мозга, астроцитарная оболочка капилляров развита сравнительно слабо. В этих регионах возможно проникновение водорастворимых и даже заряженных молекул токсикантов в ЦНС, но также в ограниченном количестве.
Наконец последней структурой, вносящей вклад в формирование ГЭБ, является базальная мембрана, залегающая между эндотелиальными клетками капилляров и отростками астроцитов. Эта мембрана имеет упорядоченную фибриллярную макропротеидную структуру, обеспечивающую избирательное проникновение в мозг ряда важных для обеспечения его жизнедеятельности молекул (кислород, глюкоза и др.).
Аналогичный ГЭБ барьер окружает периферический отдел нервной системы (гематоневральный барьер). Однако также как и в ЦНС здесь имеются анатомические образования с повышенной проницаемостью для токсикантов. К числу таких относятся спинальные корешки дорзальных (чувствительных) ганглиев и вегетативные (автономные) ганглии.
Плацентарный барьер проницаем для многих веществ, в том числе высокомолекулярных соединений. Это обстоятельство может иметь неблагоприятные последствия для плода особенно при попадании токсикантов в организм матери в первые 12 недель беременности (период органогенеза).
Важным элементом распределения некоторых ксенобиотиков в организме является их депонирование. Депонирование - это накопление и длительное сохранение химического вещества в относительно высокой концентрации в одном или нескольких органах (или тканях). Порой депонирование не сопровождается повреждением биологически значимых молекул-мишеней (токсический процесс не формируется).
В основе депонирования лежат два явления:
- высокое физико-химическое сродство ксенобиотика к неким компонентам биосистемы (химическое взаимодействие с элементами биосистемы или избирательное накопление липофильных веществ в жировой ткани);
- кумуляция благодаря избирательному, активному захвату токсиканта клетками органа (ткани).
Ряд токсикантов депонируется в тканях настолько прочно, что выведение их из организма практически невозможно. Например, период полуэлиминации кадмия из организма человека составляет более 20 лет.
Явление депонирование веществ связано с явлением кумуляция, но не тождественно ему. Под материальной кумуляцией понимают процесс постепенного накопления токсиканта при длительном поступлении в организм преимущественно в области функционально-значимых структур-мишеней, действие на которые приводит к развитию токсического процесса. Явление кумуляции лежит в основе хронических интоксикаций. (В ряде случаев выявляется так называемая функциональная кумуляция - накопление неблагоприятных эффектов токсиканта при его продолжительном введении).
Элиминация
Элиминацией называется вся совокупность процессов, приводящих к снижению содержания токсиканта в организме. Она включает процессы экскреции (выведения) ксенобиотика из организма и его биотрансформацию.
Экскреция
Основными органами экскреции являются легкие (для летучих соединений), почки, печень, в меньшей степени слизистая желудочно-кишечного тракта, кожа и ее придатки.
Легочная экскреция
Газы и пары летучих веществ выделяются через легкие в соответствии с градиентом их парциального давления между кровью и альвеолярным воздухом. Закономерности экскреции газообразных (парообразных) веществ полностью идентичны закономерностям их поступления через легкие (см. выше).
Почечная экскреция
Почки - важнейший орган выделения. Через почки выводятся продукты обмена веществ, многие ксенобиотики и продукты их метаболизма. Масса почек чуть менее 0,3% массы тела, однако, через орган протекает около 30% минутного объема крови. Благодаря хорошему кровоснабжению, находящиеся в крови вещества, подлежащие выведению, быстро переходят в орган, а затем и выделяются с мочой. В основе процесса лежат три механизма (рис. 7):
- фильтрация через гломерулярно-капиллярный барьер;
- секреция эпителием почечных канальцев;
- реабсорбция клетками эпителия.
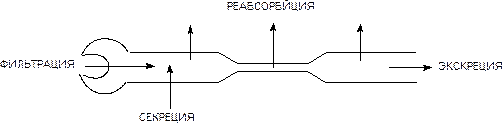
Рисунок 7. Механизмы, регулирующие процесс экскреции ксенобиотиков через почки
Фильтрация:
- все низкомолекулярные вещества, находящиеся в растворенном состоянии в плазме крови.
Секреция:
- органические кислоты, мочевая кислота и т.д.;
- сильные органические основания, тетраэтиламмоний, метилникотинамид и т.д.;
Реабсорбция:
- пассивная обратная диффузия всех жирорастворимых веществ;
- неионизированные молекулы органических кислот;
- активная реабсорбция глюкозы, лактата, аминокислот, мочевой кислоты, электролитов, воды.
Через почки протекает около 700 мл плазмы крови в минуту, из которых 20% (125 - 130 мл/мин) отфильтровывается через гломерулярно-капиллярный барьер. Собирающаяся в почечных клубочках первичная моча, по сути, представляет собой сыворотку крови. Более 99% отфильтрованной жидкости реабсорбируется в почечных канальцах. При этом концентрация растворенных в моче веществ возрастает в 100 раз. Хорошо растворимые в липидах соединения, по этой причине, практически полностью диффундируют из первичной мочи, через эпителий почечных канальцев, обратно в кровь (реабсорбция). Выведение таких веществ из организма практически не происходит.
Способность к выведению через почки у слабых кислот и оснований во многом определяется рН первичной мочи: выведение слабых оснований усиливается при подкислении мочи (преобладает ионизированная форма оснований - затруднена реабсорбция их в канальцах); выделение слабых кислот усиливается при подщелачивании мочи (преобладает ионизированная форма кислот).
Многие токсиканты выводятся через почки с помощью механизма активной секреции. Функции секретирующей структуры выполняет эпителий почечных канальцев. Существуют независимые механизмы активного транспорта для веществ со щелочными и кислотными свойствами.
Печеночная экскреция
Печеночная экскреция - отчасти следствие простой диффузии веществ в желчь, отчасти - активного транспорта ксенобиотиков, осуществляемого гепатоцитами. Благодаря активному транспорту отношение концентраций веществ в желчи и плазме крови значительно выше 1. Высокая концентрация химических веществ в желчи обеспечивает осмос воды из сосудистого русла в желчные ходы. Наиболее активно печенью выводятся вещества с молекулярной массой более 600 дальтон, имеющие в структуре полярную анионную или катионную группу.
Ряд ксенобиотиков, выделяющихся с желчью (липофильные вещества, либо гидрофильные соединения, превращающиеся в липофильные под влиянием кишечной флоры), способны к обратному всасыванию слизистой кишечника и по системе портальной вены повторно накапливаются в печени. Это явление называется гепато-энтеральной циркуляцией.
4.4.2. Метаболизм ксенобиотиков (биотрансформация)
Многие ксенобиотики в организме подвергаются метаболическим превращениям (биотрансформации).
Основной биологический смысл биотрансформации - превращение исходного токсиканта в форму, удобную для скорейшей экскреции. Биотрансформация - ферментативный процесс.
Выделяют 2 фазы метаболических превращений чужеродных соединений (рис. 8):
- I фаза, окислительной, восстановительной либо гидролитической трансформации молекулы;
- II фаза - синтетических превращений.
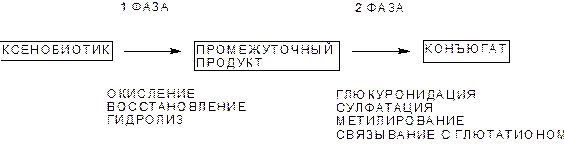
Рисунок 8. Фазы метаболизма чужеродных соединений
В первой фазе происходят следующие реакции биотрансформации:
- окисление - гидроксилирование, декарбоксилирование, образование оксидов, десульфурирование, дегалогенизирование молекул, окисление спиртов и альдегидов;
- восстановление - восстановление альдегидов, азовосстановление, нитровосстановление;
- гидролиз - расщепление эфиров, амидных связей.
Основные энзимы, активирующие процессы биотрансформации первой фазы: цитохром Р-450 зависимые оксидазы смешанной функции (Р-450), флавинсодержащие монооксигеназы смешанной функции (ФМО), гидропероксидазы, алкоголь и альдегиддегидрогеназы, флавопротеинредуктазы, эпоксидгидраза.
Нередко в результате метаболизма вещества на первом этапе образуются промежуточные продукты, обладающие высокой биологической активностью (табл. 8).
Таблица 8.
