Изменение органов и систем органов в процессе старения
Как правило, после 40-50 лет у человека возникают стойкие внешние проявления старения, в частности кожных покровов. Появляются морщины, образующиеся из-за потери подкожной жировой ткани, пигментные пятна. Кожа становится сухой и шершавой в связи с уменьшением количества потовых желёз, теряется её эластичность, она становится дряблой.
Признаки старения сердечно – сосудистой системы становятся заметными обычно в возрасте после 40 лет. Закономерные изменения наблюдаются в стенках сосудов: в них откладываются липиды, прежде всего холестерин, что наряду с другими структурными превращениями снижает эластичность и искажает ответы на различные стимулы, регулирующие кровообращение. Типичным является разрастание в стенках сосудов и сердца соединительной ткани , замещающей рабочую мышечную ткань. В результате снижается эффективность работы сердца и нарушается кровоснабжение тканей и органов.
В основе функциональных расстройств дыхательной системы лежит разрушение межальвеолярных перегородок, что сокращает дыхательную поверхность, разрастание в лёгких соединительной ткани, снижает эффективность аэрогематического обмена кислорода. В итоге с возрастом падает жизненная ёмкость лёгких.
Изменением в системе пищеварения является потеря зубов. Падает эффективность функционирования пищеварительных желёз, нарушения двигательной функции кишечника нередко приводят к привычным запорам.
В процессе старения страдает функция мочевыделительной системы, снижается интенсивность фильтрации в почечных клубочках, так же как и обратное всасывание веществ из фильтрата в почечных канальцах. Ухудшение функции мочевыделения объясняется гибельюс возрастом значительного количества нефронов.
Снижается сила сокращений поперечно – полосатой мускулатуры, быстрее развивается утомление, наблюдается атрофия мышц. Характерно снижение прочности костей.
В процессе старения организма происходят существенные изменения в репродуктивной системе. У женщин овогенез прекращается по достижении ими менопаузы. Образование сперматозоидов в мужском организме возможно даже в преклонном возрасте.
Изменения гормонального профиля людей в связи с угасанием репродуктивной функции носит сложный характер. Происходит прогрессивное снижение с возрастом концентрации у мужчин тестостерона, а у женщин эстрадиола и прогестерона. Эти сдвиги сопровождаются повышением секреции эстрадиола и прогестерона у мужчин и тестостерона у женщин.
Изменения в процессе старения функций эндокринной системы носит объективно сложный характер. Ухудшается перенос гормонов к тканям.
Изменения нервной системы включают нарастающую гибель нейронов, снижение синтеза медиаторов, ослабление связей между отдельными мозговыми структурами, уменьшение скорости проведения нервных импульсов. С большим трудом вырабатываются условные рефлексы.
Происходит снижение надёжности механизмов регуляции, направленных на поддержание постоянства жизненно важных параметров внутренней среды организма – гомеостаза.
В старости наблюдается снижение функций практически всех органов чувств. Падает острота зрения, появляется старческая дальнозоркость, снижается чувствительность органа слуха, хуже различаются запах и вкус, нарушается чувство равновесия.
С возрастом заметно изменяются функции иммунной системы. За гуморальный иммунитет ответственны В-лимфоциты, за клеточный иммунитет Т-лимфоциты, хотя могут участвовать и в реакциях гуморального иммунитета. К старости наблюдается ослабление реакций как гуморального, так и клеточного иммунитета. В стареющем организме клетки иммунной системы ошибочно вырабатывают антитела против собственных клеток и белков. Таким образом, старение сопровождается нарастанием аутоиммунных реакций.
Изменения в процессе старения органов кроветворной системы заключаются в снижении продукции эритроцитов. С возрастом способность костного мозга к восстановлению массы эритроцитов падает почти в 6 раз.
Молекулярные и клеточные проявления старения многообразны. Они заключаются в изменении показателей потоков информации и энергии, состояния ультраструктур дифференцированных клеток, снижается интенсивность клеточной пролиферации.
В дифференцированных клетках млекопитающих животных старение сопровождается в целом снижением транскрипционной активности. Так, у мышей интенсивность синтеза РНК в ядрах печёночных и нервных клеток между 12-м и 30-м месяцами жизни падает на 50 %. Изменение синтеза относится не только к рРНК, не кодирующим структуру белков, но и мРНК. В сравнении с активным репродуктивным периодом жизни в стареющем организме действительно наблюдается исчезновение в клетках определённых типом мРНК, правда, в это же время регистрируется появление некоторых типов мРНК, не образующихся ранее. Таким образом, речь идёт о частичной смене биологической информации, используемой клеткой в разном возрасте.
Скорость снижения транскрипционной активности ДНК в постмитотических высокодифференцированных клетках, к примеру нервных, зависит от условий их существования в течение жизни, в частности от напряжённости их функционирования. Так, одна и та же функциональная нагрузка, распределённая между меньшим количеством клеток, приводит к более раннему падению уровня транскрипции в их ядрах. Было также показано, что параллельно изменению скорости снижения транскрипции сокращается максимально достигаемая животными продолжительность жизни. ДНК эукариотических клеток находится в комплексе с белками – гистоновыми и негистоновыми, образуя вместе с ними хроматин ядер. Предполагают, что регуляция транскрипции информации с ДНК происходит путём изменения ДНК-белковых связей в хроматине. С возрастом такие связи становятся менее подвижными, отмечается снижение содержания в хроматине негистоновых белков.
Изменение трансляции в процессе старения изучают по содержанию рРНК, мРНК, активности аминоацил-тРНК-синтетаз (ферменты активации аминокислот). Интенсивность белкового синтеза в целом снижается в зрелом возрасте.
Немало важное значение при старении имеют изменения энергетики организма, в частности обратная связь между продолжительностью жизни животных различных видов и удельной скоростью обмена веществ отмечена давно. Изменения потока энергии в процессе старения состоят в снижении количества митохондрий в клетках, а также падении эффективности их функционирования. Важным свойством стареющего организма является смещение в процессах энергообеспечения функций соотношения между тканевым дыханием и гликолизом (бескислородный путь образования АТФ) в пользу последнего.
Изменения в процессе старения ультраструктуры клеток затрагивают практически все органеллы общего и специального назначения. Одновременно может происходить накопление необычных веществ, иногда структурно оформленных (липофусцин). Наиболее заметна возрастная перестройка постмитотических высокоспециализированных клеток – нейронов, кардиомиоцитов.
Для стареющих нервных клеток типично обеднение цитоплазмы мембранами, сокращение объёма шероховатой ЭПС, увеличение содержания в клеточных телах микрофибрилл.
На определённом этапе прогрессивная эволюция жизни на земле оказалась связанной с переходом к более эффективному аэробному типу обеспечения процессов жизнедеятельности. Использование клетками кислорода приводит к образованию свободных радикалов (О 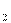 ОН, Н
ОН, Н 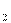 О
О 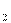 ), которые в силу чрезвычайной реакционной способности могут вызывать быстрые разрушения биологических структур (мембран,макромолекул). Неблагоприятным эффектам свободных радикалов в клетках противостоят закреплённые процессом эволюции природные антиоксидантные механизмы. К ним принадлежат ферменты, разрушающие пероксиды. В процессе старения действенность механизмов, нейтрализующих свободные радикалы и пероксиды, снижается. Свободные радикалы способны нарушить любое звено молекулярной организации клетки.
), которые в силу чрезвычайной реакционной способности могут вызывать быстрые разрушения биологических структур (мембран,макромолекул). Неблагоприятным эффектам свободных радикалов в клетках противостоят закреплённые процессом эволюции природные антиоксидантные механизмы. К ним принадлежат ферменты, разрушающие пероксиды. В процессе старения действенность механизмов, нейтрализующих свободные радикалы и пероксиды, снижается. Свободные радикалы способны нарушить любое звено молекулярной организации клетки.
С начала 60-х гг. появились новые взгляды на значение для старения и продолжительности жизни закономерностей клеточной пролиферации. На основании подсчёта числа делений фибробластов, высеваемых в культуру ткани от эмбриона человека и от людей в возрасте 20 лет и выше, было сделано заключение о пределе клеточных делений (лимит Хейфлика), которому соответствует видовая длительность жизни. Показано, что фибробласты мыши способны удваивать свою численность 14-28 раз, цыплёнка- 15- 35, человека – 40-60, черепахи – 72-114 раз.
