Азотитый баланс. биологическая полноценность белков
Белки (протеины) – это высокомолекулярные N-содержащие органические соединения, состоящие из остатков a-L-аминокислот, соединенных пептидными связями в строго определенной последовательности в полипептидной цепи.
Содержание белков в организме животных в среднем составляет 18 – 21 % (или 45 – 50 % в расчете на сухое вещество).
Белки в организме животных выполняют разнообразные функции, основными из которых являются:
- структурная. Белки входят в состав всех клеток, органов и тканей организма;
- каталитическая. Эту роль выполняют специфические белки – ферменты;
- защитная. Иммунитет организма обеспечивается белками иммуноглобулинами (антителами);
- регуляторная. В регуляции обмена веществ важная роль принадлежит гормонам, ряд из которых по химической природе являются белками (например, инсулин, регулирующий уровень глюкозы в крови);
- транспортная. Благодаря своей молекулярной массе белки могут адсорбировать на поверхности различные вещества и переносить по организму (альбумины). Транспортные белки переносят различные вещества (гемоглобин транспортирует кислород, трансферрин - железо, церулоплазмин - медь);
- cократительная. Примерами белков выполняющих эту функцию являются актин и миозин.
Энергетическая функция не является основной, т.к. белки используются в качестве энергетического топлива в последнюю очередь (при недостатке углеводов и липидов).
О белковом обмене в определенной степени можно судить на основе показателей азотистого баланса.
Азотистый баланс определяется на основании суточного потребления животным азотистых веществ с кормами, выделения их с калом и мочой. Он представляет собой отношение усвоенного азота к азоту, выделенному в виде конечных продуктов обмена. Различают 3 вида азотистого баланса:
1. Положительный – когда поступление азота превышает его выделение с мочой и калом в виде конечных продуктов распада белков и аминокислот. Это наблюдается в условиях нормального питания животных в период их роста и развития, во время беременности, лактации, яйцекладки и в восстановительную фазу после болезни. Такой баланс свидетельствует о преобладании синтеза белков над их распадом.
2. Азотистое равновесие характеризуется равным количеством поступивших азотистых веществ и выделенных в виде конечных продуктов обмена. Оно наступает у животных ко времени завершения периода интенсивного роста.
3. При отрицательном азотистом балансе азотистых веществ корма усваивается меньше, чем выделяется в виде конечных продуктов белкового обмена, т.е преобладает распад белков органов и тканей, который не компенсируется белками корма. Наиболее частой причиной отрицательного азотистого баланса является белковое голодание или наличие в рационе неполноценных белков. Такое же явление может наблюдаться при слабой доступности белков корма для усвоения их организмом, при гиповитаминозах, стрессе, различных заболеваниях острого и хронического характера.
Для обеспечения потребностей организма большое значение имеет количество и качество белков корма. Биологическая ценность белков зависит от их аминокислотного состава. Различают заменимые и незаменимые аминокислоты. Последние не синтезируются в организме животных. Кормовые белки растительного происхождения, как правило, не могут удовлетворять потребности организма в ряде незаменимых аминокислот, поэтому они являются неполноценными. На качество протеина особенно остро реагируют моногастричные животные (свиньи, лошади, птицы), а жвачные – сравнительно слабо, благодаря микробиологическим процессам в преджелудках. Поэтому для жвачных преимущественное значение имеет количество белка в суточном рационе. В тоже время КРС испытывает повышенную потребность в серосодержащих аминокислотах (цистеин, метионин), которые не восполняются микробиальным синтезом в рубце.
Для разных животных одни и теже белки могут быть неодинаково биологически ценны. Например, домашней птице необходимо давать такие корма, в белках которых кроме незаменимых аминокислот, содержатся также в достаточном количестве аргинин и глицин.
· переваривание белков и всасывание аминокислот
Необходимость расщепления белков корма вызвано тем, что они являются для организма чужеродными соединениями и кроме того, высокомолекулярными веществами, неспособными всасываться.
В желудочно-кишечном тракте (ЖКТ) белки корма подвергается действию ферментов класса гидролаз, подкласса пептидаз, в результате чего уничтожается видовая специфичность поступивших белков и они расщепляются до низкомолекулярных соединений – аминокислот, которые могут всасываться в тонком кишечнике. Схема распада белков в ЖКТ указана на рис. 15.
В желудке на белки действует соляная кислота. Она способствует набуханию белков, тем самым делая их доступными для ферментативного расщепления. Она активирует пепсиноген, стерилизует содержимое желудка, препятствуя развитию гнилостных и бродильных процессов.
Наиболее важными протеолитическими ферментами желудочного сока являются пепсин и химозин. Пепсинсинтезируется главными клетками фундальной части желудка в виде своего предшественника неактивного пепсиногена. Активация осуществляется под действием соляной кислоты и в результате аутокатализа. В процессе активации с N-конца пепсиногена отщепляется 42 аминокислотных остатка в виде полипептида. При этом полипептидная цепь укорачивается на 20 % и освобождается активный центр фермента.
Са»+
Пепсиноген + HCl (следы пепсина) ¾® пепсин + полипептид
(М.м. 42000) (М.м. 35000) (М.м. 7000)
Пепсин является эндопептидазой и действует на пептидные связи, в формировании которых участвуют ароматические аминокислоты (фенилаланин и тирозин). Пепсин легко расщепляет белки животного происхождения (казеин, миоглобин, миоген, миозин) и некоторые растительные белки, построенные в основном из моноаминодикарбоновых аминокислот (глиадин и глютелин злаковых).
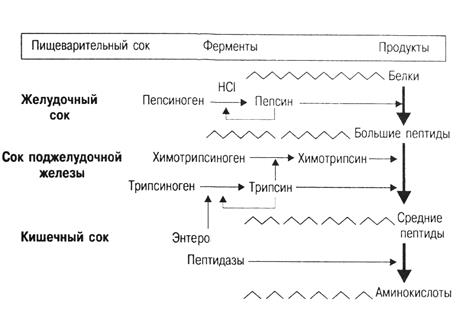
Рис. 15. Схема расщепления белков в желудочно-кишечном тракте.
Пепсин расщепляет большинство белков, за исключением кератинов шерсти, фиброинов шелка, муцинов слизи, овомукоидов, некоторых белков костей и хрящей.
Общая схема действия пепсина на белки имеет следующий вид:
Белки + nH2O + пепсин ¾® высокомолекулярные полипептиды + следы свободных аминокислот
Химозин (реннин, сычужный фермент) вырабатывается железами слизистой оболочки желудка молодых животных. Он секретируется в неактивной форме в виде прохимозина, который при рН 5,0 превращается в активную форму. Химозин превращает казеиноген молока в нерастворимую кальциевую соль казеина за счет отщепления пептида. Такой комплекс более продолжительное время задерживается в желудке, что способствует расщеплению его пепсином. Оптимум рН действия химозина лежит в пределах 3,5 – 5,0. У взрослых животных сычужный фермент малоактивен или отсутствует.
Белки и полипептиды из желудка поступают в тонкий отдел кишечника, где под действием ферментов пептидаз, синтезируемых поджелудочной железой и железистыми клетками тонкого отдела кишечника, подвергаются более глубокому гидролизу. В тонкий кишечник поступает панкреатический сок, содержащий неактивные предшественники пептидаз: трипсиноген, химотрипсиноген, прокарбоксипептидазы А и В и проэластазу.
Трипсин гидролизует примерно 1/3 пептидных связей в молекуле белка. Он синтезируется в поджелудочной железе в неактивной форме (в виде трипсиногена). Активация осуществляется в тонком отделе кишечника при участии фермента энтеропептидазы и ионов кальция в результате отщепления гексапептида с освобождением активного центра трипсина. В последующем трипсин катализирует превращение трипсиногена в активную форму.
Трипсиноген + НОН ¾¾¾¾¾® трипсин + гексапептид
(М.м. 27040) энтеропептидаза (М.м. 26680) (М.м. 360)
Трипсин гидролитически расщепляет как белки, не изменившиеся в желудке под влиянием пепсина, так и высокомолекулярные полипептиды, образовавшиеся в желудке в результате расщепления белков корма под действием пепсина. Оптимальное значение рН для действия пепсина 7,8 – 8,2.
Трипсин является эндопептидазой и расщепляет пептидные связи, образованные в основном карбоксильными группами диаминомонокарбоновых аминокислот (лизина и аргинина).
Общая схема действия трипсина следующая:
Белки (высокомолекулярные полипептиды) + nНОН ¾® низкомолекуклярные полипептиды + дипептиды + свободные аминокислоты
Химотрипсин образуется из химотрипсиногена. Его активирование происходит при помощи трипсина и химотрипсина.
Химотрипсин, как и трипсин, гидролизует белки и высокомолеклярные полипептиды, поступающие из желудка, до низкомолекулярных полипептидов, дипептидов и свободных аминокислот. Химотрипсин расщепляет связи более глубоко по сравнению с трипсином (гидролизу подвергается около половины пептидных связей). Химотрипсин гидролизует преимущественно те пептидные связи, в образовании которых участвуют карбоксильные группы фенилаланина, тирозина и триптофана.
Карбоксипептидазы А и В синтезируются в поджелудочной железе в неактивной форме, их активация осуществляется в тонком отделе кишечника при участии трипсина. Карбоксипептидаза А расщепляет пептидные связи с С-конца цепи (при наличии концевых ароматических аминокислот). Карбоксипептидаза В действует на пептиды, имеющие С-концевые участки аргинина или лизина.
В слизистой оболочке тонкого кишечника имеются аминопептидазы,расщепляющие пептидные связи с N-конца цепи (например, Мg2+-зависимая лейцинаминопептидаза).
Ди- и трипептиды расщепляются кишечными дипептидазами, которые проявляют определенную специфичность к аминокислотным остаткам.
Таким образом, под действием протеолитических ферментов желудка и тонкого кишечника кормовые белки распадаются до свободных аминокислот. Однако не все белки корма распадаются до конечных продуктов – аминокислот. Это может быть обусловлено наличием в кормовой смеси ингибиторов пептидаз. Например, соевые бобы содержат ингибитор трипсина. Интенсивность переваривания белков может тормозиться избытком жиров в рационе или слабой его гидролизуемостью под действием карбоксиэстераз поджелудочного и кишечного сока, что ведет к снижению коэффициента использования азотистых веществ корма.
