Мышечное расслабление Механизм расслабления. Роль АТФ-аз, АТФ
В норме прекращение сократительной активности и развитие состояния расслабления наступает вслед за исчезновением электрическоой активности в нервно-мышечном синапсе. Саркоплазматическая мембрана возвращается к потенциалу покоя (снаружи заряд более положительный, разница - 60 мв,). То же самое происходит во всей Т-тубулярной системе и мембране саркоплазматического ретикулума (СР). Затем саркоплазматический кальций закачивается обратно в цистерны СР посредством исключительно активного АТФ-зависимого кальциевого насоса. Са2+-АТФаза является одним из основных белков мембраны СР. За счет гидролиза каждой молекулы АТФ из саркоплазмы выводятся два иона кальция. Таким образом концентрация саркоплазматического кальция падает до 0,1 мкмоль и ниже, что в 50-100 раз меньше того уровня, который требуется для присоединения кальция к тропонину-С.
В мембране эндоплазматического ретикулума, в области цистерн, содержится большое количество гликопротеина - кальсеквестрина. Кальсеквестрин жадно связывает кальций, уменьшая его концентрацию в цистерне. Это благоприятствует аккумуляции кальция. Ещё одним местом накопления саркоплазматического кальция является митохондриальный матрикс. У митохондрий имеется активный кальциевый насос, работа которого зависит от хемиосмотического потенциала, формирующегося за счет транспорта электронов. В аэробных условиях этот насос использует энергию транспорта электронов для закачки кальция в митохондриальный матрикс. Этот процесс идет даже в ущерб синтезу АТФ.
Тетания и трупное окоченение. Ригорный комплекс
Тетания, состояние чрезмерного мышечного сокращения, иногда развивается при длительной, повторной и суммирующейся стимуляции мышц. Причиной является истощение АТФ и других высокоэнергетических фосфатов, которые помогают поддерживать нормальный уровень АТФ. К высокоэнергетическим фосфатам в данном случае относятся другие нуклеозид трифосфаты (НТФ), креатин фосфат (КФ) и АДФ (см. уравнения 5,6 и 7). Эти реакции катализируют нуклеозид дифосфокиназа, креатин киназа и аденилат киназа, соответственно.
НТФ + АТФ ® НДФ + АТФУравнение 5
КФ + АДФ ® Креатин + АТФУравнение 6
АДФ + АДФ ® АМФ + АТФУравнение 7
Тетаническая стимуляция приводит к нарастанию кальция в саркоплазме и уменьшению АТФ. В результате при сильном мышечном сокращении кальций связан с тропонином-С, но нет АТФ, достаточного для перекачки кальция в цистерны СР и разрыва актомиозиновых поперечных мостиков. Тогда митохондрии получают преимущественную возможность для закачки кальция в свой матрикс. Тем самым создаются условия для удаления кальция, связанного с тропонином-С; места связывания миозина на тонких нитях закрываются, и мышца переходит в расслабленное состояние. Однако отсутствие АТФ оставляет миозин в низкоэнергетическом конформационном состоянии. Поэтому новые циклы мышечной стимуляции хотя и приводят к сокращению мышц, но сила его невелика. Об этой физиологической реакции говорят, как о мышечном утомлении.
Смерть выравнивает все реакции. Одним из первых наступает ионное равновесие во всех отсеках организма из-за потери ионными насосами своих источников энергии. В мышцах это приводит к перемещению кальция из цистерн и извне клетки в саркоплазму. Там его концентрация достигает высокого уровня, что вызывает конформационные изменения в тропонин-тропомиозиновом комплексе. Эти изменения таковы, что места связывания на тонких нитях становятся доступны для миозина. Развивающаяся в результате некотролируемая сократительная активность ускоряет процесс истощения источников АТФ, где все или почти все молекулы миозина вовлечены в поперечно связанные актомиозиновые комплексы. Такое состояние развивается в мышцах вскоре после смерти. Оно обусловлено большим количеством поперечных связей между толстыми и тонкими нитями и известно как трупное окоченение.
Гладкие мышцы
Несмотря на то, что модель скольжения толстых и тонких нитей достаточно адекватно отражает механизм сокращения во всех мышечных группах, имеются значительные различия между поперечно-полосатой и гладкой мускулатурой. Это вытекает хотя бы из того факта, в гладких мышцах потеря тропонина не приводит к утрате сократительной способности, она продолжает регулироваться уровнем цитозольного кальция. Объяснение пришло позже, когда установили, что в регуляцию перемещения тропомиозина гладких мышц к - и от мест связывания миозина на тонких нитях вовлечен белок, связывающий Са2+/кальмодулин. Белок назвали кальдесмон. Было установлено, что он участвует в регуляции перемещения тропомиозина гладких мышц к - и от центров связывания миозина на тонких нитях.
В общих чертах, картина выглядит следующим образом. Увеличение уровня цитозольного кальция приводит к повышенному его связыванию с кальмодулином. В свою очередь, комплекс кальция с кальмодулином связывает кальдесмон. Тем самым кальдесмон отщепляется от своего места связывания на тонких нитях. Одновременно наблюдается изменение местоположения тропомиозина в спиральной бороздке F-актина и активируется актомиозиновая АТФ-аза. Когда количество кальция уменьшается, комплекс его с кальмодулином диссоциирует; кальдесмон отщепляется от этого комплекса и соединяется с тонкими нитями. Соответственно, ингибируется активность актомиозиновой АТФ-азы. В сущности, кальдесмон здесь выполняет функцию тропонина в качестве зависимого от кальция (Са2+/кальмодулина) регулятора местонахождения тропомиозина на тонких нитях.
Другой отличительной особенностью гладких мышц является наличие в составе миозина уникальной короткоцепочечной полипептидной цепи, получившей название «легкая цепь Р». Эта субъединица может находиться в фосфорилированном и дефосфорилированном состоянии. Присоединение к ней остатка фосфорной кислоты катализирует специальный фермент – киназа легкой цепи миозина, которая также зависит от комплекса Са2+/кальмодулин. В отсутствие этого комплекса гладкие мышцы неподвижны, киназа неактивна, а легкие Р-цепи нефосфорилированы. Повышение концентрации этого комплекса приводит к активации киназы легких цепей миозина, соответственно, к фосфорилированию легких Р-цепей и сокращению. Дело в том, что для сокращения гладких мышц необходимы фосфорилирование легких Р-цепей миозина и отщепление кальдесмона от тонких нитей. Цепь вышеперечисленных событий, причастных к сокращению гладких мышц, приведена на рис.17.12.
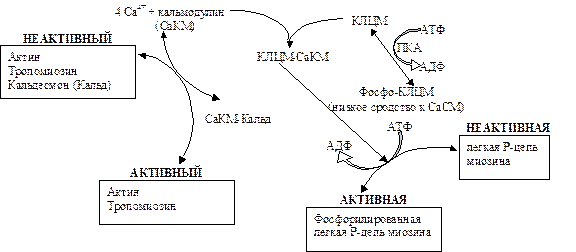
Рис.17.12.Молекулярный механизм сокращения гладких мышц
Увеличение концентрации Са2+ до 10-5 моля вызывает образование комплекса кальция с кальмодулином (СаКМ), который активирует тонкие нити за счет связывания кальдесмона (Кальд) и освобождая места связывания миозина на тонких нитях. СаКМ также связывает и активирует киназу легкой цепи миозина (КЛЦП). Активная киназа катализирует фосфорилирование легкой цепи-Р миозина, в результате активируется актомиозиновая АТФ-азная активность головок миозина. Связывание адреналина с b-адренорецепторами увеличивает количество цАМФ и, следовательно, активность зависимой от цАМФ протеинкиназы (ПКА). В результате снижается сродство МЛЦК к СаКМ, тем самым регулируется сила сокращений, вызванных увеличенным уровнем цитозольного кальция.
