Выделение аминазина из крови.
5—10 мл крови + 30—50 мл этилового спирта, подкисленного 10 % р-м щавелевой кислоты до рН = 2...3 à нагревают на кипящей водяной бане 10 мин à охлаждают à спиртовую вытяжку сливают и выпаривают досуха + 50 мл воды, нагретой до 40—60 °С à взбалтывают à фильтруют + 20 мл диэтилового эфира (2 раза) à взбалтывают 5—10 мин à отделяют эфирный слой à кислую водную фазу подщелачивают 50 %-м р-м гидроксида натрия до рН=13 и взбалтывают с 3—4 порциями диэтилового эфира (по 10 мл). Эфирные вытяжки соединяют и исследуют на наличие аминазина.
Выделение аминазина из мочи.
50—200 мл мочи + 25 % р-р серной кислоты до рН = 2...3 à нагревают на кипящей водяной бане 5 мин à охлаждают до комнатной температуры à жидкость взбалтывают 5—10 мин с диэтиловым эфиром по 50 мл (2 раза) à кислую водную фазу исследуют на наличие аминазина.
Предварительные пробы на наличие аминазина в моче.
1. К 1 мл мочи прибавляют 1 мл реактива, состоящего из 80 мл 10 %-го раствора серной кислоты и 20 мл 5 %-го раствора хлорида железа (III). При наличии аминазина и других производных фенотиазина в моче раствор приобретает розовато-лиловую окраску.
2. К 1 мл мочи прибавляют 1 мл реактива ФПН. Появление розовой окраски указывает на наличие аминазина или других производных фенотиазина в моче.
Предварительные испытания.
Качественные реакции:
· Реакция с концентрированной серной кислотой. Аминазин с концентрированной серной кислотой дает пурпурно-красную окраску.
· Реакция с концентрированной азотной кислотой. При взаимодействии аминазина с концентрированной азотной кислотой возникает пурпурно-фиолетовая окраска.
· Реакция с концентрированной соляной кислотой. Аминазин с концентрированной соляной кислотой дает розовато-фиолетовую, переходящую в красно-фиолетовую окраску.
· Реакция с реактивом Марки. Аминазин под влиянием реактива Марки приобретает пурпурную окраску.
· Реакция с реактивом Манделина. Аминазин с этим реактивом дает зеленую окраску, переходящую в пурпурную.
Обнаружение аминазина методом хроматографии.
НФ: силуфол
ПФ: бензол : диоксан : аммиак
Д: р-в Марки / HNO3 : СН5ОН
Количественное определение аминазина и его метаболитов.
1. Фотоколориметрическое определение основано на реакции с концентрированной серной кислотой. Фотометрирование проводят при λ = 508 нм в кювете 5,105; эталон сравнения – контроль реактивов. Расчет содержания аминазина и его метаболитов производится по калибровочному графику.
2. Спектрофотометрическое обнаружение. Спектрофотометрический метод основан на количественной оценке поглощения растворов токсикантов в ультрафиолетовой области. Ультрафиолетовый спектр снимается в диапазоне длин вол 220-400 нм на СФ-4, СФ-4А и др. при концентрации 10 мкг/мл в пересчете на основание.
Максимумы абсорбции неизмененного аминазина при λ = 254-255 нм (макс.) и λ = 300-305 нм (мин). Неизмененный аминазин обычно обнаруживается в желудке и желудочно-кишечном тракте и их содержимом. Основной метаболит – сульфоксид – имеет максимумы абсорбции при длинах волн 238-240, 273; 298 и 340 нм. Химико-токсикологическим анализом по описанной методике обнаруживается 53-60% аминазина, добавленного к органам. Граница обнаружения 0,2 мг, граница определения 0,5 мг аминазина в 100 г органов.
Дипразин
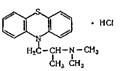 |
Дипразин (пипольфен, прометазин, протазии и др.) — белый кристаллический порошок, легкорастворимый в воде и этиловом спирте, хлороформе (1 : 2), почти не растворим в диэтиловом эфире.
Дипразин экстрагируется органическими растворителями из щелочной среды.
Дипразин имеет выраженную противогистаминную активность. Он обладает седативным действием, усиливает действие наркотических, снотворных и анальгезирующих средств. Дипразин применяется для лечения аллергических заболеваний, зудящих дерматозов, хореи, энцефалита и др.
Главным метаболитом дипразина является сульфоксид этого препарата. Часть дипразина в неизмененном виде выделяется с мочой. Кроме этого, с мочой выделяется и сульфоксид дипразина, который можно обнаружить в моче даже через 14 сут после приема указанного препарата.
Выделение из биологического материала (по Б. М. Саломатину).
100 г измельченного биологического материала + этиловый спирт, подкисленным 10% р-м щавелевой кислоты до рН = 2...3. à кислые спиртовые вытяжки на водяной бане (при 40 °С) упаривают до густоты сиропа à + 96° этиловым спиртом à фильтруют à выпаривают досуха + 100 мл воды (темп. 40—60 °С) à жидкость охлаждают и фильтруют à + 5 % р-р щавелевой кислоты до рН = 2...3 + диэтиловый эфир (по 50 мл 2 раза) + 50%-м р-м гидроксида натрия до рН = 13 + 4 порции диэтилового à объединенные эфирные вытяжки + 0,5 н р-р серной кислоты à водные вытяжки соединяют и нагревают 3 мин на водяной бане (темп. 50—60 °С) à кислые водные вытяжки используют для обнаружения.
Обнаружение дипразина
· Реакция с концентрированной серной кислотой. Дипразин с концентрированной серной кислотой дает пурпурно-красную окраску.
· Реакция с концентрированной азотной кислотой. При взаимодействии дипразина с концентрированной азотной кислотой появляется бледная пурпурно-красная окраска, переходящая в желтую.
· Реакция с концентрированной соляной кислотой. Дипразин с концентрированной соляной кислотой дает розовато-фиолетовую окраску, переходящую в пурпурно-фиолетовую.
· Реакция Витали — Морена.
· Реакция с реактивом Марки. Дипразин с реактивом Марки дает пурпурную окраску.
· Реакция с реактивом Манделина. Реактив Манделина с Дй-празином дает зеленую окраску, переходящую в пурпурную.
Обнаружении методом ТСХ
НФ: силуфол
ПФ: бензол : диоксан : аммиак
Д: р-в Марки / HNO3 : СН5ОН
