Графическое и динамическое моделирование реакций
Существует два взаимно дополняющих подхода в моделировании реакций: динамический и графический.
Динамическая модель отражает развитие процесса во времени. Основой модели является система дифференциальных уравнений. Для реакций первого, второго и третьего порядка системы линейны относительно кинетических коэффициентов и содержат, соответственно, линейные, квадратичные и кубические члены относительно концентраций. Таким образом, выше излагался именно динамический подход в моделировании реакций. Построение динамической модели в каждом конкретном случае может представлять трудности даже для вполне изученных реакций.
Графический подход использует аппарат теории графов, раздела топологии для описания сколь угодно сложных реакций и процессов. Основными преимуществами является наглядность описания стадийных переходов, полезная для классификации и облегчающая понимание процессов. Рассмотрим основные термины теории графов и её применение для кинетических расчетов в исследовании ферментативных процессов.
Метод графов в анализе кинетических схем
Центральное понятие теории графов- сам граф. Граф- совокупность точек (вершин) и соединяющих их линий, если линии имеют направления (ориентированы), то их называют дугами (ветвями); если не ориентированы, то их называют ребрами. Ребрам и дугам в кинетике приписываются численные значения, обычно равные константам скорости, в теории графов число характеризует вес ветви. Для анализа кинетической схемы выбирают одну из вершин графа в качестве базовой(базы), выбор базы произволен, но важен для простоты и правильности расчетов с помощью теории графов. Возможны ребра, начинающиеся и оканчивающиеся на одной и той же вершине; их называют петлями и граф с такими ребрами называют псевдографом. Путь графа- непрерывная совокупность ветвей в каком- либо направлении, при котором ни одна из вершин не встречается дважды. Граф может быть: связанным, если каждая его вершина связана хотя бы с одной другой вершиной; неориентированным, если каждое его ребро не ориентировано; ориентированным (орграфом), если каждое ребро ориентировано. Вершины связанные ребром называются смежными, в полном графе все вершины смежные. Если в графе присутствуют и ориентированные и неориентированные, то граф называют смешанным. Любой граф может быть превращен в ориентированный путем замены всех неориентированных ребер парой дуг соединяющих одни и те же вершины, но с противоположными направлениями; появление кратных ребер обуславливает использование названия мультиграф. Путь начинающийся и заканчивающийся на одной и той же вершине называют циклом, а граф, содержащий такой путь- циклическим, т.е. пара дуг образует цикл, а мультиграф- циклический. Связный граф, не содержащий циклов, называется деревом. Совокупность всех ветвей, проходящих через все вершины графа и ведущих к базе называется базовым деревом. Обычно в качестве базовой выбирают вершину, образующую наибольшее дерево. Сумма величин всех базовых деревьев, направленных к данной базе, называется определителем базы(базовым определителем графа). Для определения уравнения стационарной скорости реакции требуется вычисление всех базовых определителей графа. В расчетах базовых определителей важны следующие свойства:
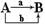 |
1. Кратные ветви складываются: граф эквивалентен графу 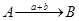 , т.е. путь (А®В) равен a+b.
, т.е. путь (А®В) равен a+b.
2. Ветви, направленные к одной базе перемножаются: для графа 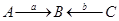 путь (А,С®В) равен ab.
путь (А,С®В) равен ab.
3. Путь графа равен произведению величин всех ветвей этого пути: для графа 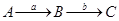 путь (А®С) равен ab.
путь (А®С) равен ab.
Стационарная скорость реакции с помощью метода графов вычисляется следующим образом
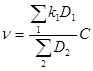 [Г1]
[Г1]
где D2- базовые определители всех состояний всех реагентов, кроме того, зависимость скорости превращения от концентрации которого изучается, D1- базовые определители всех состояний реагентов, приводящих к образованию продуктов, k1- константы скоростей стадий, приводящих к образованию продуктов, С- концентрация реагента, относительно которого получаются кинетические зависимости. Для ферментативных реакций D2- базовые определители всех состояний фермента, D1-базовые определители состояний фермента, приводящих к образованию продуктов, k1-константы стадий, приводящих к образованию продуктов, С- концентрация субстрата.
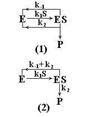 |
Используя выше приведенные свойства графов выведем уравнение стационарной кинетики для уравнения [Ф0]. Граф реакции запишем следующим образом (1) или, сложив параллельные ветви (k-1 и k2), в виде (2). Получим базовые определители Ds= k-1+k2 и Dr= Des= k1S (предшествует образованию продукта), константа стадии образования продукта k2. Стационарная скорость ферментативной реакции определяется следующим образом
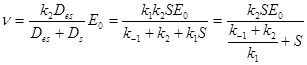 [Г2]
[Г2]
Полученное уравнение совпадает с уравнением [Ф4], что подтверждает применимость метода графов в кинетических исследованиях.
При фактическом изображении кинетических графов существует большая свобода в размещении вершин и в выборе соединяющих их ребер. Графы считаются одинаковыми и называются изоморфными, если существует взаимооднозначное отображение множество вершин одного на множество вершин другого при котором сохраняется смежность вершин.
Геометрически любая химическая реакция может быть представлена графом с n (n= 1, 2, ¼) вершинами, каждая из которых соответствует одному и только одному веществу. Исходные реагенты соединяются с конечными и промежуточными направленными дугами, которым приписывают вес равный константе соответствующего элементарного процесса. Отсутствие дуги или вес равный 0 означает отсутствие прямого взаимодействия.
Порядок реакции изображается количеством направленных дуг, если возникает продукт, который может быть выделен, то его изображают вершиной, если нет, то в точку реакции направляют количество стрелок, равное количеству исходных реагентов, а из неё выходят стрелки, количество которых равно количеству продуктов (т.е. пересечение без вершины соответствует неустойчивому промежуточному комплексу). Для мономолекулярных процессов константа точно соответствует весу данной дуги, для двух- и трех молекулярных процессов константа относится ко всей группе стрелок, которая изображает превращение.
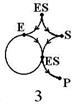
Для каталитических, в том числе и ферментативных, процессов характерно наличие циклов, т.к. вещество- катализатор после цикла реакций остается неизменным. Для изображения таких реакций часто применяется прием удвоения вершин и ребер. Для реакции [Ф0] граф примет вид (3).
 |
Особенности транспорта в биологических объектах
Для описания кинетики в гетерогенных системах появляется необходимость учитывать скорость подхода веществ к месту реакции. Биологические ткани имеют клеточное строение, т.е. с учетом ферментативного протекания большинства реакций бесспорно значение деталей проникновения реагентов на активный центр. Для веществ внутри организма существует несколько механизмов попадания внутрь клетки:
1. Простая диффузия- движение веществ против градиента в соответствии с законом Фика; таким образом вода из гипотонических растворов всасывается в клетки.
2. Облегченная диффузия- в клеточных стенках присутствуют участки, связывающие различные вещества. Связанные таким образом вещества легче попадают внутрь клеток, возможен эстафетный механизм, когда вещества проходят через клеточную стенку, переходя с участка на участок.
3. Активный транспорт- проходит с затратами энергии, запасенной в АТФ, и позволяет переносить вещества из областей низкой концентрации в области высокой. Таким образом осуществляется перенос ионов К+ и Са2+ внутрь клеток, несмотря на малые их концентрации вне клетки.
В целом, наряду с механизмами диффузии, обычными для химии, в биологии имеются пути создания и изменения концентраций, характерные только для нее. Поэтому при исследовании биохимических реакций необходимо учитывать все пути создания концентраций реагентов, т.к. кинетические уравнения очень чувствительны к точности измерения концентраций в системе (основным источником возможных ошибок на рис.3 может быть именно малый масштаб исходного графика и следующие из этого возможные ошибки оценки концентраций).
Приведенные сведения показывают важность в исследовании биологических процессов закономерностей химической кинетики, ознакомление с которыми составляет задачу настоящей работы.
