Локалізація ферментів у клітині
Зараз ферменти виявлено в усіх структурних компонентах клітини. Різновидність їх в тих чи інших органелах залежить в основному від функцій органел і природи хімічних процесів, які в них відбуваються. Так, у мітохондріях, де протікають аеробні процеси, що забезпечують клітину енергією, зосереджено всі ферменти і кофактори
дихального ланцюга, а також ферменти окислювального фосфорилю-вання, які беруть участь в утворенні АТФ. У цих структурних компонентах клітини локалізовано також ферменти циклу ди- і трикарбоно-вих кислот та ферменти ^-окислення жирних кислот.
Ферменти циклу утворення сечовини зосереджено в різних орга-нелах. Так, орнітин (карбамоїлтрансфераза) і більшу частину карба-маткінази зосереджено в мітохоидріях, а два інших ферменти цього циклу (аргініносукцинат-ліаза та аргініносукцинат-синтетаза) знаходяться в цитоплазмі. Для завершення циклу, очевидно, має місце зустрічний транспорт орнітину і цитруліну крізь мембрану мітохондрій.
Досить важливим компонентом клітини є ядро. В ньому відбувається синтез різних нуклеотидів і окремих видів нуклеїнових кислот. Вважають, що в ядрі зосереджені такі ферменти, як НМФ-адеиіліл-трансфераза, ДНК-полімераза І, ДНК-полімераза II тощо. У рибосомах зосереджено ферменти, які каталізують процеси синтезу білка. В них виявлено також ферменти, що. беруть участь у синтезі нуклеїнових кислот. Різні ферменти класу гідролаз локалізовані переважно в лізосо,мах, де відбуваються процеси деструкції органічних сполук до тих структурних одиниць, з яких вони побудовані. Важливою функцією лізосом є постачання ферментів для внутрішньо- і позаклітинного використання.
Цілий, ряд ферментів з відповідними структурами клітини не зв'язаний, а перебуває в розчиненому стані в цитоплазмі. До таких ферментів належать ферменти гліколізу, біосинтезу ліпідів, вуглеводів, амінокислот та їй.
Отже, в клітинах організму має місце відповідна локалізація ферментів у певних її структурах, в яких відбуваються реакції. Необхідно відмітити, що всі біохімічні реакції і процеси, які відбуваються в клітині, скоординовані між собою. Це забезпечує нормальну життєдіяльність різних органів і тканин, а також організму в цілому.
ВИКОРИСТАННЯ ФЕРМЕНТІВ
Ферменти широко використовують у багатьох галузях народного господарства, медицині. Так, в харчовій промисловості при випіканні хліба використовують ферментні препарати, які значно поліпшують його якість і аромат. Крім того, прискорюється визрівання тіста і значно зменшуються витрати цукру на виготовлення булочних виробів. Ферменти, які спричиняють молочнокисле бродіння, застосовують при виготовленні молочних продуктів — кефіру, ряжанки і простокваші. Такий фермент, як хімозин (виділяють із слизової оболонки сичуга), зумовлює зсідання білків молока і використовується в сироварінні. У м'ясній промисловості застосовують протеолітичні Ферменти, які частково розщеплюють білки і прискорюють дозрівання м'яса: роблять його більш м'яким і ніжним, поліпшують смак, аро-
мат, підвищують його соковитість. З такого м'яса виготовляють високоякісні продукти: напівфабрикати, ковбаси, консерви тощо. Процес дозрівання м'яса в звичайних умовах досить тривалий, наприклад, для дозрівання яловичини необхідно витримати її 10—14 діб при температурі 2—4 °С. При обробці такого м'яса протеолітичними ферментами дозрівання його скорочується до 1—2 діб.
Недавно розроблено промисловий метод одержання ферменту глюкозооксидази. Цей фермент застосовують як антиокислювач при зберіганні м'яса, фруктових соків та інших продуктів, що швидко псуються.
Різні види ферменту амілази використовують у пивоварінні і при виробництві спирту. Так, застосування ферментних препаратів у пивоварінні дає можливість зекономити 165 г ячменю при виробництві кожного декалітра пива.
Перспективним є використання ферменту пектинази. Цей фермент розщеплює пектинові речовини в стінках клітини і цим самим сприяє підвищенню виходу соків із плодів і ягід на 15—20 %.
Останнім часом ферменти почали застосовувати і в хімічній промисловості для перебігу таких реакцій, як відновлення, окислення, дегідратація, декарбоксилювання тощо. Ферменти часто використовують для виділення ізомерів амінокислот L- або D-ряду із їх рацемічних сумішей, які добувають при хімічному синтезі амінокислот.
Ферменти та їх препарати використовують також у тваринництві з метою підвищення продуктивності тварин. Так, наприклад, використання пепсину для підкормки поросят віком 2—4 місяці (3 г на одну голову) підвищує їх середньодобовий приріст на 18 % і знижує використання кормів на одиницю приросту на 15 %. Для підкормки телят, поросят і ягнят використовують різні ферментні препарати (ава-морін, орізин, терризин), які мають протеолітичну та амілолітичну дію. Вони сприяють підвищенню продуктивності тварин на 8—15 %. Вважають, що ферменти доцільно згодовувати лише молодим тваринам, в яких, порівняно з дорослими, ферментативні системи, що здійснюють травлення в шлунку, розвинені недостатньо.
В останні роки ферментні препарати успішно застосовують і при силосуванні різних кормів, в результаті чого поліпшується хімічний склад і біологічна цінність силосованих кормів, засвоєння їх організмом тварин.
Ферменти як лікувальні препарати більш широко почали застосовувати в медицині. Так, при лікуванні захворювань травного каналу застосовують пепсин, трипсин та інші ферменти. У лікувальній практиці використовуються також окремі ферменти — лізоцим і гіалуро-нідаза, що мають здатність гідролізу вати складні полісахариди. Ці ферменти підвищують проникність тканин і клітинних мембран, що зумовлює їх протизапальну дію. Крім того, лізоцим руйнує оболонки окремих хвороботворних бактерій і використовується для лікування
деяких інфекційних захворювань. Зараз нагромаджено значний клінічний досвід щодо успішного використання ферментів (протеїназ) в хірургічній практиці для обробки ран, виразок, що довго не загоюються, лікування остеомієлітів та ряду інших захворювань, які важко піддаються звичайному лікуванню. Тепер почали ефективно використовувати ферменти для розсмоктування згустків крові (тром* бів), які утворюються в середині кровоносних судин. З цією метою застосовують фібринолізип (плазмін), стрептокіназу, стрептазу, уро-кіназу тощо.
Новою перспективною галуззю медичної ензимології є використання іммобілізованих ферментів, тобто ферментів, які прикріплені до відповідних нерозчинних речовин (носіїв), що захищають їх від руйнування. Такими носіями часто є природні або синтетичні високомо-лекулярні сполуки — білки, полісахариди, різні синтетичні полімери. Іммобілізовані ферменти, зберігаючи катал;тичну активність, набувають підвищену стабільність, більш тривалий час діють в організмі і виявляють нижчу антигенність. Зараз уже створені і успішно використовуються іммобілізовані фібринолітичні ферменти (стреп-тодеказа та ін.) для лікування різних тромбозів.
Важливе значення мають ферменти в діагностиці різних захворювань. Підвищення або зниження активності ферментів крові порівняно з нормою є важливим показником патологічних змін в організмі. Цінність ферментативної діагностики — висока специфічність і можливість визначення відхилень на ранніх стадіях захворювання.
Запитання і вправи для самоконтролю
1. Які речовини називаються ферментами?
2. Схарактеризуйте роль ферментів у процесах життєдіяльності організмів.
3. Схарактеризуйте особливості дії ферментів як біокаталізаторів.
4. Яка хімічна природа ферментів?
5. Наведіть основні докази білкової природи ферментів.
6. Що таке прості ферменти? Наведіть приклади.
7. Яка будова складних ферментів?
в. Дайте визначення поняттям: кофактор, простетична група, активатор.
9. Яка роль коферменту і кофактора в процесі біокаталізу?
10. Наведіть приклади основних видів коферментів ферментних систем.
П. Напишіть структурні формули сполук, які виконують функції простетич-них груп складних ферментів.
12. Що таке активний центр ферментів-протеїнів і ферментів-протеїдів?
13. Дайте характеристику алостеричного центру ферментів.
14. Поясніть механізм дії ферментів.
15. Назвіть характерні властивості ферментів.
16. Як впливає на активпість ферментів температура і рН середовища?
17. Що таке специфічність дії ферментів? Види специфічності та їх характе-
18. Дайте характеристику активаторів та інгібіторів ферментів. Наведіть при-
19. Назвіть принципи номенклатури і класифікації ферментів.
20. 
 Що таке шифр ферментів? Поясніть це на прикладах.
Що таке шифр ферментів? Поясніть це на прикладах.
21. Перерахуйте класи ферментів та схарактеризуйте їх.
22. Напишіть хімізм реакцій розщеплення субстрату під впливом а-, Р- і у-амілази.
23. Напишіть схему ферментативного розщеплення мальтози, визначіть клас ферменту.
24. Як діє а-амілаза на такий субстрат, як сахароза? Відповідь поясніть.
РОЗДІЛ V. ХІМІЯ ВУГЛЕВОДІВ
Вуглеводи є невід'ємною складовою частиною всіх клітин і тканин живих організмів.
В організмі людини і тварин вуглеводи виконують цілий комплекс життєво необхідних функцій. Найважливішими з них є енергетична, структурна і захисна. Деякі вуглеводи (пентози, гексози) використовуються в синтез Г біологічно активних речовин — нуклеотидних ко-ферментів, нуклеїнових кислот та деяких інших.
Термін «вуглеводи» вперше був запропонований у 1844 p. K. Шмід- j том. Ці речовини формально за складом можна розглядати як сполуки вуглецю з водою С;і (Н20)т. Тепер відомо багато речовин, які відносять до вуглеводів, але вони не відповідають наведеній вище формулі. Хоч назва «вуглеводи» і не повністю відповідає хімічному складу речовин, які до них відносять, вона збереглася до цього часу і стала тривіальною. Вуглеводи ще часто називають сахарами.
Відповідно до існуючої класифікації всі вуглеводи поділяють на три групи: моносахариди, олігосахариди і полісахариди.
МОНОСАХАРИДИ
Моносахариди — це вуглеводи, які не піддаються пдг^аллзуз^іво-ренням більш, простих^ сполук. їм відповідає загальнаГформула СПН2А, Де п = 4, 5, 6, 7, 8 і т. д.
Моносахариди поділяють на альдози (містять альдегідну групу) і кетози (містять кетогрупу). Залежно від числа атомів вуглецю в ланцюзі моносахаридів розрізняють тетрози С4Н804, пентози С5Н10О6, гексози С6Н1206, гептози С7Н1407 і> т. д. Найбільш поширені альдози і кетози, що належать до пентоз (рибоза, дезоксирибоза, ксилоза, і арабіноза) і гексоз (глюкоза, маноза, галактоза, фруктоза).
Стереоізомерія моносахаридів. Просторова ізомерія моносахаридів пов'язана з асиметричними атомами вуглецю у складі їх молекул. Загальна кількість стереоізомерів N, якщо в молекулі є п асиметричних С-атомів, виражається формулою N = 2п. В альдогексоз, наприклад, їх чотири, тому кількість оптичних ізомерів для них N = (24) =»
s= 16, або 8 пар оптичних антиподів. Антиподи кожної пари відрізняються знаком обертання площини поляризації.
Слід зазначити, що знак обертання — ознака нестійка. Деякі речовини можуть змінювати його залежно від умов поляриметричного вимірювання (температури, розчинника, концентрації), а також у процесі хімічних перетворень. Тому при складанні назв оптичних ізомерів слід зазначати не тільки знак обертання, а й просторову конфігурацію молекул, оскільки вона часто не збігається із знаком обертання.
Для позначення конфігурації оптичних ізомерів часто порівнюють їх просторову будову з конфігурацією стандартної оптично активної сполуки — «ключа». Для моносахаридів таким «ключем» є гліцериновий альдегід, що має два оптичних ізомери — D-гліцерино-вий і L-гліцериновий альдегіди:
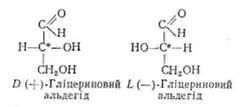
Моносахариди, в яких розміщення водню і гідроксилу біля останнього (найбільш віддаленого від альдегідної чи кетогрупи) асиметричного С-атома таке саме, як у D (-|-)-гліцеринового альдегіду, відносять до D-ряду, а якщо воно таке, як у L (—)-гліцеринового альдегіду, то до L-ряду. Наприклад:
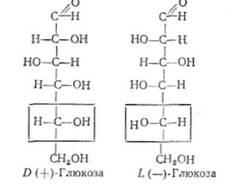
природі поширені в основному D-ізомери моносахаридів, серед их крім D (-і-)-глюкози найчастіше трапляються такі альдо- і ке-
тогексози:
альдопентоз:
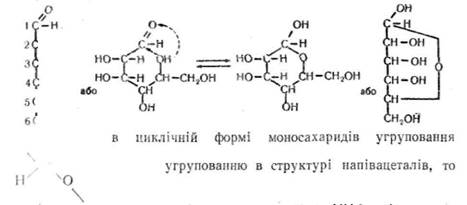
У розчинах 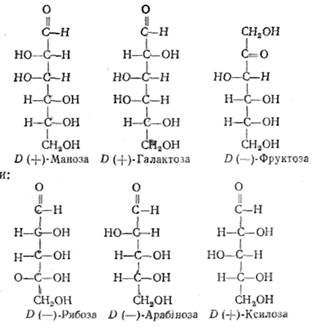 моносахариди перебувають одночасно в ациклічній (ланцюговій) і циклічній формах з шестичленним (піранозним) або п'ятичленним (фуранозним) кільцем. Обидві форми є структурними ізомерами — таутомерами, оскільки перебувають у стані рівноваги:
моносахариди перебувають одночасно в ациклічній (ланцюговій) і циклічній формах з шестичленним (піранозним) або п'ятичленним (фуранозним) кільцем. Обидві форми є структурними ізомерами — таутомерами, оскільки перебувають у стані рівноваги:
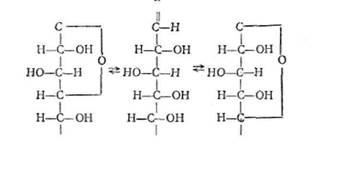 |
| сн2он сн2он сн2он фуранозна форма Ациклічна форма Піранозна форма D- глюкози D-глюкози D-глюкози Рівновага сильно зміщена в бік циклічної форми, у вигляді якої моносахариди вступають у реакції конденсації при утворенні полісахаридів, нуклеїнових кислот, глікозидів та інших сполук. У кристалічному стані моносахариди мають циклічну форму. |
нх/он о нх/он
 |
Циклічна ({юрма утворюється внаслідок внутрішньомолекулярної взаємодії карбонільної групи з просторово найближче розміщеною спиртовою групою:
н-он
н-он
н-он
[н-он
;н?он
Оскільки /ОН
'С\ аналогічне
цю форму називають ще напівацетальною, а групу ОН біля С, — напів-ацетальиим гідроксилом. На відміну від інших груп ОН, у молекулах моносахаридів напівацетальнпй гідроксил має підвищену хімічну активність. Продукти заміщення водню на алкільний залишок або складніший замісник називаються ацеталями, або глікозидами, звідки ще одна назва цього гідроксилу — глікозидний гідроксил. Глікозиди — ефіролодібні сполуки, які легко піддаються кислотному гідролізу, але не можуть перетворюватися на ациклічну форму (альдегідну чи кетонну).
З утворенням циклу в молекулах моносахаридів з'являється новий асиметричний С-атом (Q), внаслідок чого число оптичних ізомерів подвоюється. Так, для альдогексоз їх буде не 16, а 32. Це пояснюється різним просторовим розміщенням напівацетального гідроксилу і водню, які зв'язані з Сгатомом. З'являються дві ізомерні модифікації: а-форма (напівацетальний гідроксил розміщений з того самого боку, що й ОН-група, біля останнього асиметричного С-атома) і р-форма (розміщення напівацетального гідроксилу протилежне). Наприклад:
О
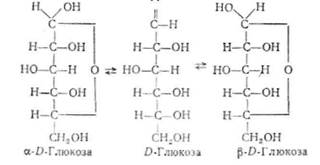
Відрізняючись між собою розчинністю і величиною кута обертання площини поляризації світла, сс- і 0-форми можуть переходити одна в одну. Це найкраще спостерігати у свіжоприготовлених розчинах моносахаридів, наприклад, глюкози, яка в кристалічному стані має иапівацетальну а-форму і кут питомого обертання -f-112 °С. У свіжо-приготовленому водному розчині глюкози кут питомого обертання площини поляризації поступово зменшується, поки не досягне величини +52,5°. Це явище називається мутаротацією (від лат. muto — змінюю і rotatio — обертання). Воно спричинюється частковим переходом a-D-глюкози в p-D-глюкозу, кут питомого обертання якої 4- 19,3°.
Явище мутаротації — один із доказів наявності циклічної (напів-ацетальної) форми моносахаридів. її існування підтверджується ще й тим, що моносахариди дають не всі реакції, характерні для альдегідів або кетонів.
До цього часу користувалися проекційними формулами, запропонованими Е. Фішером, О. А. Коллі, Б. Толленсом. Ці формули не дають повного уявлення про просторове розміщення всіх частин молекули моносахариду. Щоб передати просторову конфігурацію ]
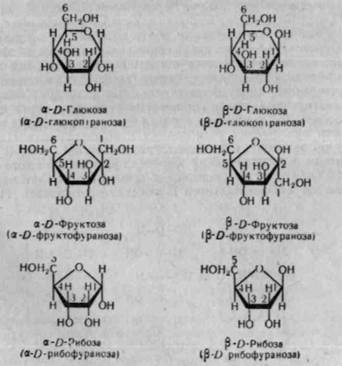
моносахариду, англійський дослідник Н. Хеуорс запропонував для циклічних структур моносахаридів перспективні формули. В них атоми й атомні групи, розміщені в проекційних формулах праворуч, зображують знизу площини кільця, а розміщені ліворуч — зверху площини кільця. Атоми вуглецю, що утворюють кільце, часто не пишуть. Н. Хеуорс також запропонував називати моносахариди з шестичленним кільцем піранозами, а з п'ятичленним — фуранозами (назви походять від назв кисневмісних гетероциклічних сполук — фурану і пірану) з префіксом від назви моносахариду. Для прикладу наведемо циклічні формули деяких гексоз і пентоз та їх назви (див. с 212). Слід зазначити, що проекційні формули Н. Хеуорса, зокрема гексоз, не відображають їхньої справжньої конформації. Дослідженнями Рівса та інших авторів встановлено, що піранозне кільце, подібно до циклогексану, може набувати конформацію у формі крісла або ванни: 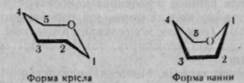
Конформація у формі крісла більш стійка, тому вона характерна для більшості природних моносахаридів:
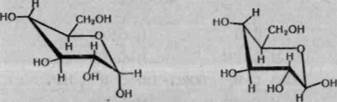
а-/>глюкоза (З-О-глюкоза
Способи добування.Головним джерелом добування моносахаридів є природна сировина. Піддаючи кислотному або ферментативному гідролізу ди- і полісахариди, вилучені з неї, добувають моносахариди!
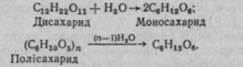
Серед синтетичних способів відома альдольна конденсація формальдегіду. Цим способом О. М. Бутлеров у 1861 р. добув першу саха-
2J3
 ристу речовину, яку назвав метиленітан. Е. Фішер, повторивши дослід О. М. Бутлерова, встановив, що метиленітан — це суміш моносахаридів:
ристу речовину, яку назвав метиленітан. Е. Фішер, повторивши дослід О. М. Бутлерова, встановив, що метиленітан — це суміш моносахаридів:
 |
V ~ Н-С-Н + Н-С-Н + Н-С-Н + Н-С-Н + H-C<f u Ca(0"'' ■»
н/ І І ІО І II І II ! хн
о«-.. !- о*-....... : о*-......... ■ о<-........ ■'• о*-......... ■•
-+ CH,-CH-CH-CH-CH-C<f„
І І І І І Хн
он он он он он
Гексоза
Фізико-хімічні властивості.Моносахариди — безбарвні кристалічні солодкі на смак речовини, добре розчинні у воді. їх розчини мають нейтральну реакцію.
Як зазначалося раніше, в розчинах моносахариди існують у вигляді циклічної та ациклічної форм, які перебувають між собою у рухомій рівновазі. Тому для моносахаридів властиві реакції як багатоатомного альдо- або кетоспирту, так іреакції циклічної напів-ацетальної форми.
Окислення моносахаридів.Моносахариди легко піддаються окисленню. При цьому утворюються відповідні кислоти. Так, при окисленні кожної з альдогексоз утворюються три різних кислоти. Наприклад, при окисленні альдегідної групи глюкози утворюється одноосновна карбонова кислота, яку називають глюконовою:
 |
О
II
с—н соон
І І
н-с-он н-с-он
НО-С-Н + НОВг т* НО—С—Н + НВг.
Н-С-ОН Н-С—ОН
І
-он н—с—он
сн,он сн2он
D-Глюкоза D-Глюконова кислота
При енергійному окисленні глюкози, наприклад концентрованою азотною кислотою, утворюється двохосновна карбонова кислота — сахарна (див. с 215).
При окисленні лише первинної спиртової групи утворюється мо-нокарбонова кислота, яку називають глюкуроновою. Взагалі гексу-ронові кислоти відіграють в організмі важливу роль. Вони входять до складу деяких полісахаридів і глікопротсїдів. Велику кількість гексуронових кислот знайдено в лейкоцитах і тромбоцитах крові!
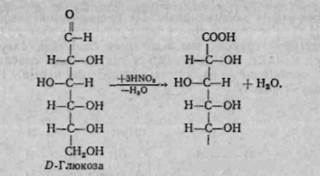 |
соон
D-Сахарна кислота
Відновлення моносахаридів. При відновленні альдегідних і ке-тонних груп гексоз утворюються відповідні спирти. Наприклад, при відновленні глюкози утворюється спирт сорбіт, манози — маніт, а при відновленні фруктози утворюється два стереоізомери — сорбіт і маніт:
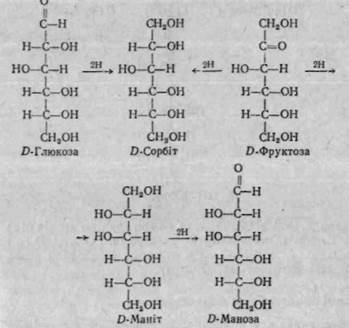
Ці спирти виявлені в окремих органах і тканинах організму. Так, сорбіт і дульцит утворюються із гексоз в плаценті і кришталику ока. Крім того, сорбіт міститься в багатьох фруктах і овочах, його знайдено також у морських водоростях.
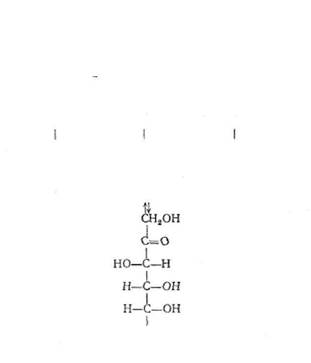
Епімеризація моносахаридів. Це процес зміни конфігурації груп Н і ОН біля асиметричного атома вуглецю, зв'язаного безпосередньо з альдегідною групою, внаслідок чого одні моносахариди перетворюються на інші. Він здійснюється під впливом слабких основ, а в живих організмах — за участю певних ферментів. Візьмемо для прикладу глюкозу:
 |
О О
II II
с—н снон с—н
І II І
н—с-он с—он но—с— н
І ІЛ 1
НО—С— Н *і НО-С—Н £=; НО-С-Н
І І І
Н-С—ОН Н—С-ОН Н—С—ОН
І І І
Н—G—ОН Н—С—ОН Н—С—ОН
. сн2он сн2он сн,он
D (+)-Тлюкоза Енольна D (-Ь)-Маноза
форма
Ft
СН2ОН D (—)-Фруктоза
Моносахариди, які відрізняються конфігурацією атомів біля асиметричного Gj-атома, називаються епімерами. Отже, D (+)-глюкоза і D (+)-маноза — епімери, які в лужному середовищі через енольну форму перетворюються на фруктозу.
