Генные болезни
Генные болезни встречаются чаще, чем хромосомные. Диагностика этих заболеваний обычно начинается с анализа клинических и биохимических данных, родословной пробанда, типа наследования. Моногенные болезни могут иметь аутосомно-доминантный, аутосомно-рецессивный и Х-сцепленный типы наследования.
При аутосомно - доминантном типе наследования патологический признак встречается в каждом поколении родословной и распределение между больными и здоровыми часто составляет 50:50, но вероятность может быть 100, 75 %. Однако пенетрантность патологических проявлений почти всегда ниже 100 %. Клинические проявления заболеваний и их выраженность могут быть различными не только между семьями, но и внутри одной семьи. Кроме того, клинические признаки могут появиться не сразу после рождения, а спустя много лет.
При аутосомно-рецессивном типе наследованияправильному анализу способствуют указания на родственный брак (двоюродный брат и сестра), данные биохимических исследований дефектов обмена веществ (выявление энзимопатий). Научной группой ВОЗ разработана и рекомендована к практическому применению следующая классификация наследственных заболеваний обмена веществ:
1) наследственные нарушения обмена аминокислот (фенилкетонурия и др);
2) наследственные нарушения обмена углеводов (гликогеновая болезнь галактоземия и др.);
3) наследственные нарушения обмена липидов (болезни Ниманна-Пика, болезнь Гоше и др.);
4) наследственные нарушения обмена стероидов (адреногенитальный синдром и др.);
5) наследственные нарушения обмена пуринов и пиримидинов (синдром Леша—Найхана и др.);
6) наследственные нарушения обмена соединительной ткани (мукополисахаридозы, синдром Марфана и др.);
7) наследственные нарушения гема- и порфирина (гемоглобинопатии и др);
8) наследственные нарушения обмена в эритроцитах (анемия Минковского—Шоффара и др.);
9) наследственные аномалии обмена металлов (болезнь Коновалова—Вильсона и др.);
10) наследственные нарушения обмена билирубина (синдром Криглера-Найяра и др.);
11) наследственные нарушения всасывания в пищеварительном тракте (муковисцидоз, целиакия, непереносимость лактозы и др.).
Рассмотрим наиболее часто встречающиеся ферментопатии, возникающие в результате генных мутаций.
ЗАБОЛЕВАНИЯ, СВЯЗАННЫЕ С РАССТРОЙСТВОМ АМИНОКИСЛОТНОГО ОБМЕНА
Фенилкетонурия (ФКУ, фенилпировиноградная олигофрения, болезнь Феллинга). Это заболевание обусловлено биохимическим дефектом превращения аминокислоты фенилаланина. Тип наследования аутосомно-рецессивный. Больные являются гомозиготами по гену фенилкетонурии, а родители гетерозиготами. Биохимический дефект состоит в ферментном (энзимном) блоке нормального превращения фенилаланина в аминокислоту тирозин из-за недостаточности ферменга фенилаланингидроксилазы. Количество фенилаланина в организме накапливается и концентрация его в крови увеличивается в 10—100 раз. Далее он превращается в фенилпировиноградную кислоту, являющуюся нейротропным ядом.
Накопление фенилаланина в организме идет постепенно, и клиническая картина развивается медленно. В первом полугодии жизни у ребенка бывают срыгивания, могут развиваться дерматиты и судорожные припадки. Судорожный синдром развивается по типу малой эпилепсии. В последующем соматическое развитие ребенка мало страдает, но психическое развитие, моторика все больше отстают или деградируют. Только 0,5 % больных сохраняют нормальный интеллект. В характере выявляется импульсивность, резкая возбудимость, склонность к агрессии.
Почти все дети блондины с голубыми глазами. С мочой и потом выделяются продукты обмена фенилаланина (фенилуксусная кислота) и от ребенка исходит неприятный запах («мышиный», «волчий», «затхлый»). Частота этого заболевания составляет 1 на 5600 новорожденных.
Исключение из питания фенилаланина с первых месяцев жизни способствует нормальному развитию ребенка. В настоящее время все новорожденные обследуются на уровень фенилаланина в крови: для этого несколько капель крови на фильтровальной бумаге посылают в лабораторию, где с помощью хроматографического метода определяют содержание данной аминокислоты.
Реже используется проба Феллинга: к 2—5 мл свежей мочи ребенка добавляют 10 капель 10 % раствора треххлористого железа. Появление сине-зеленого окрашивания свидетельствует о наличии заболевания и ребенок должен быть обследован количественными методами для установления окончательного диагноза.
ЗАБОЛЕВАНИЯ, СВЯЗАННЫЕ С НАРУШЕНИЕМ ОБМЕНА УГЛЕВОДОВ
Одной из основных частей пищи человека являются углеводы, которые выполняют энергетическую и структурную функции и являются составными частями некоторых биологически активных веществ (ферментов, гормонов, иммунных тел), мукополисахаридов. Основным углеводом пищи для детей грудного возраста является лактоза, а в последующем — крахмал.
Представителем в нарушении межуточного обмена углеводов является гликогеновая болезнь.
Характерной особенностью этого заболевания является нарушение энзимного звена в сложной цепи процессов, связанных с синтезом и разложением гликогена (животного крахмала). В норме образующийся из глюкозы гликоген при голодании должен снова превратиться в глюкозу и только в этом виде организм человека может использовать углеводы для других целей. Различают несколько типов гликогенозов.
Первый типгликогеноза — гепаторенальный, или болезнь Г и р к е. При этом заболевании накопившийся гликоген в печени и почках не может обратно превратиться в глюкозу и в организме развивается гипогликемия, так как в печени отсутствует фермент глюкозо-6-фосфатаза, которая играет важную роль в регуляции уровня глюкозы в крови. Наследуется заболевание по аутосомно-рецессивному типу.
В различные возрастные периоды клиническая картина болезни Гирке неодинакова.
В период новорожденности основными симптомами являются гипогликемические судороги и гепатомегалия. Задержка роста начинает отмечаться с 1-го года жизни. Характерен внешний вид больных: большая голова, «кукольное» лидо, короткая шея, выступающий живот (рис. 13). Уровень глюкозы в крови почти всегда ниже нормы, а липидов и молочной кислоты увеличен. На почве гипогликемии отмечаются обморочные состояния или судороги. Умственное развитие почти не изменяется, половое развитие задерживается. В крови повышается уровень мочевой кислоты и после пубертатного периода нередко наблюдаются признаки подагры.
При нагрузке глюкозой отмечается либо нормальная гликемическая кривая, либо диабетическая, когда уровень сахара в крови к 90—120 мин не приходит к исходному уровню и имеется высокий подъем. При введении адреналина, уровень глюкозы в крови увеличивается незначительно. Диагноз подтверждают после исследования биопсийного материала печени.
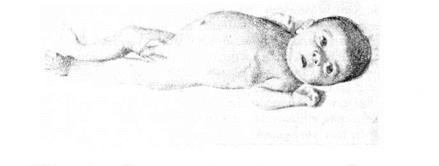
Рис. 13 Внешний вид страдающего гликогенозом первого типа (большая голова, короткая шея, «кукольное лицо», выступающий живот)
В лечебном плане большое значение уделяют диетотерапии. Частоту приемов пищи необходимо увеличить для предупреждения выраженной гипогликемии. В этих же целях повышают количество углеводов в диете. Жир ограничивают, белки назначают в соответствии с возрастной нормой. Лечение глюкагоном несколько улучшает прогноз заболевания.
Второй типгликогеноза, или болезнь Помпе, самый неблагоприятный. Его называют генерализованным, так как накопление гликогена происходит не только в печени, но и в скелетных мышцах, миокарде, легких, селезенке, надпочечниках, стенках сосудов, нейронах.
У новорожденных детей размеры сердца нормальные. Спустя 1—2 месяца у ребенка появляется мышечная слабость, теряются уже имеющиеся двигательные навыки. При кормлении и плаче отмечается цианоз. В это время выявляются кардиомегалия и макроглоссия. Сухожильные рефлексы исчезают, но плотность мышц остается нормальной. Накопившийся секрет в дыхательных путях приводит к затяжному течению пневмонии, а затем и к гибели больного.
Диагностика заболевания возможна еще до рождения ребенка. Для этого определяют активность специфических ферментов в амниотической жидкости и ее клетках (определение кислой а-1,4-глюкозидазы).
Третий, четвертый, пятый, шестойи другие типы гликогеноза напоминают клиническую картину первого типа и без биохимических исследований дифференциальная диагностика затруднительна.
Галактоземия. Это заболевание характеризуется накоплением в крови галактозы и проявляется отставанием в физическом и умственном развитии, тяжелым поражением печени, нервной системы, глаз и других органов. Наследуется галактоземия по аутосомно-рецессивному типу, частота патологии составляет 1 из 16000.
Галактоза является составной частью молочного сахара лактозы, при гидролизе которой в пищеварительном тракте образуются глюкоза и галактоза Галактоза тормозит всасывание глюкозы и этим создает углеводную среду в кишечнике. Она необходима для миелинизации нервных волокон. Однако избыточные ее количества для организма нецелесообразны, и поэтому она превращается в глюкозу с помощью фермента галактоза- 1-фосфат-уридил-трансферазы. При низкой активности этого фермента происходит накопление галактоза-1-фосфата, который оказывает токсическое действие на функции печени, мозга, хрусталик глаза.
Начало заболевания может проявляться с первых дней жизни расстройствами пищеварения, интоксикацией (понос, рвота, обезвоживание), развитием гипотрофии. Печень увеличивается, при пальпации она плотная, появляется желтуха, нарастают признаки печеночной недостаточности. Обнаруживается помутнение хрусталика глаза (катаракта). При тяжелом течении и без лечения дети погибают на первом году жизни, а при вскрытии обнаруживают цирроз печени. У выживших отмечается резкое отставание психомоторного развития, гепатомегалия, катаракта. Наиболее точным методом диагностики галактоземии является исследование в эритроцитах ферментов галактоза-1-фосфата и галактоза- 1-фосфатуридил-трансферазы, галактозы в крови и моче, где уровни ее увеличены.
Исключение из пищи молока (источника галактозы) дает возможность нормально развиваться больному ребенку.
НАСЛЕДСТВЕННЫЕ ЗАБОЛЕВАНИЯ, СВЯЗАННЫЕ С НАРУШЕНИЕМ ЛИПИДНОГО ОБМЕНА
В группу липидов входят триглицериды, холестерол (холестерин), эфиры холестерола, фосфолипиды, сфинголипиды, свободные или неэстерифицированные жирные кислоты (НЭЖК) и др.
Нарушение обмена липидов может происходить на уровне расщепления, всасывания, транспорта, а также при межуточном обмене. Исследования показали, что можно выделить два основных типа наследственных нарушений обмена липидов:
1) липидозы или сфинголипидозы — болезни, приводящие к накоплению сфинголипидов в клетках разных тканей (внутриклеточные липидозы)
2) болезни с нарушением липопротеидов, содержащихся в крови.
Среди наследственных заболеваний, приводящих к накоплению липидов внутри клеток, наиболее изучены болезнь Ниманна—Пика, Гоше и амавротическая идиотия.
Болезнь Ниманна—Пика.Это заболевание связано с накоплением сфингомиелина в мозге, печени, ретикуло-эндотелиальной системе. Сущность нарушения обмена сфингомиелинов состоит в утрате ферментативной активности сфингомиелиназы. Тип наследования аутосомно-рецессивный. В патогенетическом плане заболевание связано с включением в состав сфингомиелина жирных кислот, что не свойственно нормальному сфингомиелии. Атипичный сфингомиелин накапливается в клетках. Заболевание развивается в раннем детском возрасте с отказа от еды, появления рвоты, увеличения живота, печени, селезенки (рис. 14). У таких больных отмечаются мышечная слабость, судороги, снижается слух и зрение. На глазном дне у 20—30 % детей отмечается пятно вишневого цвета. В анализах крови — анемия, тромбоцитопения, вакуолизированные лимфоциты, увеличение холестерина, лецитина, сфингомиелина Прогноз заболевания неблагоприятный. Дети погибают в раннем возрасте.
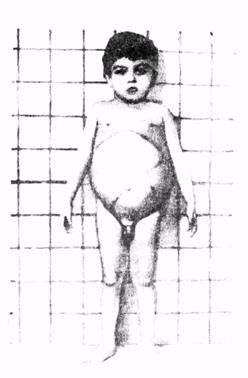
Рис. 14 Внешний вид ребенка с болезнью Ниманна-Пика.
Болезнь Гоше.При этом заболевании в клетках нервной, ретикулоэндотелиальной системы накапливаются цереброзиды. В основе болезни Гоше лежит утрата активности фермента глюкоцереброзидазы, приводящая к накоплению в клетках ретикуло-эндотелиальной системы глюкоцереброзида. Различают детскую и ювенильную формы. В пунктате костного мозга, селезенки находят крупные клетки Гоше. Накопление цереброзидов в клетках нервной системы приводит к их разрушению.
Детский тип проявляется в первые месяцы жизни задержкой умственного и физического развития, увеличением живота, печени и селезенки, развитием Дыхательной недостаточности (инфильтрация легких клетками Гоше), гипертонией мышц, наблюдаются судороги и ребенок погибает на первом году жизни.
Ювенильная форма поражает детей различных возрастов, и заболевание носит хронический характер. В клинической картине отмечаются анемия, спленомегалия, пигментация кожи (коричневые пятна), остеопороз, переломы и деформация костей. Развитие иммунодефицитных состояний приводит к смерти.
Амавротическая идиотия(болезнь Тей—Сакса). Это заболевание связно с резким увеличением в клетках мозга, а также печени и селезенки ганглиозидов из-за дефицита гексозаминидазы А в организме.
При рождении и в первые 3—4 месяца жизни дети не отличаются от здровых сверстников. Заболевание развивается медленно, ребенок становится менее активным, теряет приобретенные навыки. Рано появляются расстройства зрения, слуха. Психические изменения прогрессируют вплоть до идиотии. Развивается гипотония мышц, возникает паралич конечностей. Часто бывают тонические судороги.
Диагноз основывается на определении активности гексозаминидаз, типичных изменениях глазного дна (атрофия сосков зрительных нервов, вишнево-красное пятно в макулярной области). Несмотря на лечебные мероприятия, прогноз неблагоприятный.
НАСЛЕДСТВЕННЫЕ ЗАБОЛЕВАНИЯ ОБМЕНА СТЕРОИДОВ
Образование кортикостероидов имеет сложный ферментативный путь. Из коры надпочечников выделено более 40 соединений, однако в кровь поступает только несколько гормонов: гидрокортизон, альдостерон, кортикостерон и небольшое количество андрогенов и эстрогенов. На промежуточном пути образования кортикостероидов могут возникать различные ферментативные блоки, что приводит к развитию заболеваний.
Адреногенитальный синдром (АГС). Развивается в результате наследственного дефекта фермента 21-гидроксилазы, приводящего к нарушению биосинтеза гормонов коры надпочечников. Распространенность мутантного гена в популяции составляет 1:20—50. Тип наследования данного заболевания аутосомно-рецессивный. В клинической картине выделяют три формы: сольтеряющую, вирильную и форму с гипертензией.
Сольтеряющая форма развивается в первые недели жизни. Проявляется отказом ребенка от груди, рвотой, а иногда и учащением стула, что способствует значительному обезвоживанию организма. При этом у ребенка могут развиться коллаптоидное состояние, судороги, нарушение сердечной деятельности, что приводит к летальному исходу. Лабораторное исследование сыворотки крови выявляет гипонатриемию, гипохлоремию и гиперкалиемию, Дифференциально-диагностическое значение имеет гиперкалиемия, так как при пилоростенозе, кишечном токсикозе с эксикозом всегда отмечается низкий уровень калия в сыворотке крови. У новорожденных девочек отмечается различная степень маскулинизации от умеренной гипертрофии клитора до полного срастания губно-мошоночных складок с формированием мошонки Внутренние половые органы таких больных сформированы правильно, кариотип — 46ХХ. Отмечается гиперпигментация околососковой и генитальной областей. У мальчиков основным клиническим симптомом является преждевременное половое развитие, закрытие зон роста эпифизов, в связи с чем, больные имеют низкий рост. Во всех случаях отмечается повышение в моче уровня 17-кетостероидов. Если таким больным не оказывается правильная и своевременная терапевтическая помощь (введение гидрокортизона, физиологического раствора), то заболевание заканчивается смертью. На вскрытии помимо общего истощения, обезвоживания, специфичным является обнаружение увеличенных надпочечников.
Вирильная форма АГС развивается вследствие избыточного образования андрогенов при недостатке гидрокортизона. Значительное увеличение клитора, полового члена, оволосение по мужскому типу характеризуют эту форму АГС, которая может наблюдаться у детей младшего и дошкольного возраста. Истинное половое развитие задерживается, так как андрогенные гормоны тормозят секрецию гонадотропина гипофизом и половые железы не развиваются.
Гипертоническая форма имеет такую же клиническую картину, как и вирильная, но сопровождается увеличением артериального давления, гипертрофией левого желудочка, что ведет в последующем к изменению в сосудах, поражению почек. Лабораторные исследования выявляют повышение экскреции с мочой 17-оксикортикостероидов и 17-гидроксикортикостероидов, снижение в крови кортизола и альдостерона.
НАСЛЕДСТВЕННЫЕ НАРУШЕНИЯ БИОСИНТЕЗА ТИРЕОИДНЫХ ГОРМОНОВ
Гипотиреоз. Это заболевание, обусловленное понижением функции щитовидной железы. Оно может развиться вследствие поражения щитовидной железы — первичный гипотиреоз, поражения гипоталамо-гипофизарной области, регулирующей тиреоидную функцию, — вторичный гипотиреоз. Гипотиреоз может быть как врожденный, так и приобретенный.
Первичный врожденный гипотиреоз чаще возникает в результате внутриутробного порока развития щитовидной железы (аплазия, гипоплазия и др.) или из-за генетического дефекта в синтезе тиреоидных гормонов.
Больные дети рождаются с большой массой тела, что связано с отеком тканей. После рождения у ребенка длительно держится желтуха. Они плохо растут и имеют малую прибавку массы тела, отстают в нервно-психическом развитии, отмечаются запоры. Кожа при гипотиреозе сухая, бледная, шелушащаяся, холодная на ощупь. Частота сердечных сокращений ниже нормы, границы сердца расширены. У многих больных имеется систолический шум. Отмечаются грубый голос и скудный рост волос на голове. Рентгенологическое исследование костей запястья выявляет отставание костного возраста.
Для диагностики используют исследование в крови гормонов щитовидной железы (тироксина и трийодтиронина), а также тиреотропного гормона гипофиза. Вспомогательное значение имеет повышение уровня холестерина в крови (более 6,8 ммоль/л).
Гипотиреоз может быть и у взрослых людей, клиническими проявлениями которого служат заторможенность, гиподинамия, бледность, сухость и отечность кожи, брадикардия, снижение температуры тела, артериального давления. После инфекций, охлаждения, приема снотворных препаратов и проведения оперативных вмешательств может развиться гипотиреоидная (миксематозная) кома.
Наследование гипотиреоза аутосомно-рецессивное.
Лечение гипотиреоза проводят с помощью заместительной терапии препаратами щитовидной железы, начиная с малых доз. Можно использовать и синтетические препараты — тироксин и трийодтиронин. При недостатке тиреотропного гормона используют его синтетический аналог. Гипотиреоидная кома требует неотложных мероприятий, в том числе и введения гидрокортизона.
При своевременной диагностике и адекватной терапии прогноз для больных с гипотиреозом благоприятный.
НАСЛЕДСТВЕННЫЕ БОЛЕЗНИ СОЕДИНИТЕЛЬНОЙ ТКАНИ
Соединительная ткань выполняет в организме опорную, трофическую и защитную функции, обеспечивает постоянство внутренней среды живого организма. Выделяют три компонента соединительной ткани:
а) клеточные элементы,
б) коллагеновые, эластические и ретикулярные волокна,
в) аморфное основное вещество.
Сложная структура соединительной ткани имеет генетическую природу и дефекты ее биосинтеза и распада приводят к развитию различных наследственных заболеваний.
Болезнь Марфана.Это наследственное заболевание, характеризующееся системным поражением соединительной ткани. Тип наследования — аутосомно-доминантный. В развитии этого заболевания имеет значение поражение эластина и коллагена, выражающееся в нарушении внутри- и межмолекулярных связей в этих структурах. Для больных типичны высокий рост, длинные (паукообразные) пальцы, воронкообразная или килевидная грудная клетка, плоскостопие (рис. 15). Нередко встречаются бедренные и паховые грыжи, гипоплазия мышц и подкожной клетчатки, мышечная гипотония. При обследовании выявляются врожденные пороки сердца, а свозрастом развивается расслаивающаяся аневризма аорты. Зрение у таких больных снижено, при осмотре выявляется миопия, отслойка сетчатки, подвывих хрусталика, катаракта, косоглазие. В моче определяется повышенное количество мукополисахаридов и их составных частей, которые играют важную роль в формировании коллагена и эластических волокон.

Рис. 15 Внешний вид больной с синдромом Марфана в возрасте 9 лет:
а – диспропорциональное телосложение, длинные тонкие конечности, узкое лицо;
