Кислотно – основное титрование (алкалиметрия).
ЛЕКЦИЯ № 2.
RESORCINUM.
РЕЗОРЦИН.
 |
ОН
ОН
М – диоксибензол
Получение:
Резорцин является составной частью многих смол и танинов, но получают его синтетически в сульфураторах из бензола. Бензол обрабатывают серной кислотой и затем сплавляют со щелочью, предварительно нейтрализовав бензолдисульфоновую кислоту гашеной известью.
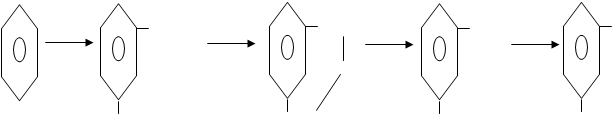
2Н2SO4 OSO2H Ca(OH)2 OSO2 Na2CO3 ONa NaOH OH
Ca
OSO2H OSO2 ONa OH
Свойства:
Резорцин – белый или белый со слабым желтоватым или розоватым оттенком кристаллический порошок, со слабым характерным запахом. Под влиянием света и воздуха постепенно окрашивается в розовый цвет, хорошо растворим в воде, спирте, эфире, мало в хлороформе.
Подлинность:
- УФ спектр.
- При добавлении к раствору резорцина раствора железа хлорида (III) образуется сине – фиолетовое окрашивание, переходящее от добавления раствора аммония гидроксида в буровато – желтое.
- При сплавлении резорцина с фталевым ангидридом в присутствии конц. серной кислоты и затем при растворении сплава в щелочи образуется красновато – коричневый раствор с зеленой флуорисценцией.
- Температура плавления. От 109 до 1120 С.
Чистота:
- Определяют сульфатную золу, не более 0,1%
- Не должно быть примесей пирокатехина, фенолов
- Потеря в массе при высушивании
- Микробиологическая чистота
- Раствор д. б. бесцветным и прозрачным
- рН от 5,0 до 6,5
Количественное определение:
Метод броматометрии: точную навеску препарата помещают в мерную колбу, вместимостью 100 мл, растворяют в воде и доводят объем раствора водой до метки. Точный объем полученного раствора переносят в склянку для бромирования, прибавляют 0,1 М р-ра калия бромата, р-ра калия бромида, 50% р –ра кислоты серной, перемешивают и оставляют на 15 минут. Затем к смеси прибавляют раствора калий йодида, смесь сильно взбалтывают и оставляют на 10 минут в темном месте. Выделившийся йод титруют 0,1 М р-ром натрия тиосульфата, индикатор 1 мл раствора крахмала.
 KBrO3 + 5KBr + 6HCI 3Br2 + 6HCI + 3H2O
KBrO3 + 5KBr + 6HCI 3Br2 + 6HCI + 3H2O
 Br
Br
 | |||
 | |||
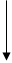 OH + 3Br2 OH
OH + 3Br2 OH

- 3HBr


Br Br
OH OH
 Br2 + 2KI I2 + 2KBr
Br2 + 2KI I2 + 2KBr
 I2 + 2Na2S2O3 2NaI + Na2S4O6
I2 + 2Na2S2O3 2NaI + Na2S4O6
Мr Т • (V1K1 – V2K2) • 100 • A

 Э = 6 Х = а • А1
Э = 6 Х = а • А1
Применение:
Антисептическое средство при кожных заболеваниях в виде мазей, паст.
Внутрь – для дезинфекции желудка, кишечника.
Хранение:
Сп. Б. В сухом, защищенном от света месте. Срок годности 3 года.
АРОМАТИЧЕСКИЕ КИСЛОТЫ.
КИСЛОТА БЕНЗОЙНАЯ.
ACIDUM BENZOICUM.
 СООН
СООН
 |
Бензойная кислота получила свое название от бензойной смолы, из которой она была впервые выделена в 1608г. Содержится в смоле до 80%. В1775г фармацевт Шееле получил эту кислоту, обрабатывая смолу щелочами. Небольшое количество ароматических кислот содержится в ягодах, плодах, коре некоторых растений, а также в смолах, камедях, бальзамах.
Получают синтетически.
Современный способ получения основан на окислении толуола различными окислителями: азотная кислота, хромовая кислота, диоксид марганца.
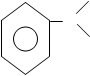
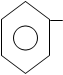
 1. O
1. O
СН3 C
 +3MnO2 + 3H2SO4 OH + 3MnSO4 +4H2O
+3MnO2 + 3H2SO4 OH + 3MnSO4 +4H2O
2. Окисление кислородом воздуха в жидкой фазе.
 |  |
СН3 СООН
 3О2 2 2Н2О
3О2 2 2Н2О
Описание:
Бесцветные игольчатые кристаллы или белый мелкокристаллический порошок. Мало растворим в воде, растворим в кипящей воде, легко растворим в спирте, хлороформе, эфире и бензоле. Растворим в жирных маслах.
При нагревании возгоняется. Перегоняется с водяным паром.
Подлинность:
- С железа хлоридом.
 Кислоту бензойную растворяют в 0,1 н растворе едкого натра (реакция раствора д.б. нейтральной), образуется нерастворимый в воде основной бензоат железа розовато- желтого цвета.
Кислоту бензойную растворяют в 0,1 н растворе едкого натра (реакция раствора д.б. нейтральной), образуется нерастворимый в воде основной бензоат железа розовато- желтого цвета.

 O
O
 COONa C
COONa C
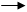 6 + 2 FeCL3 + 10H2O O- Fe * Fe(OH)3 * 7 H2O
6 + 2 FeCL3 + 10H2O O- Fe * Fe(OH)3 * 7 H2O
 |
COOН
3 + 6 NaCL
2) t о плав. 122 –124,5 оС.
Чистота:
Проверяют наличие примесей восстанавливающих веществ, фталевой кислоты.
Хлориды, сульфаты , тяжелые металлы в пределе ГФ Х.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ:
Кислотно – основное титрование (алкалиметрия).
Метод основан на кислых свойствах препарата.
Точную навеску растворяют в нейтрализованном по ф/ф спирте и титруют 0,1 н р-ром натрия гидроксида, индикатор ф/ф до розового окрашивания.
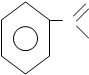
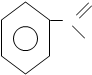 O O
O O
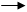 C + NaOH C + H2O
C + NaOH C + H2O
OH ONa
Э = Mr
Хранение:
В хорошо укупоренной таре т. к. бензойная кислота возгоняется.
Применение:
Антисептическое средство.
Наружно – антипаразитарное.
НАТРИЯ БЕНЗОАТ.
NATRII BENZOAS.
 |
COONa
Получение:
При нейтрализации бензойной кислоты раствором карбоната натрия.
 | |||||
 | |||||
 | |||||
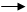 COOH + Na2CO3 COONa + H2O + CO2
COOH + Na2CO3 COONa + H2O + CO2
2 2
Описание:
Белый кристаллический или аморфный порошок без запаха или с очень слабым запахом. Легко растворим в воде, умеренно растворим в спирте 90 о. Практически нерастворим в эфире и хлороформе.
Подлинность:
- Бензоат – ион см. бензойную кислоту.
- Определяют ультрафиолетовый спектр препарата.
- Na+ - окрашивает пламя в желтый цвет.
- Препарат растворяют в воде, прибавляют азотную кислоту, выделившиеся белые кристаллы отфильтровывают, промывают водой и высушивают до постоянного веса, определяют температуру плавления (ГФ Х).
Чистота:
